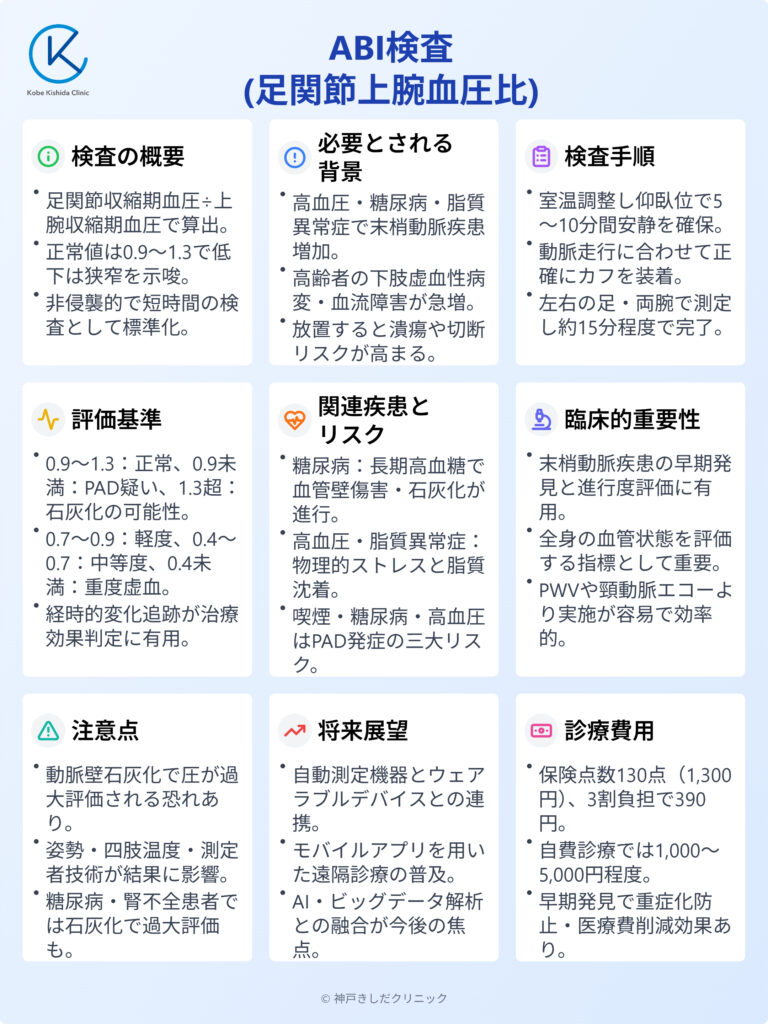
足関節上腕血圧比(ABI)は、下肢の動脈血流状態を把握するために用いられる基本的かつ重要な検査です。
近年、高齢化の進行や糖尿病・高血圧・脂質異常症など生活習慣病の増加に伴い、末梢動脈疾患(PAD)の早期発見と予防の重要性が広く認識されるようになりました。
ABI検査は比較的簡便に行え、非侵襲的な手法で足の血流障害を評価できるため、患者さんに大きな負担をかけずにリスクを見極めることができます。
本記事では、ABI検査の基本的な知識や検査手順、結果の解釈、関連疾患とのつながりから最新の研究動向までを幅広く解説します。
神戸きしだクリニック公式Youtubeチャンネルでの音声解説はこちら。
1. ABI検査の概要
1.1. ABI検査とは
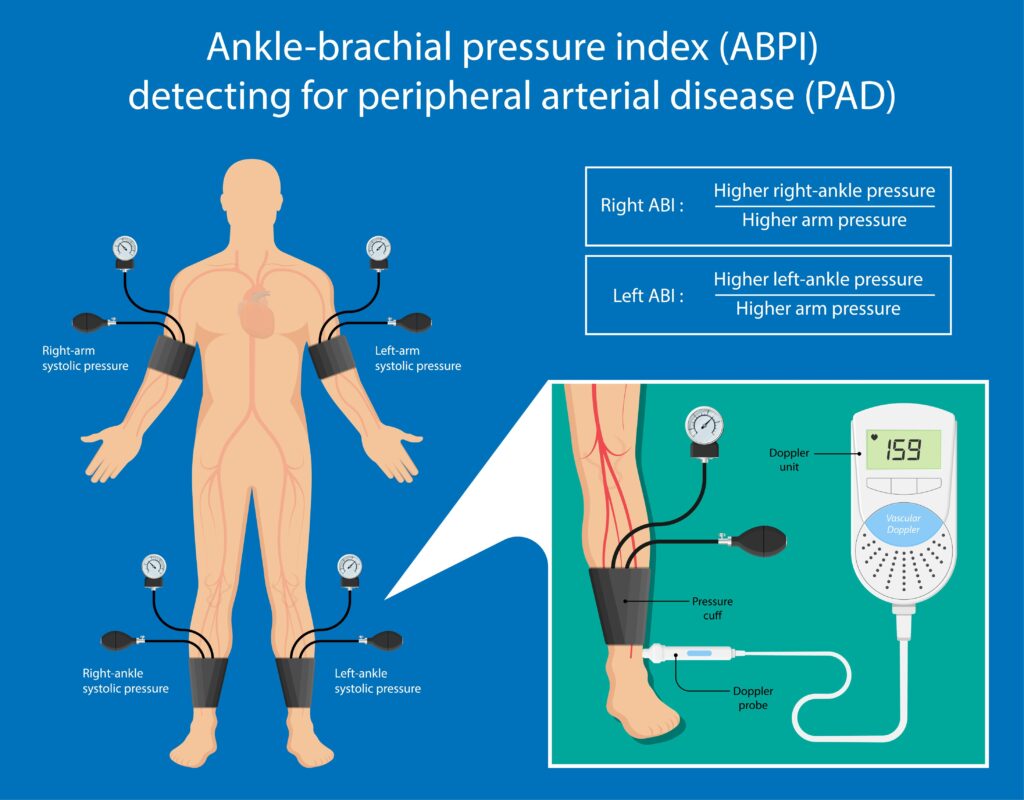
ABI(Ankle-Brachial Index)検査とは、足関節部と上腕部の収縮期血圧を比較することで末梢血流状態を評価する検査です。
一般的には、仰臥位の患者さんの上腕と足関節に血圧計またはドップラー測定機器を装着し、足関節収縮期血圧を上腕収縮期血圧で割った値がABIとなります。
正常範囲は0.9~1.3とされ、この値が低下すると下肢動脈の狭窄や閉塞の可能性を示唆します。末梢動脈疾患(PAD)のスクリーニングや重症度評価を行う上で、医療現場において重要な位置を占める検査の一つです。
1.2. 歴史と開発の経緯
ABI検査のルーツは、末梢血流障害の診断に用いられていたさまざまな手法の中から、より簡便に圧力差を数値化する試みとして発展してきました。
1960年代にはドップラー機器の実用化が進み、血流信号を耳で聴取するだけでなく波形や血圧を定量的に把握する方法が確立されました。
その後、非侵襲的で、かつ検査の所要時間が短いことから、ABIは世界的に末梢動脈疾患の初期スクリーニング検査として標準化され、ガイドラインにも広く推奨されるようになりました。
1.3. 検査機器と原理
ABI検査には主に、カフ(血圧計のマンシェット)とドップラー型超音波装置または専用の自動測定装置が使用されます。
ドップラー方式の場合は、足関節にカフを巻き、ドップラー探触子を足背動脈や後脛骨動脈の上に当てて血流音を確認しながらカフ圧を調節し、血流が消失する点と再び流れ始める点を測定して収縮期血圧を読み取ります。
上腕部でも同様に測定し、その比率を求めることでABI値を算出します。この原理は「血液流動音の変化とカフ圧の比較」という非常にシンプルな仕組みに基づいており、熟練した技術や高額な装置を必要としません。
1.4. 臨床的な重要性
ABI検査は、末梢動脈疾患の疑いがある患者を早期に見つけるだけでなく、病状の進行度合いを把握する上でも欠かせない検査です。
重症例では潰瘍や壊疽などを防ぐために早期の治療介入が必要であり、その判断材料としてABIの測定は非常に有用です。
また、ABIは下肢だけでなく全身の血管状態の指標として捉えられることも多く、冠動脈疾患や脳血管障害のリスク評価においても意味を持ちます。
さらに、ABIの変化を追うことで、運動療法や薬物療法の効果判定や、血行再建術後の経過観察にも活用されます。
1.5. 他の血管機能検査との比較
ABI検査以外にも、血管機能を評価する方法としては脈波伝播速度(PWV)や頸動脈エコー検査、Toe-Brachial Index(TBI)などがあります。
それぞれに特徴がありますが、ABIは実施のしやすさ・費用対効果・リスク評価の統合性など多角的に評価すると、非常に優位性が高い手法です。
特に、重症下肢虚血(CLI)の診断や治療方針の決定においては、初期段階ではまずABI検査を行うことがガイドラインでも推奨されています。
(表1:ABI検査とその他の血管検査の比較例)
| 検査名 | 評価対象 | メリット | デメリット |
|---|---|---|---|
| ABI | 下肢動脈 | 簡便かつ短時間で測定可能 | 動脈硬化が高度な場合、過大評価の可能性あり |
| PWV | 動脈スティフネス | 動脈硬化度を定量評価 | 専用機器が必要 |
| 頸動脈エコー | 頸動脈プラーク | 詳細な形態評価が可能 | 検査技師の熟練度に依存 |
| TBI | 下肢末端(足趾) | 末端血流をより正確に評価 | 測定がやや煩雑 |
- ABIはスクリーニング検査として優先度が高い
- 他検査と併用することで精度向上が期待できる

2. ABI検査が必要とされる背景
2.1. 生活習慣病の増加と下肢血管障害
近年、高血圧や糖尿病、脂質異常症といった生活習慣病が世界的に増加し、それに伴い末梢動脈疾患の有病率も上昇しています。
下肢の血管障害は無症候性のケースも多く、歩行距離の短縮や下肢の冷感・しびれなどに気づかず進行してしまうことが少なくありません。
ABI検査はこうした初期病変を見逃さないための有用なツールとして重要視されているのです。
2.2. 高齢化と下肢虚血の増加
日本をはじめとする先進国を中心に高齢化が進むにつれ、下肢の虚血性病変や血流障害を起こす患者数が急増しています。
動脈硬化は加齢とともに進行しやすく、もともと生活習慣病を抱えている方の場合はさらにリスクが高まります。
そういった背景から、高齢者の健康診断や人間ドックでもABI検査が組み込まれるケースが増え、予防的な視点での血管チェックが重視されています。
2.3. 末梢動脈疾患(PAD)の早期発見・早期治療
末梢動脈疾患は、適切な検査と治療が行われないまま放置されると、重度の下肢虚血や潰瘍、最悪の場合は切断に至ることもあります。
また、PAD患者は心血管イベントのリスクも高いことが知られており、心筋梗塞や脳卒中など重大な合併症の発症予防にもつながります。
ABI検査は早期スクリーニングにおいてコストパフォーマンスが高く、多くのガイドラインで推奨されている手法です。
2.4. 医療費抑制の観点
治療の遅れによる重症化は、患者さんの生活の質(QOL)を大きく低下させるだけでなく、長期的には医療費の増大を招く可能性があります。
ABI検査を積極的に導入して早期にリスクを把握し、適切な治療プランを立案することは、医療経済的な観点からも大きな意義があります。
特に、高齢者人口の増加が予測される社会においては、予防医療や早期発見・早期治療の取り組みが重要な政策課題の一つとなっています。
2.5. ガイドラインにおける推奨度
欧米を中心とした血管外科学会や循環器学会などのガイドラインでも、ABI検査は末梢動脈疾患を疑うすべての患者さんに対して推奨される基本的な検査として位置付けられています。
加えて、危険因子(喫煙、糖尿病、高血圧、高コレステロール血症など)を複数抱える患者の場合は、ABIの定期的測定が合併症の予防と早期治療につながるとの報告もあり、総合的なリスク管理の一環としても注目されています。
(表2:ABIが推奨される主なガイドライン例)
| ガイドライン名 | 推奨される対象 | 推奨度 |
|---|---|---|
| ACC/AHA PADガイドライン | 下肢虚血を疑う患者全般 | Class I |
| ESCガイドライン | 糖尿病・喫煙者など高リスク群 | Class I |
| JCSガイドライン | 血管疾患疑いの中高齢者 | 推奨度A |
- 早期発見はQOL維持と医療費抑制に直結する
- ガイドラインでもABI検査は最優先で推奨

3. ABI検査の手順と注意点
3.1. 検査準備と環境設定
ABI検査を行う前には、検査環境を整え、患者さんがリラックスできる状況を作ることが大切です。室温を適度に保ち、仰臥位で5~10分程度安静にしてもらったうえで測定を開始します。
衣類やアクセサリーが血圧計のカフの巻き付けを妨げないよう、必要に応じて脱衣を行い、検査に集中できる状態を作ります。
また、喫煙や運動直後などは血管の収縮・拡張が大きく変動するため、測定の30分前くらいまでには控えるよう指導することが望ましいです。
3.2. 上腕と足関節のカフ装着
上腕部と足関節(足背動脈、後脛骨動脈付近)にカフを巻きます。カフは動脈の走行に合わせて正しく装着し、過度な緊張が生じないよう注意します。
足関節の場合、足首よりやや上部に巻き、ドップラー探触子を動脈の拍動が強く聴取できる部位に当てて測定を行います。
特に末梢循環が悪い患者さんの場合は、血流音の聴取が困難な場合もあるため、予備測定や部位の微調整を慎重に行います。
3.3. ドップラーを用いた収縮期血圧の測定
ドップラー探触子を血管に当てたまま、カフを徐々に膨らませていきます。
血流音が消失した後、ゆっくりと空気を抜きながら血流音が再び聴こえ始めるタイミングのカフ圧を読み取ることで、収縮期血圧を測定します。
足関節と上腕部の収縮期血圧をそれぞれ2回以上測定し、平均値をとることでより正確な値を得るようにすることが一般的です。この作業を左右の足関節と上腕部で行い、四肢の測定データを総合的に評価します。
3.4. ABI値の算出と検査時間
ABIは足関節の収縮期血圧を上腕の収縮期血圧で割って算出されます。通常、片側の測定は5分程度で完了するため、両足および両腕を合わせても比較的短時間で検査が完了します。
患者さんの状態によっては測定にやや時間がかかることもありますが、非侵襲的で痛みもほとんどないため、苦痛の少ない検査といえます。
安静状態を保ちながら行うので、急な姿勢変換や精神的ストレスを避けるように配慮が必要です。
3.5. 注意点と検査結果の誤差要因
ABI検査は簡便な一方で、いくつかの要因によって測定誤差が生じる可能性があります。動脈壁が石灰化している重症の糖尿病患者の場合、足関節で血圧が過大評価される可能性があります。
また、測定時の患者さんの姿勢、四肢の温度、測定者の熟練度なども結果に影響を及ぼします。
検査結果を解釈する際は、可能な限り複数回測定し平均化すること、そして患者個人の背景や臨床症状を総合的に加味することが重要です。
(表3:ABI検査手順のポイント)
| ステップ | 内容 | ポイント |
|---|---|---|
| 1. 準備 | 仰臥位で5分安静 | 運動・喫煙を30分前までに控える |
| 2. カフ装着 | 上腕・足関節に巻く | 動脈の走行を確認して正確に装着 |
| 3. ドップラー測定 | 血流音を確認 | 血流音が消失、再開する圧を正確に読む |
| 4. 値の算出 | 足関節圧 ÷ 上腕圧 | 0.9~1.3が正常範囲 |
- 重症の石灰化などでは過大評価のリスク
- 平均化・複数回測定で精度を高める

4. ABI検査結果と評価基準
4.1. 正常値と異常値の目安
一般的に、ABIの正常値は0.9~1.3の範囲とされています。0.9未満の場合は下肢動脈の狭窄・閉塞を示唆し、末梢動脈疾患が疑われます。
一方、1.3を超える場合は、動脈壁の石灰化などによる血管の硬化が進んでいる可能性があり、測定値が実際よりも高く出ていると考えられます。
したがって、単純に「高い=良い」と判断するのではなく、患者さんの背景や臨床症状との組み合わせで慎重に評価する必要があります。
4.2. 軽度・中等度・重度の分類
ABI値は、狭窄や閉塞の重症度を評価する上でも用いられます。
多くのガイドラインでは、0.4~0.9の範囲が軽度~中等度のPADを疑う領域とされ、特に0.4未満の場合は重症虚血の可能性が高いと判断されます。
重症例では安静時疼痛や潰瘍が生じることもあり、迅速な血行再建や外科的治療を含む総合的な対応が求められます。
4.3. 狭窄率との相関と限界
ABI値が低いほど狭窄率が高い傾向があるものの、実際の血流障害の程度は個人差が大きいため、必ずしもABI値だけで臨床像を断定できるわけではありません。
さらに、糖尿病患者や末期腎不全患者では動脈硬化と石灰化が進行し、逆にABI値が虚血の実態を反映できないケースも存在します。
こうした場合、Toe-Brachial Index(TBI)や下肢血管造影などの追加検査が必要となることがあります。
4.4. 経時的変化の重要性
ABI値は一度の測定結果だけでなく、経時的な変化を追うことが大切です。
運動療法や生活習慣の改善、薬物治療によってABIが改善したり、逆に悪化の兆候がみられたりすることで治療効果や疾患進行度を客観的に把握できます。
患者さんにも検査結果をわかりやすくフィードバックすることで、治療へのモチベーション向上につながるケースも多く見られます。
4.5. 臨床現場での具体的な活用例
ABI検査結果は、日常診療のさまざまな場面で活用されています。
例えば、健診やドックでABI値が低かった場合には、早期に専門医へ紹介し、カテーテル検査などを行って虚血の有無を確かめる手順が一般的です。
また、血行再建術後のフォローアップとしてABIを定期測定することで、再狭窄の兆候を見逃さずに対応できます。
加えて、複数の危険因子を持つ患者さんにおいては、ABI測定を組み合わせた総合的なリスク評価が有効です。
(表4:ABI値と末梢動脈疾患の重症度)
| ABI値 | 判定 | 対応 |
|---|---|---|
| 1.3超 | 石灰化の可能性:追加検査要 | TBIや血管エコーを検討 |
| 0.9~1.3 | 正常範囲 | 定期観察を推奨 |
| 0.6~0.9 | 軽度~中等度の狭窄:PAD疑い | 専門医受診を推奨 |
| 0.4~0.6 | 中等度~重度の狭窄:潰瘍リスク | 血行再建など検討 |
| 0.4未満 | 重度虚血:切断リスク | 迅速な治療介入 |
- 1.3超は石灰化の影響を考慮
- 定期的なフォローアップで経時的変化を把握

5. ABI検査に関連する疾患とリスク要因
5.1. 糖尿病と下肢血管合併症
糖尿病は、長期にわたり血糖値が高い状態が続くことで血管壁が傷害され、末梢血管の狭窄や閉塞を引き起こしやすい疾患です。
特に重症化すると微小血管とともに大血管にも障害が及び、ABI検査で値の低下が認められることが多くあります。
ただし、石灰化が進行すると逆にABIが1.3を超えてしまう場合もあるため、糖尿病患者ではTBIの併用が推奨されるケースが増えています。
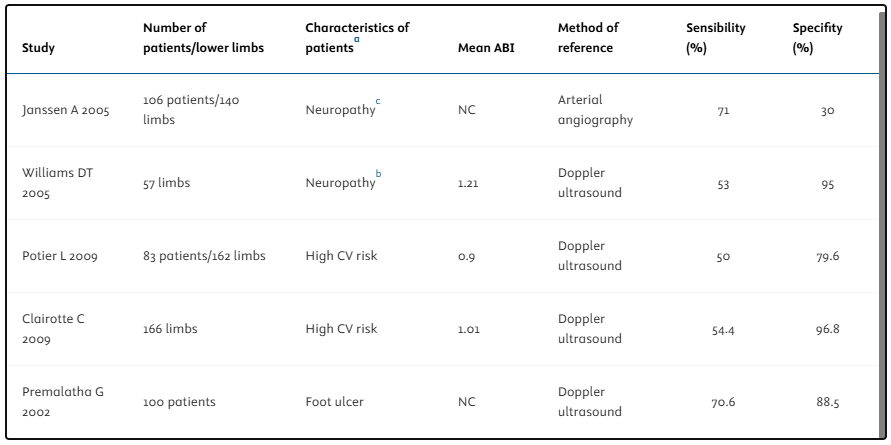
所見:「糖尿病患者における足関節上腕血圧比(ABI)の診断効率は、高心血管(CV)リスク、神経障害、腎症、および足病変を有する患者において限定的である可能性がある。その理由として、感度の低さと異常に高い正常値の割合(表2参照)が挙げられ、これは動脈内膜中膜石灰化(MAC)の高い有病率による可能性が示唆される。ABIの診断効率向上の一手段として、閾値を1〜1.1程度に引き上げる、または足関節収縮期血圧の最小値を用いて計算する方法が考えられる。しかし、MACが存在する場合には、BrooksらによりABIよりも足趾血圧測定の方が感度が高いことが示されている[61]。同様に、国際糖尿病足合意(ICDF)ガイドラインに基づき診断された臨床的末梢神経障害を有する場合、足趾血圧の感度は100%であったのに対し、ABIの感度は53%にとどまった。したがって、MACリスクが高い患者(臨床的神経障害、腎症、長期糖尿病罹患)では、ABIの解釈には注意を要し、正常値であっても末梢動脈疾患(PAD)の除外には不十分である。足関節レベルの動脈は足趾レベルよりも石灰化の頻度が高いため、高感度な足趾血圧測定などの代替評価法が推奨される。今後、より具体的な推奨を提供するための追加研究が必要である。」
5.2. 高血圧・脂質異常症による動脈硬化
高血圧や脂質異常症は、動脈硬化を進行させる代表的な疾患です。長期間にわたる血圧の上昇は血管壁に物理的なストレスを与え、脂質の沈着とあわせて血管内腔を狭窄させます。
ABI値が低下している場合は、下肢だけでなく冠動脈や頸動脈でも動脈硬化が進んでいる可能性が高く、包括的な血管評価とリスクファクター管理が必要となります。
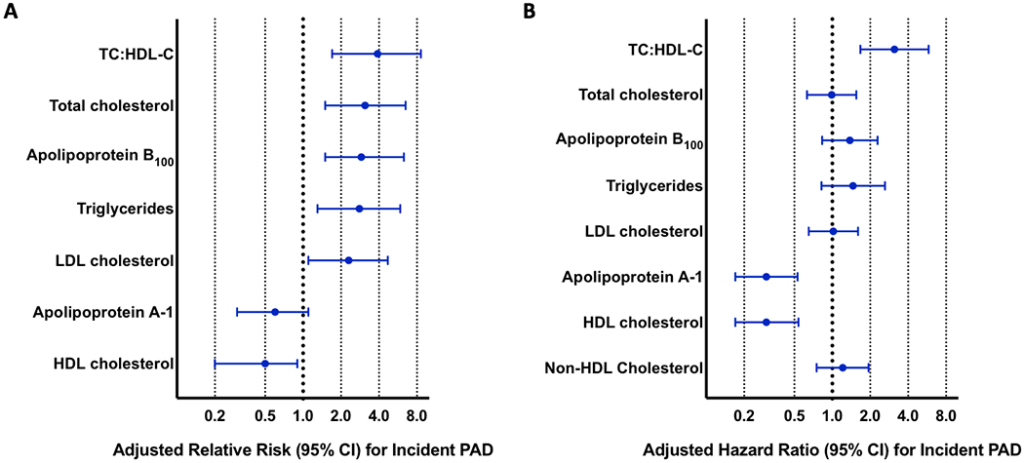
所見:「(A) 医師健康研究における標準的脂質指標およびアポリポタンパク指標と新規発症末梢動脈疾患(PAD)とのリスク関連を示す。標準的脂質およびアポリポタンパク指標の上位四分位群と下位四分位群の相対リスクおよび95%信頼区間を算出し、年齢、喫煙、糖尿病、高血圧、早期動脈硬化の家族歴、運動頻度、体格指数(BMI)で調整した。(B) 女性健康研究における標準的脂質指標およびアポリポタンパク指標と新規発症PADとのリスク関連を示す。標準的脂質およびアポリポタンパク指標の上位三分位群と下位三分位群のハザード比および95%信頼区間を算出し、年齢、喫煙(パックイヤー)、メタボリックシンドローム、高血圧、ホルモン療法、高感度C反応性タンパク(hs-CRP)、脂質低下療法、無作為化治療群、BMIで調整した。PAD:末梢動脈疾患、TC:HDL-C:総コレステロール/高比重リポ蛋白コレステロール比、LDL:低比重リポ蛋白。」
5.3. 喫煙と末梢血管障害
喫煙は動脈硬化を促進する要因の一つであり、末梢動脈疾患の発症リスクを大幅に高めることが知られています。タバコに含まれるニコチンや一酸化炭素は血管内皮機能を低下させ、動脈硬化を進行させます。
そのため、喫煙者のABI値が低く出る場合は、喫煙習慣の改善指導を行うとともに、血行再建術や薬物療法が必要かどうかを総合的に評価することが重要です。
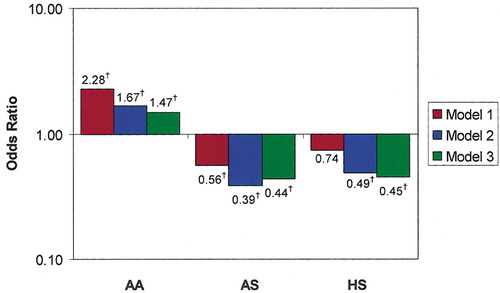
所見:「新規リスク因子を追加した解析においても、民族別の末梢動脈疾患(PAD)のオッズ比(OR)は統計的に有意な関連を示した。年齢、性別、民族、従来のリスク因子、および新規リスク因子を調整後、PADのORはアフリカ系アメリカ人で1.47(95%信頼区間[CI]: 1.07–2.02)に低下したが、ヒスパニック(OR = 0.45, 95% CI: 0.29–0.70)および中国系(OR = 0.44, 95% CI: 0.24–0.78)ではほぼ変化しなかった。図は、異なるリスク因子カテゴリの影響を調整した後の民族別PADオッズ比を示す。(1) 年齢・性別・民族で調整、(2) モデル1に加えて喫煙、糖尿病、高血圧、脂質異常症、BMI、教育歴、収入を調整、(3) モデル2に加えてインターロイキン-6、フィブリノーゲン、D-ダイマー、ホモシステインを調整。図1の解析では、非ヒスパニック系白人を基準群とし、PADの民族別オッズ比を比較している。(†p<0.05)」
5.4. 腎不全と血管石灰化
末期腎不全の患者さんは、カルシウムやリンの代謝異常により血管石灰化が進行しやすいことが知られています。
石灰化によって動脈壁が硬化すると、実際には血流が悪いのにカフで測定すると高い血圧値が得られてしまうことがあり、ABIが1.3以上になってしまうケースも珍しくありません。
こういった背景を考慮して、腎不全を抱える患者さんには追加検査や専門的な血管評価が求められます。
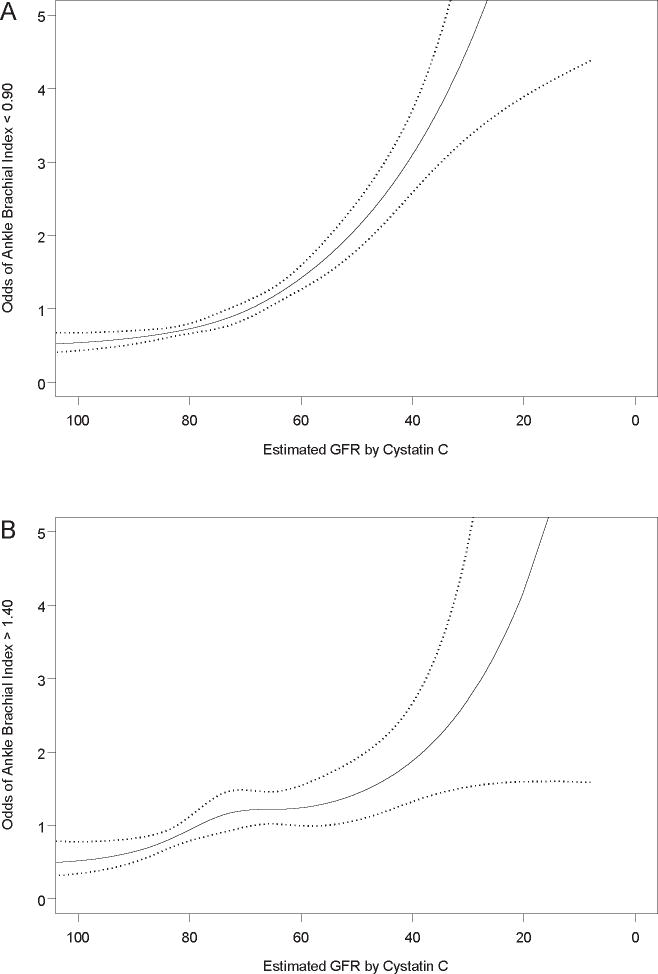
所見:「慢性腎疾患(CKD)の重症度と足関節上腕血圧比(ABI)との関連を評価するため、腎機能を連続変数として低ABIおよび高ABIとの関連を解析した。全体として、腎機能の早期低下段階では緩やかな線形関連を認めたが、推算糸球体濾過率(eGFR)80 ml/min/1.73m²未満の群では、この関連がより急峻になる傾向を示した(図)。この図はナチュラルキュービックスプライン関数を用いた解析を示す。実線は相対リスクを表し、点線は95%信頼区間を示す。本スプライン関数は、年齢、性別、人種/民族、高血圧、糖尿病、喫煙、BMI、LDL、HDL、およびCRPを調整した。」
5.5. その他のリスク要因
家族歴や遺伝的要因による血管リスクも無視できません。加齢による生理的変化に加え、肥満、運動不足など生活習慣面の影響も大きいといわれています。
また、慢性炎症を伴うリウマチ性疾患なども動脈硬化の進行を加速させることが報告されています。したがって、ABI検査を行う際は、単にABI値のみではなく、患者さんの多面的なリスクファクターを総合的に把握することが重要です。
(表5:主な疾患・リスク要因とABIの関係)
| 疾患・要因 | ABIへの影響 | 備考 |
|---|---|---|
| 糖尿病 | 石灰化による過大評価 or 低下 | TBI併用を推奨 |
| 高血圧 | 動脈硬化進行で低下 | 心血管リスク増大に注意 |
| 喫煙 | 血管内皮機能障害で低下 | 禁煙指導の徹底 |
| 腎不全 | 石灰化による過大評価 | 追加検査で正確な評価を行う |
| 脂質異常症 | 動脈硬化進行で低下 | LDLコレステロール管理が重要 |
- 多因子が絡むため、総合的な管理が必須
- 石灰化の有無を判断する追加検査の重要性
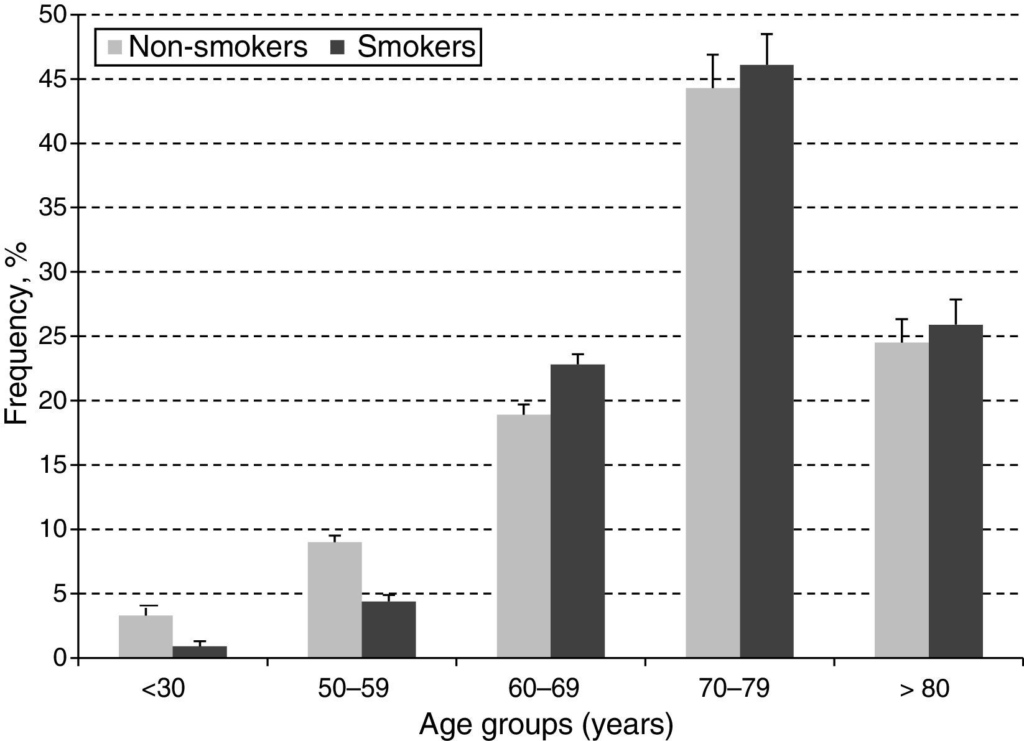
所見:「PAD症例における喫煙頻度を年齢層別に解析した結果(図)、60歳以上の対象者で喫煙率が高い傾向を認めたが、群間の差は統計的に有意ではなかった(p=0.107)。」

6. ABI検査の今後の展望と最新研究
6.1. 自動測定機器の普及
最近では、ドップラー方式だけでなく、カフを自動制御しながら同時に上腕と足関節の血圧を測定できる自動測定機器が普及しつつあります。
このような機器は、測定者の熟練度に依存する部分を減らし、検査精度の向上と検査時間の短縮を実現しています。
さらに、複数部位の血圧を同時に測定できるため、左右差の判定や四肢血流の総合的な比較がスムーズに行えます。
6.2. ウェアラブルデバイスとの連携
近年のヘルスケア分野では、スマートウォッチや活動量計などのウェアラブルデバイスが急速に発展しています。
将来的には、こうしたデバイスと連携してABIを含む末梢血流データを日常的に収集し、異常が検出された際には早期に受診を促すシステムの開発が期待されています。
すでに研究段階では、フォトプレチスモグラフィー(PPG)技術を応用して血流状態を簡易モニタリングする試みが進められており、今後の技術革新が待たれます。
6.3. モバイルアプリを用いた遠隔診療
高齢者人口の増加や医療スタッフの不足が叫ばれる中、遠隔診療のニーズが高まっています。
ABI検査においても、簡易型の測定デバイスを家庭などで使用し、スマートフォンのアプリを通じて医療機関とデータを共有するシステムの開発が進められています。
これにより、地理的条件や身体的制約がある患者さんでも定期的にABIを測定し、異常値が出れば迅速に医師の診断を仰ぐことが可能となります。
6.4. 他のバイオマーカーとの組み合わせ
ABI単独では把握しきれない血管リスクを、他のバイオマーカーや画像検査と組み合わせて総合的に評価するアプローチも注目されています。
例えば、頸動脈エコー検査のプラーク評価や血液検査での炎症マーカー、さらには心臓MRIなどを組み合わせることで、より精密かつ個別化された治療プランを立案できる可能性があります。
多角的な評価を行うことで、リスクの見逃しを最小限にする研究が広がっています。
6.5. 研究動向と将来展望
欧米を中心に、ABI値をはじめとする血管評価指標を用いた大規模臨床研究が行われています。
これらの研究では、ABI値が低い患者群での心血管イベント発症率の上昇や、逆にABI値の改善が得られた場合のアウトカム改善効果などが報告されています。
今後は、日本を含めたアジア圏でも同様の大規模データが蓄積されることで、より地域特性に合った診療ガイドラインの構築が進むと期待されます。
(表6:最新研究動向とキーワード)
| 研究テーマ | キーワード | 期待される成果 |
|---|---|---|
| 自動測定機器の精度検証 | コスト効率、標準化 | 臨床での迅速導入と誤差低減 |
| ウェアラブルデバイスとの組み合わせ | PPG、活動量計、AI | 日常的モニタリングと早期発見 |
| 大規模コホート研究でのABI活用 | リスク評価、長期追跡 | 心血管イベントの予測精度向上 |
| 遠隔診療プラットフォームへのABI測定技術統合 | モバイルヘルス、在宅ケア | 医療資源の効率化と患者負担軽減 |
- AIやビッグデータ解析との融合が今後の焦点
- 国際共同研究で地域差を踏まえた標準化が期待

7. 日本国内におけるABI関連の診療費用
1. 保険診療での価格と自己負担額
ABI検査は日本の公的医療保険で算定可能な生理学的検査です。
保険点数は130点と定められており、1点=10円換算で検査費用は1,300円になります。
患者の自己負担額は保険適用時の負担割合によります。
たとえば、一般被保険者(3割負担)の場合は約390円、1割負担の高齢者の場合は約130円の自己負担でABI検査を受けることができます。
なお、この費用には検査に必要な機器や人件費が含まれており、別途初診料や再診料が加算される場合があります。
| 検査種別 | 保険点数 | 検査費用(点数×10円) | 一般被保険者(3割負担) | 高齢者(1割負担) | 備考 |
|---|---|---|---|---|---|
| ABI検査 | 130点 | 1,300円 | 390円 | 130円 | 機器・人件費込み。初診・再診料は別途。 |
2. 自費診療での価格
症状がなく自主的に動脈硬化の評価を希望する場合や、人間ドック・健康診断のオプションとしてABI検査を受ける場合は、保険適用外(自費診療)となります。
自費の場合、料金は医療機関ごとに設定されていますが、概ね数千円程度が多いです。
- あるクリニックではABI検査を3,300円(税込)で提供している例があります。
- 病院の健診オプションでは、1,100円~2,000円前後と比較的安価に設定されているケースもあり、徳洲会グループの健診では1,100~1,650円ほどで追加できる場合もあります。
自費料金は施設により幅があり、おおむね1,000~5,000円未満で受けられることが多いです。
なお、ABI検査は短時間で痛みもなく、動脈硬化のスクリーニングとして希望者に利用されています。
| 検査種別 | 自費診療価格 | 備考 |
|---|---|---|
| ABI検査 | 約1,000~5,000円未満 | 例: クリニック 3,300円、病院健診オプション 1,100~2,000円、徳洲会グループ 1,100~1,650円 |
3. 追加検査が必要な場合の費用
ABI検査で異常が認められた場合、病変の詳細評価のために追加検査が行われることがあります。
代表的な追加検査とその費用目安(保険適用時の点数と自己負担目安)は以下の通りです。
【血管エコー(超音波検査)】
- 下肢動脈の超音波検査は保険点数450点に区分されています。
- 検査箇所により異なりますが、下肢血管エコー1件あたり約4,500円の診療報酬となります。
- 自己負担3割の場合、約1,350円程度の負担となります。
- 超音波検査は非侵襲的で、その場で血流の状態や狭窄の有無を可視化できるため、有用な追加検査です。
【CT検査】
- 下肢のCTアンギオグラフィー(造影CT)などでは、撮影部位や装置性能により点数が決まります。
- 下肢CTアンギオグラフィーとしては、保険点数は1,060~1,500点であり、自己負担は3,180円~4,500円程度が見込まれます。
- 高性能16列以上のマルチスライスCTでは、所定点数がやや上乗せされる場合もあります。
- 自費でCT検査を受ける場合、全額負担で約1.5万円~2万円が相場となる場合もあります。
【MRI検査】
- 下肢動脈のMRI(MRA)は、詳細評価に用いられます。
- MRI撮影料は部位により異なりますが、一般的には1,500~2,000点程度です。
- 下肢のMRAも装置や検査範囲により1,330~1,850点となり、自己負担は約4,000~5,650円程度が見込まれます。
- 自費でMRI検査を受ける場合は、1回あたり数万円(施設により2~3万円以上)の費用がかかることがあります。
| 検査項目 | 保険点数 | 検査費用(点数×10円) | 自己負担額(3割負担) | 備考 |
|---|---|---|---|---|
| 血管エコー(下肢超音波検査) | 450点 | 4,500円 | 1,350円 | 下肢動脈の血流状態・狭窄の有無を評価。 |
| CT検査(下肢CTアンギオグラフィー) | 1,060~1,500点 | 10,600~15,000円 | 3,180円~4,500円 | 部位や装置性能により異なる。 例: 頭部CTは1470点(約14,700円、自己負担約4,410円) |
| MRI検査(下肢MRA~造影MR) | 1,330~1,850点 | 13,330~18,500円 | 約4,000~5,650円 | 自費の場合は施設により2~3万円以上もあり得る。 |
以上のように、ABI検査で異常が認められた場合の追加検査も、保険適用であれば比較的低負担で受けることができます(3割負担であれば、超音波検査からCT/MRIまで数千円規模)。
ただし、入院下で検査を行う場合や、高額な造影剤・機器を使用する場合は、自己負担限度額制度の適用が考慮されます。
各種料金は診療報酬改定により年度ごとに変動するため、2024年時点の最新情報では上記のようになっています。
各医療機関の公表資料や厚労省の診療報酬点数表を参照すると、詳細を確認することができます。
以上