1型糖尿病(いちがたとうにょうびょう)とは、膵臓(すいぞう)でインスリンという重要なホルモンが十分に作られなくなる病気です。
この疾患は、自己免疫反応により膵臓のβ細胞が破壊されることで発症します。
インスリンは血糖値を調節する役割を担っているため、その不足により血液中のブドウ糖濃度が高くなってしまいます。
1型糖尿病は、主に小児期や青年期に発症することが多いですが、成人になってから発症することもあります。
遺伝的要因や環境要因が複雑に絡み合って発症すると考えられていますが、まだ完全には解明されていません。
病型
1型糖尿病(いちがたとうにょうびょう)は、1A型(自己免疫性)と1B型(特発性)の2つの主要な病型に分類されます
これらの病型は、発症メカニズムや診断基準において異なる特徴を持ち、患者の管理方法に影響を与える可能性があります。
1A型(自己免疫性)1型糖尿病の特徴
1A型は、1型糖尿病の中で最も一般的な病型であり、自己免疫反応により膵臓のβ細胞が破壊されることで発症します。
この型では、体の免疫システムが誤って自身の膵臓のβ細胞を攻撃し、インスリン産生能力を低下させてしまいます。
1A型の診断には、血液検査で膵島関連自己抗体の存在を確認することが重要となります。
以下は、1A型で一般的に検出される主な自己抗体です。
- 膵島細胞抗体(ICA)
- グルタミン酸脱炭酸酵素(GAD)抗体
- インスリン自己抗体(IAA)
- チロシンフォスファターゼ(IA-2)抗体
これらの自己抗体の存在は、1A型の診断をサポートする強力な証拠となります。
| 自己抗体 | 検出率 |
| ICA | 70-80% |
| GAD抗体 | 65-80% |
| IAA | 30-50% |
| IA-2抗体 | 60-70% |
1A型の患者では、複数の自己抗体が同時に検出されることがあり、これは診断の確実性を高める要因となります。
1B型(特発性)1型糖尿病の特徴
1B型は、自己免疫性の証拠がなく、発症の原因が明確でない1型糖尿病の病型です。
この型では、膵臓のβ細胞の破壊が起こっているものの、その機序が不明であるため「特発性」と呼ばれます。
1B型の患者では、1A型で見られるような自己抗体が検出されず、診断はインスリン分泌能の低下と高血糖症状に基づいて行われます。
| 特徴 | 1A型 | 1B型 |
| 自己抗体 | あり | なし |
| 発症原因 | 明確 | 不明 |
1B型は、1型糖尿病全体の中では比較的稀な病型であり、その発症メカニズムの解明は今後の研究課題となっています。
1A型と1B型の発症頻度と地域差
1型糖尿病の病型の分布には、地域や人種による違いが見られます。
例えば、欧米では1A型が1型糖尿病の大多数を占めるのに対し、アジアでは1B型の割合が比較的高いことが報告されています。
日本においても、1型糖尿病患者の中で1B型の割合が他の地域よりも高いことが知られています。
| 地域 | 1A型の割合 | 1B型の割合 |
| 欧米 | 90-95% | 5-10% |
| 日本 | 60-70% | 30-40% |
このような地域差の背景には、遺伝的要因や環境要因が関与していると考えられていますが、その詳細はまだ解明されていません。
1A型と1B型の臨床的意義
1型糖尿病の病型を正確に診断することは、以下の理由から臨床的に大切です。
- 予後予測:1A型と1B型では、膵臓のβ細胞の破壊速度や残存インスリン分泌能の推移が異なる可能性があります。
- 合併症リスク評価:病型によって、長期的な合併症のリスクが異なる可能性があります。
また、1A型と1B型の鑑別は、将来的な治療法の開発や個別化医療の実現に向けて不可欠な情報となります。
現在、1型糖尿病の病型に関する研究は進行中であり、新たな知見が蓄積されつつあります。
これらの研究成果は、患者一人ひとりに最適な管理戦略を立てる上で、ますます重要性を増していくことでしょう。

1型糖尿病の主症状と見逃せない兆候
1型糖尿病(いちがたとうにょうびょう)の主症状は、高血糖に起因する様々な身体の変化と不調として現れ、患者の生活に静かに、しかし確実に影響を及ぼしていきます。
これらの症状は、病気の進行とともに徐々に顕著になり、時に劇的な形で患者の日常を変えてしまう可能性を秘めています。
口渇と多飲:乾いた砂漠を潤す水の誘惑
1型糖尿病患者が最初に気づくことの多い症状は、異常な口渇感と、それに伴う多飲であり、これらは体内で繰り広げられる静かな戦いの最初の兆候となります。
高血糖状態が続くと、体内の細胞が水分を失い、まるで砂漠の中にいるかのような激しい脱水状態に陥りやすくなり、患者は生命維持のために絶え間なく水分を求めるようになります。
この状態を補うため、患者は常に喉の渇きを感じ、水分摂取量が著しく増加することがあり、時には通常の2倍から3倍もの水分を摂取することもあります。
| 症状 | 特徴 |
| 口渇 | 持続的な喉の渇き |
| 多飲 | 通常の2-3倍の水分摂取 |
この症状は、夜間に頻繁にトイレに行く必要がある夜間頻尿にもつながることがあり、患者の睡眠の質を著しく低下させる要因となることがあります。
多尿:止まらない水の流れ
口渇と多飲に密接に関連するのが、多尿症状であり、これは体内の水分バランスが崩れていることを如実に示す兆候です。
高血糖状態では、腎臓の機能が過剰に働き、体内の余分なブドウ糖を尿と一緒に排出しようとするため、結果として尿の量が増加し、患者は頻繁にトイレに行く必要に迫られます。
患者の中には、1日の尿量が通常の2倍以上に達する者もいて、この状況は日常生活に大きな支障をきたす可能性があります。
- 昼間の頻尿
- 夜間頻尿(夜中に何度もトイレに行く)
多尿は体内の水分バランスを更に崩し、悪循環のように更なる脱水状態を引き起こす要因となり、患者の身体に大きな負担をかけることになります。
体重減少:消えゆく身体の秘密
1型糖尿病の進行に伴い、多くの患者が急激な体重減少を経験し、これは周囲の人々にも明らかに気づかれる変化となることがあります。
これは、体がブドウ糖を効率的に利用できないため、代わりに脂肪や筋肉を分解してエネルギー源として使用するという、体内での緊急事態の結果です。
体重減少の程度は個人差がありますが、短期間で5-10%の体重減少が見られることもあり、特に若年者や痩せ型の患者では、この変化が顕著に現れ、周囲の人々の心配や懸念を招くことがあります。
| 期間 | 体重減少率 |
| 1ヶ月 | 2-5% |
| 3ヶ月 | 5-10% |
この急激な体重減少は、単なる外見の変化だけでなく、体力の低下や免疫機能の低下にもつながる可能性があり、患者の健康状態に深刻な影響を及ぼすことがあります。
疲労感と倦怠感:枯れゆく生命力の警鐘
1型糖尿病患者の多くが訴えるのが、持続的な疲労感と倦怠感であり、これらの症状は患者の日常生活の質を著しく低下させる要因となります。
体内でブドウ糖が適切に利用されないため、細胞はエネルギー不足に陥り、日常生活に必要な活力が失われていき、患者は常に疲れを感じ、やる気が出ない状態に陥ることがあります。
この症状は、軽度の倦怠感から極度の疲労まで、幅広い範囲で現れる可能性があり、患者の生活の様々な側面に影響を及ぼします。
- 日中の眠気
- 集中力の低下
- 筋力の低下
疲労感は患者の学業や仕事、社会生活に支障をきたすこともあり、時には深刻な精神的ストレスの原因ともなりかねません。
視力の変化:曇りゆく世界の輪郭
高血糖状態が続くと、目の水晶体に影響を与え、一時的な視力の変化を引き起こすことがあり、これは患者にとって不安や混乱の源となることがあります。
患者は、突然ものがぼやけて見えたり、焦点が合いにくくなったりする経験をすることがあり、この症状は日常生活や仕事に大きな支障をきたす可能性があります。
この症状は、血糖値のコントロールが改善されると通常は回復しますが、重要な早期発見の手がかりとなるため、軽視せずに適切な対応を取ることが大切です。
| 視力の変化 | 特徴 |
| 近視化 | 遠くのものが見えにくくなる |
| 遠視化 | 近くのものが見えにくくなる |
視力の変化は、1型糖尿病の進行を示す静かな警告サインとして認識されており、早期の対応が将来的な合併症のリスクを軽減する可能性があります。
1型糖尿病の主症状は、個々の患者によって現れ方や程度が異なる可能性があり、また、症状が徐々に進行することもあるため、初期段階では気づきにくいこともあります。
しかし、これらの症状を早期に認識し、適切な対応を取ることが、病気の管理において不可欠であり、患者の生活の質を維持する上で重要な役割を果たします。

複雑に絡み合う原因とトリガー
1型糖尿病(いちがたとうにょうびょう)の発症には、遺伝的要因と環境要因が複雑に絡み合っています。
この疾患の原因やきっかけは、1A型(自己免疫性)と1B型(特発性)で異なる特徴を示し、その解明は現在も進行中の重要な研究課題となっています。
遺伝的要因:DNA内に潜む素因
1型糖尿病の発症リスクには、遺伝的要因が大きく関与しています。
特定の遺伝子変異や多型が、この疾患への感受性を高めることが分かっています。
HLA(ヒト白血球抗原)遺伝子群は、1型糖尿病の発症リスクと強い関連があることが知られており、特にHLA-DQ遺伝子とHLA-DR遺伝子の特定の組み合わせが、高リスクとされています。
| HLA遺伝子型 | リスク |
| DQ2/DR3 | 高 |
| DQ8/DR4 | 高 |
| DQ6/DR2 | 低 |
しかし、遺伝的素因があるからといって、必ずしも発症するわけではありません。環境要因との相互作用が、発症の引き金となることが多いのです。
環境要因:外部からの挑戦
1型糖尿病の発症には、様々な環境要因が関与していると考えられています。
これらの要因は、遺伝的素因を持つ個人の免疫系に影響を与え、自己免疫反応を引き起こす可能性があります。
主な環境要因には以下のようなものがあります:
- ウイルス感染(特にエンテロウイルス)
- 食事要因(早期の牛乳タンパク質暴露など)
- 環境化学物質への暴露
- ストレス
例えば、ウイルス感染は膵臓のβ細胞に直接的なダメージを与えたり、免疫系の誤った反応を引き起こしたりする可能性があります。
自己免疫反応:体内での混乱
1A型1型糖尿病の主な原因は、自己免疫反応によるβ細胞の破壊です。この過程では、体の免疫系が誤って膵臓のインスリン産生細胞を攻撃します。
自己抗体の存在は、この自己免疫反応の証拠となります。
| 自己抗体 | 標的 |
| GAD抗体 | グルタミン酸脱炭酸酵素 |
| IA-2抗体 | チロシンフォスファターゼ |
| IAA | インスリン |
これらの自己抗体は、診断の重要なマーカーとなるだけでなく、発症前の段階で検出されることもあります。
β細胞の破壊:静かなる消失
1型糖尿病の発症過程では、膵臓のβ細胞が徐々に破壊されていきます。この破壊は通常、数週間から数年にわたって進行し、インスリン産生能力の低下をもたらします。
β細胞の破壊速度は個人差が大きく、年齢や遺伝的要因、環境要因によって影響を受けます。
| β細胞残存率 | 臨床的特徴 |
| 80-90% | 無症状 |
| 50-80% | 耐糖能異常 |
| <50% | 顕性糖尿病 |
β細胞の破壊が進行し、残存率が50%を下回ると、通常、臨床的な症状が現れ始めます。
1B型(特発性)の謎:未知なる原因を追って
1B型1型糖尿病は、自己免疫性の証拠がないにもかかわらず、β細胞の機能不全や破壊が起こる型です。
この型の原因は未だ明らかになっておらず、遺伝子変異や未知の環境要因が関与している可能性があります。
1B型の特徴:
- 自己抗体陰性
- 急激な発症が多い
- 人種や地域による発症頻度の差が大きい
1B型の研究は、1型糖尿病の新たな発症メカニズムの解明につながる可能性があり、大切な研究分野となっています。
1型糖尿病の原因とトリガーの解明は、予防法や新たな治療法の開発につながる可能性を秘めています。
遺伝的要因と環境要因の複雑な相互作用を理解することは、個別化医療の実現に向けた重要なステップとなるでしょう。
今後の研究の進展により、1型糖尿病の発症メカニズムがさらに明らかになり、患者一人ひとりに最適な予防戦略や治療法が確立されることが期待されています。

1型糖尿病の診察と診断の謎解き
1型糖尿病(いちがたとうにょうびょう)の診察と診断は、医師と患者が協力して行う精密な調査のようなものです。
この過程では、症状の聴取から始まり、血液検査、尿検査、そして時には遺伝子検査まで、様々な手法を駆使して病態を明らかにしていきます。
問診:患者の物語を紐解く
診察の第一歩は、詳細な問診から始まります。
医師は患者の症状、その経過、家族歴、生活習慣などについて丁寧に聞き取りを行い、1型糖尿病の可能性を探ります。
この過程で、医師は探偵のように細かな情報を収集し、疾患の全体像を把握しようと努めます。
問診で聴取される主な項目:
- 症状の種類と発症時期
- 症状の進行速度
- 家族の糖尿病歴
- 最近の体重変化
- 日常的な食事・運動習慣
これらの情報は、1型糖尿病の診断を進める上で重要な手がかりとなります。
身体診察:体の中の変化を探る
問診に続いて、医師は詳細な身体診察を行います。
この段階では、体重、身長、血圧などの基本的な測定に加え、皮膚の状態、呼吸の様子、心音など、全身の状態を注意深く観察します。
| 診察項目 | 確認ポイント |
| 体重 | 急激な減少 |
| 皮膚 | 乾燥、弾力 |
| 呼吸 | 深く速い呼吸 |
| 口腔 | 乾燥、口臭 |
身体診察では、1型糖尿病に特徴的な身体の変化を見逃さないよう、医師は細心の注意を払います。
血液検査:数値で見える体内の変化
1型糖尿病の診断において、血液検査は中心的な役割を果たします。
血糖値の測定はもちろんのこと、HbA1c(ヘモグロビンエーワンシー)の検査、自己抗体の検査など、様々な項目を調べることで、病態を詳細に把握します。
主な血液検査項目:
- 空腹時血糖値
- 随時血糖値
- HbA1c
- GAD抗体
- IA-2抗体
- インスリン自己抗体(IAA)
これらの検査結果は、1型糖尿病の診断を確定する上で不可欠な情報となります。
尿検査:体外に漏れ出す手がかり
尿検査も1型糖尿病の診断において重要な役割を果たします。
尿中のブドウ糖や酵素を調べることで、体内の代謝状態を間接的に知ることができます。
| 尿検査項目 | 異常値 |
| 尿糖 | 陽性 |
| ケトン体 | 陽性 |
尿検査は簡便で非侵襲的な検査方法であり、スクリーニングや経過観察に有用です。
負荷試験:体の反応を見極める
糖負荷試験は、体のインスリン分泌能力と糖代謝能力を評価するための重要な検査です。
経口ブドウ糖負荷試験(OGTT)では、一定量のブドウ糖を摂取した後の血糖値の変化を時間を追って測定します。
| 時間 | 正常値 | 糖尿病型 |
| 0分 | <110 | ≥126 |
| 120分 | <140 | ≥200 |
この検査結果は、1型糖尿病の診断基準の一つとなっています。
遺伝子検査:DNAレベルの探索
一部のケースでは、遺伝子検査が行われることがあります。
特に若年発症の1型糖尿病や、家族歴が濃厚な場合には、遺伝子変異の有無を調べることで、診断の確実性を高めることができます。
遺伝子検査で調べる主な遺伝子:
- HLA-DQ
- HLA-DR
- インスリン遺伝子
これらの遺伝子の特定の変異は、1型糖尿病の発症リスクと関連があることが知られています。

画像所見
1型糖尿病(いちがたとうにょうびょう)の画像所見は、直接的な診断よりも合併症の評価や経過観察において重要な役割を果たします。
1A型(自己免疫性)と1B型(特発性)の両方で、画像診断は患者の健康状態を可視化し、医療チームに貴重な情報を提供します。
膵臓の画像診断
1型糖尿病では、膵臓のβ細胞が破壊されるため、膵臓の画像診断が注目されます。
しかし、初期段階では膵臓の形態的変化が乏しいため、通常のCTやMRIでは顕著な所見が得られないことが多いです。
それでも、長期経過例では膵臓の萎縮が観察されることがあり、これは疾患の進行を示す一つの指標となります。
| 画像モダリティ | 主な所見 |
| CT | 膵臓萎縮 |
| MRI | 膵臓容積減少 |
高度な画像技術の発展により、将来的には膵臓のβ細胞量を非侵襲的に評価できる可能性があります。
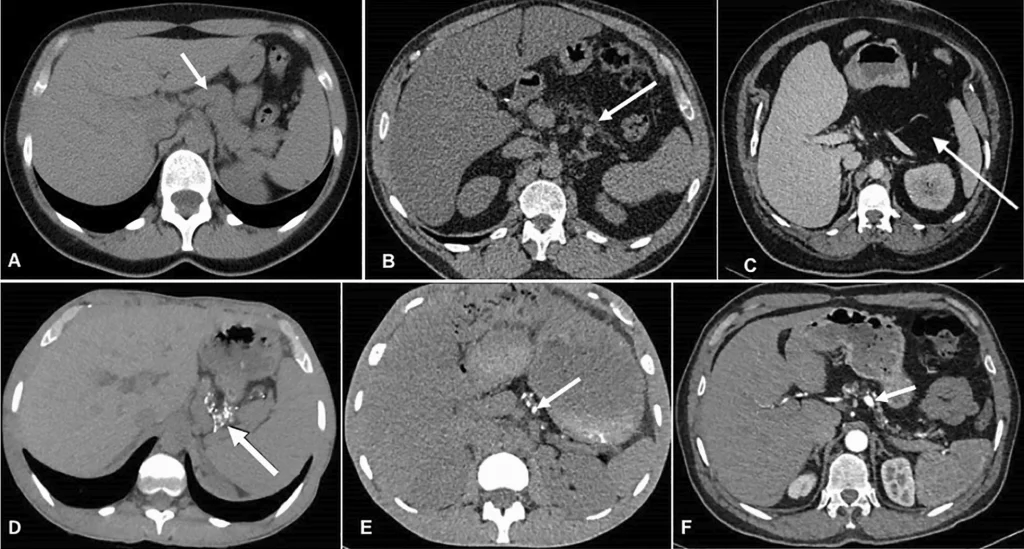
所見:上段:膵脂肪浸潤の異なる程度を示す。(a) 正常な膵臓、(b) 膵部分脂肪浸潤、(c) 膵完全脂肪浸潤(いずれも白矢印)。下段(d–f):膵石灰化の3つの例(矢印)。特筆すべきは、下段のすべての画像が膵部分脂肪浸潤を示している。
網膜の画像診断
糖尿病性網膜症は1型糖尿病の重要な合併症の一つであり、眼底検査や光干渉断層撮影(OCT)などの画像診断が不可欠です。
これらの検査により、網膜の微小血管の変化や浮腫、出血などを詳細に観察することができます。
眼底検査で観察される主な所見:
- 網膜の微小動脈瘤
- 点状出血
- 硬性白斑
- 綿花様白斑
OCTでは、網膜の層構造の変化や黄斑浮腫の程度を定量的に評価することができ、経時的な変化を追跡するのに適しています。
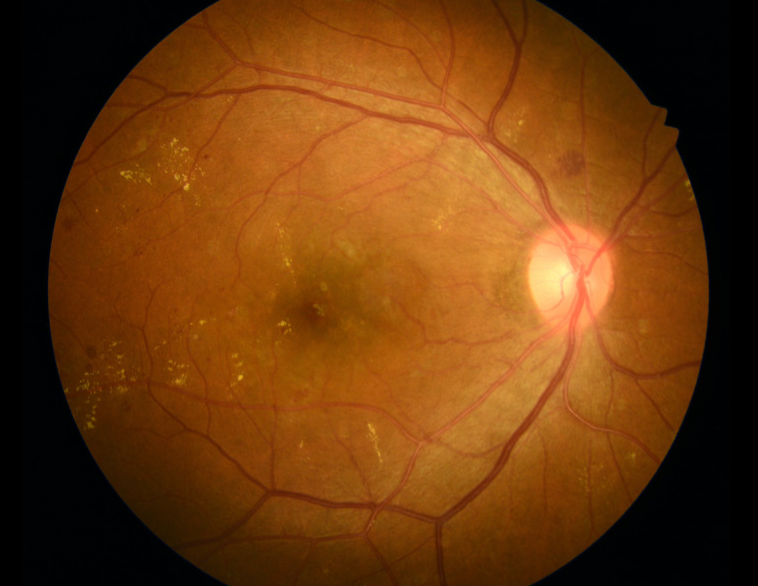
所見:右眼の中等度非増殖糖尿病性網膜症(NPDR)の従来の50°カラー眼底写真(CFP)。網膜内の斑状出血、炎症状出血、および硬性白斑が黄斑部および視神経乳頭周囲に認められる。
腎臓の画像診断:沈黙の臓器の声を聴く
糖尿病性腎症は1型糖尿病の重大な合併症であり、腎臓の画像診断は早期発見と経過観察に役立ちます。
超音波検査やCT、MRIなどが用いられ、腎臓のサイズ、形態、血流などを評価します。
| 病期 | 腎臓サイズ | 腎皮質エコー |
| 早期 | 正常〜腫大 | 正常 |
| 中期 | 腫大 | 軽度上昇 |
| 末期 | 萎縮 | 著明上昇 |
また、腎動脈抵抗指数(RI)の上昇は、腎症の進行を示唆する所見として注目されています。
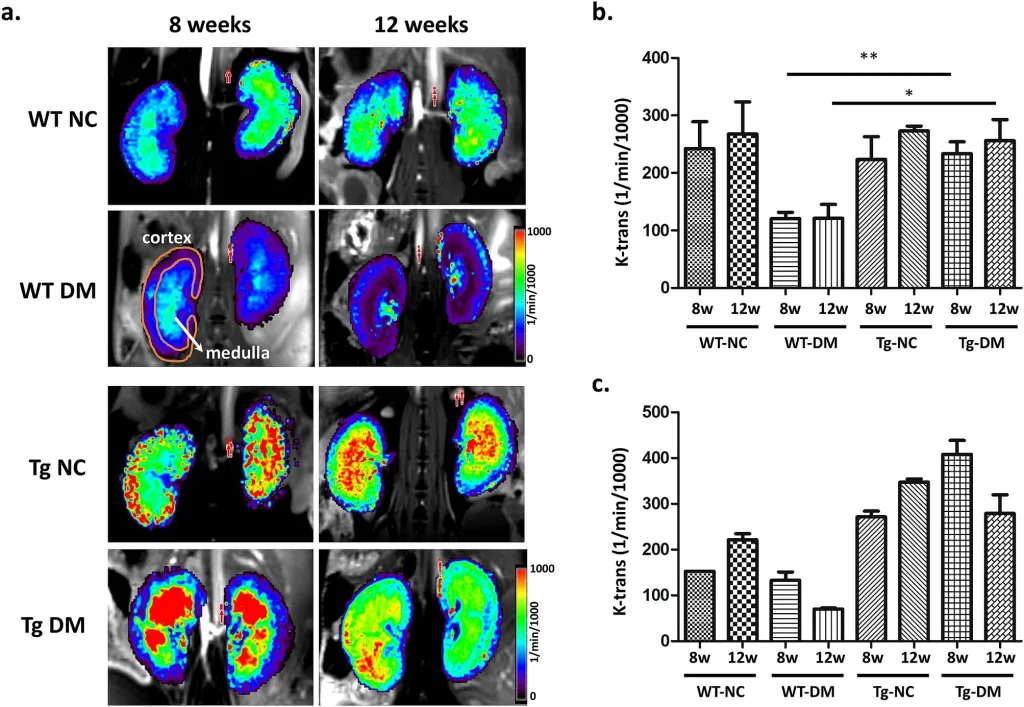
所見:野生型およびmiR29aトランスジェニックマウスを対照およびDM動物として比較したDCE-MRIである。(a) 各実験群の血管相画像から腎臓のKtransマッピングを含むDCE-MR画像。カラーバーの単位はmL/min/1000 mL。 (b) 対照群およびSTZ誘発DM群における腎皮質構造のKtrans値。 (c) 対照群およびSTZ誘発DM群における腎髄質構造のKtrans値。(* < 0.05の一元配置分散分析、各群間の有意差; WT、野生型; Tg、miR29aトランスジェニックマウス; NC、正常対照; DM、糖尿病マウス; n = 5)。このようにDCE-MRIにて腎血流の予測が報告されている。
心臓の画像診断
1型糖尿病患者は心血管疾患のリスクが高いため、心臓の画像診断は予防的観点からも重要です。
心エコー検査、冠動脈CT、心臓MRIなどが用いられ、心機能や冠動脈の状態を評価します。
心エコー検査で評価する主な項目:
- 左室駆出率(LVEF)
- 拡張能
- 壁運動異常
冠動脈CTでは、冠動脈の石灰化や狭窄の有無を非侵襲的に評価することができ、早期の冠動脈疾患の検出に役立ちます。
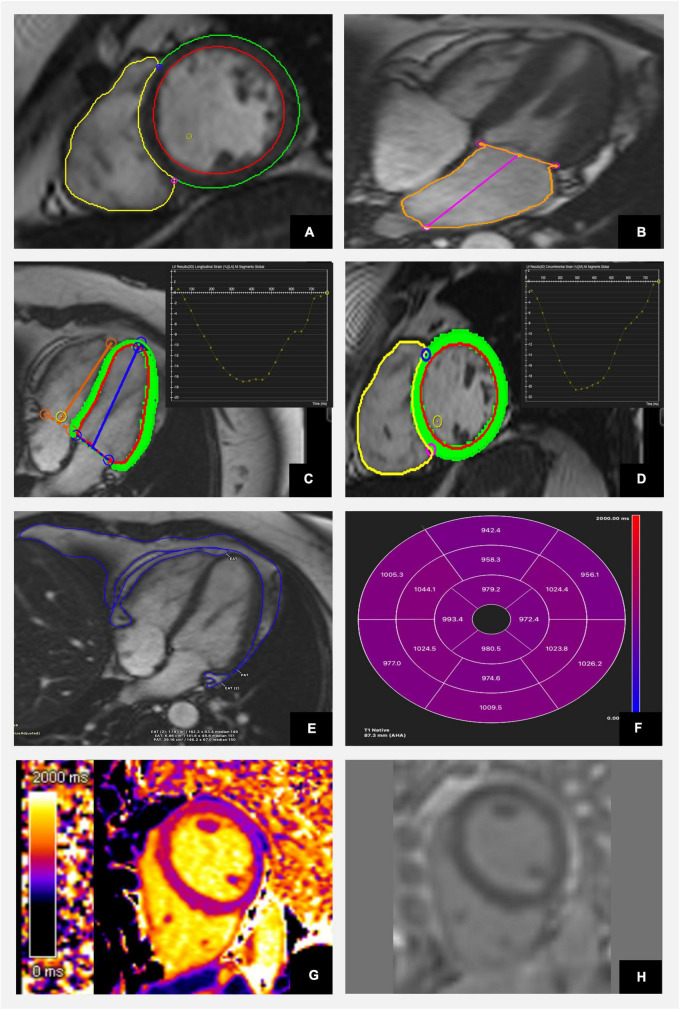
所見:心磁気共鳴画像法(CMR)を用いて糖尿病性心疾患の特徴を評価し、CVI42ソフトウェアを使用して解剖学的および機能的評価ならびに組織特性を解析した結果である。(A) 短軸スタック画像を使用した左心室(LV)および右心室(RV)の容積と機能の評価。(B) 左心房のサイズ評価。(C) 縦方向のストレイン解析。
(D) 周方向のストレイン解析。(E) 心外膜および心膜脂肪組織の推定。(F) 17セグメントAHAモデルを用いた平均セグメントネイティブT1マッピング値の表現。(G) ネイティブT1マッピングのカラーマップ。(H) 遅延ガドリニウム画像には、局所線維化の証拠は認めない。
脳の画像診断
1型糖尿病患者は脳血管障害のリスクも高く、脳のMRIやCT検査が重要となります。
これらの検査では、脳梗塞や微小出血、白質病変などを評価します。
| 画像所見 | 臨床的意義 |
| ラクナ梗塞 | 小血管病変 |
| 微小出血 | 出血リスク |
| 白質病変 | 認知機能低下 |
MRアンギオグラフィーでは、脳血管の狭窄や動脈瘤の有無を評価することができ、脳血管障害の予防に役立ちます。
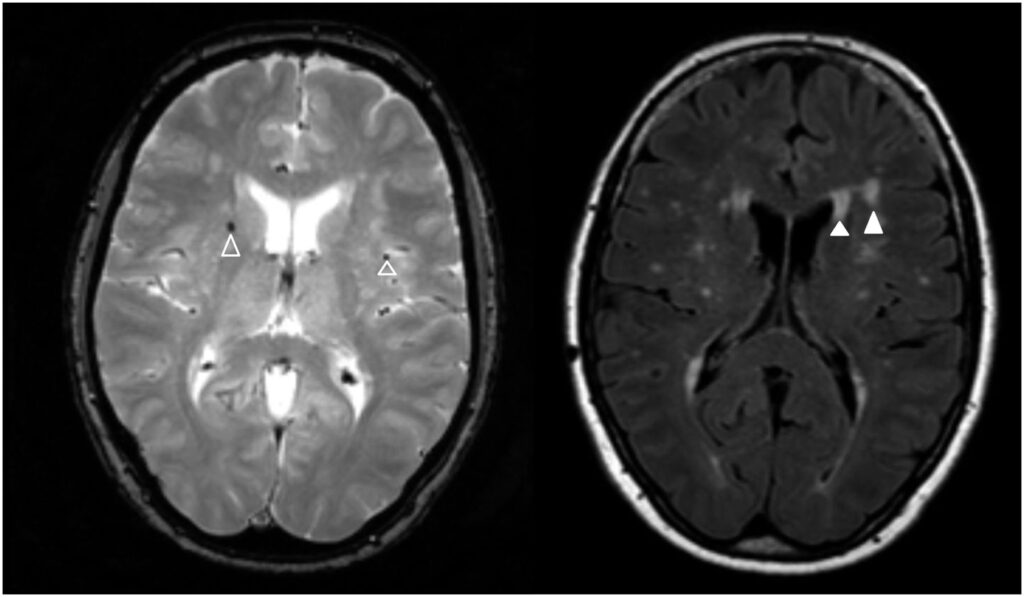
所見:左の画像は、微小出血(大きな開いた△)および微小出血に似た血管(小さな開いた△)を示すT2強調画像である。右の画像は、周囲の脳脊髄液の影響を除去したFLAIR画像で、脳室周囲(小さな閉じた△)および深部(大きな閉じた△)の白質高信号病変(WMH)を示している。

治療方法と薬、治癒までの期間
1型糖尿病(いちがたとうにょうびょう)の治療は、現在のところ完全な治癒を目指すものではなく、長期的な血糖コントロールと合併症予防を主眼としています。
1A型(自己免疫性)と1B型(特発性)の両方において、インスリン補充療法が基本となりますが、近年の医学の進歩により、より効果的で患者の生活の質を向上させる新しい治療法が登場しています。
インスリン補充療法:生命維持の要
1型糖尿病の治療の中核を担うのが、インスリン補充療法です。
患者は、体内で不足しているインスリンを外部から補充することで、血糖値を適切な範囲内に保ちます。
インスリン製剤は、作用時間によって以下のように分類されます。
- 超速効型インスリン
- 速効型インスリン
- 中間型インスリン
- 持効型インスリン
これらを組み合わせて使用することで、食事や活動に合わせた細やかな血糖コントロールが可能となります。
| インスリン種類 | 作用発現 | 作用持続時間 |
| 超速効型 | 10-15分 | 3-5時間 |
| 速効型 | 30分 | 5-8時間 |
| 中間型 | 1-3時間 | 12-18時間 |
| 持効型 | 1-2時間 | 24時間以上 |
インスリン投与方法には、インスリンペン、インスリンポンプ、皮下注射などがあり、患者の生活スタイルや好みに応じて選択されます。
血糖モニタリング
効果的な血糖コントロールのためには、定期的な血糖値の測定が不可欠です。
従来の指先穿刺による血糖自己測定に加え、近年では持続血糖モニタリング(CGM)システムが普及しつつあります。
CGMは皮下に挿入したセンサーを通じて24時間連続的に血糖値を測定し、スマートフォンなどで確認することができます。
| モニタリング方法 | 測定頻度 | 特徴 |
| 指先穿刺 | 随時 | 簡便 |
| CGM | 連続 | 詳細なデータ取得可能 |
これらのデータを基に、医療チームと患者が協力してインスリン投与量や食事・運動計画を調整していきます。
食事療法と運動療法:生活習慣の改善
インスリン療法と並んで重要なのが、食事療法と運動療法です。
これらは血糖コントロールを助けるだけでなく、全身の健康維持にも貢献します。
食事療法のポイント:
- バランスの取れた栄養摂取
- 炭水化物摂取量の管理
- 規則正しい食事時間
運動療法の効果:
- インスリン感受性の改善
- 心血管系の健康維持
- ストレス解消
これらの非薬物療法は、薬物療法と組み合わせることで、より効果的な血糖コントロールを可能にします。
新しい治療法:パンクレアティンα細胞の再プログラミング
最新の研究では、1型糖尿病の新たな治療アプローチとして、パンクレアティンα細胞の再プログラミングが注目されています。
この方法では、膵臓のα細胞をインスリン産生細胞に変換することを目指しています。
| 従来の方法 | 新しいアプローチ |
| β細胞の再生 | α細胞の再プログラミング |
| 幹細胞治療 | 遺伝子編集技術の応用 |
この革新的な治療法が実用化されれば、1型糖尿病の根本的な治療につながる可能性があります。
免疫療法:自己免疫反応を制御する
1A型(自己免疫性)1型糖尿病に対しては、免疫療法の研究も進んでいます。
この治療法は、自己免疫反応を抑制または調整することで、残存するβ細胞を保護し、インスリン分泌能を維持することを目指しています。
主な免疫療法アプローチ:
- T細胞を標的とした治療
- B細胞を標的とした治療
- 制御性T細胞の増強
これらの治療法は、特に発症初期の患者において効果が期待されています。

知っておくべき副作用とリスク
1型糖尿病(いちがたとうにょうびょう)の治療は、患者の生命維持と生活の質向上に不可欠ですが、同時に様々な副作用やリスクを伴う可能性があります。
1A型(自己免疫性)と1B型(特発性)の両方において、主にインスリン療法に関連する副作用や、長期的な合併症のリスクが存在し、これらを理解し適切に対処することが、効果的な疾患管理において重要です。
低血糖
インスリン療法における最も一般的で危険な副作用は、低血糖です。
過剰なインスリン投与や、食事摂取量の減少、予想外の身体活動などにより、血糖値が急激に低下することがあります。
低血糖の症状は個人差がありますが、一般的に以下のようなものが挙げられます。
- 冷や汗
- 動悸
- 手の震え
- 集中力低下
重度の低血糖は意識障害や昏睡を引き起こす可能性があり、生命に関わる緊急事態となります。
| 低血糖の程度 | 血糖値 | 主な症状 |
| 軽度 | 50-70 mg/dL | 空腹感、動悸 |
| 中等度 | 30-50 mg/dL | 冷や汗、手の震え |
| 重度 | 30 mg/dL以下 | 意識障害、昏睡 |
低血糖のリスクは、インスリン療法を受ける全ての患者に存在し、日常生活に大きな影響を与える可能性があります。
インスリン注射部位の問題
長期にわたるインスリン注射は、注射部位に様々な問題を引き起こす可能性があります。
これらの問題は、インスリンの吸収に影響を与え、血糖コントロールを困難にすることがあります。
主な注射部位の問題:
- 皮下脂肪の肥厚(リポハイパートロフィー)
- 皮下脂肪の萎縮(リポアトロフィー)
- 注射部位の感染
これらの問題を予防するためには、注射部位のローテーションが大切ですが、患者によっては習慣化が難しいことがあります。
体重増加:甘美な罠
インスリン療法の開始や強化に伴い、体重が増加することがあります。これは、インスリンが脂肪細胞での脂肪貯蔵を促進する作用を持つためです。
| 体重増加の程度 | インスリン療法開始後の期間 |
| 2-4 kg | 3-6ヶ月 |
| 4-6 kg | 6-12ヶ月 |
体重増加は、心血管疾患のリスク増加や、インスリン抵抗性の悪化につながる可能性があり、長期的な健康管理において注意が必要です。
インスリンアレルギー:稀だが重大な問題
インスリン製剤に対するアレルギー反応は稀ですが、発生した場合は深刻な問題となる可能性があります。
アレルギー反応の種類は以下のように分類されます。
- 即時型反応(注射直後に発生)
- 遅延型反応(数時間後に発生)
アレルギー反応の症状には、注射部位の発赤や腫れ、全身性の蕁麻疹、まれにアナフィラキシーショックなどがあります。
心理的負担:目に見えない重荷
1型糖尿病の管理は、患者に大きな心理的負担を強いることがあります。
日々の血糖測定やインスリン投与、食事管理などの継続的な自己管理は、ストレスや不安、抑うつ症状を引き起こす可能性があります。
| 心理的問題 | 推定有病率 |
| 不安障害 | 20-30% |
| うつ病 | 15-20% |
これらの心理的問題は、血糖コントロールの悪化や生活の質の低下につながる可能性があり、包括的な患者ケアにおいて重要な課題となっています。
長期合併症のリスク:時間との戦い
厳格な血糖コントロールを行っても、長期的な合併症のリスクは完全には排除できません。
主な長期合併症には以下のようなものがあります。
- 糖尿病性網膜症
- 糖尿病性腎症
- 糖尿病性神経障害
- 大血管障害(心筋梗塞、脳卒中など)
これらの合併症は、患者の生活の質を著しく低下させる可能性があり、定期的な検査と早期介入が不可欠です。

再発の可能性と予防の仕方
1型糖尿病(いちがたとうにょうびょう)は、一度発症すると完全な治癒は難しく、生涯にわたる管理が必要となります。
しかし、1A型(自己免疫性)と1B型(特発性)の両方において、厳格な血糖コントロールと生活習慣の改善により、合併症の予防や進行の遅延が可能です。
再発という言葉は厳密には当てはまりませんが、血糖コントロールの悪化や合併症の出現を防ぐことが、1型糖尿病患者の長期的な健康維持において重要です。
血糖コントロールの維持
1型糖尿病患者にとって安定した血糖コントロールの維持は、合併症予防の要となります。
血糖値の変動を最小限に抑えることで、体の様々な組織や臓器へのダメージを軽減することができます。
血糖コントロールの目標値は個人によって異なりますが、一般的な指標は以下の通りです。
| 指標 | 目標値 |
| HbA1c | 7.0%未満 |
| 食前血糖 | 80-130 mg/dL |
| 食後2時間血糖 | 180 mg/dL未満 |
これらの目標値を達成し維持するためには、以下の点に注意を払う必要があります。
- 規則正しいインスリン投与
- バランスの取れた食事
- 適度な運動
- 定期的な血糖モニタリング
継続的な自己管理と医療チームとの連携が、長期的な血糖コントロールの鍵となります。
生活習慣の改善:日々の選択が未来を作る
1型糖尿病の管理において、生活習慣の改善は合併症予防に大きな影響を与えます。
健康的な生活習慣は、血糖コントロールを助けるだけでなく、全身の健康維持にも貢献します。
重要な生活習慣の改善ポイント:
- 禁煙
- 適正体重の維持
- ストレス管理
- 十分な睡眠
これらの習慣を日常生活に組み込むことで、1型糖尿病の長期的な管理がより効果的になります。
定期的な検査:早期発見が鍵を握る
合併症の予防には、定期的な検査による早期発見と早期介入が不可欠です。
1型糖尿病患者は、以下のような検査を定期的に受ける必要があります。
| 検査項目 | 推奨頻度 |
| HbA1c測定 | 3-6ヶ月ごと |
| 眼底検査 | 年1回以上 |
| 尿アルブミン検査 | 年1回以上 |
| 神経学的検査 | 年1回以上 |
これらの検査により、合併症の早期兆候を捉え、適切な対応を取ることが可能となります。
免疫システムの調整:自己免疫反応との共存
1A型(自己免疫性)1型糖尿病では、免疫システムの調整が重要な課題となります。
自己免疫反応を完全に止めることは困難ですが、その進行を遅らせる試みが行われています。
免疫調整のアプローチ:
- 抗炎症食の摂取
- ストレス軽減法の実践
- 適度な運動による免疫機能の強化
これらの方法は、残存するβ細胞の保護や、新たな自己免疫反応の抑制に寄与する可能性があります。
教育と自己管理スキルの向上:知識は力なり
1型糖尿病の長期管理において、患者教育と自己管理スキルの向上は大切な役割を果たします。
正確な知識と適切な自己管理スキルを身につけることで、日々の血糖コントロールが改善し、合併症のリスクを低減することができます。
| 教育内容 | 目的 |
| 栄養教育 | 適切な食事選択 |
| 運動指導 | 安全な運動実践 |
| 低血糖対策 | 緊急時の対応 |
| ストレス管理 | メンタルヘルスケア |
継続的な学習と、新しい情報の取り入れが、1型糖尿病との上手な付き合い方を見つける助けとなります。
1型糖尿病は完治が難しい疾患ですが、適切な管理により、健康的で充実した生活を送ることが可能です。
血糖コントロールの維持、生活習慣の改善、定期的な検査、免疫システムの調整、そして継続的な教育と自己管理スキルの向上が、合併症予防の要となります。

治療費
1型糖尿病の治療費は、長期的な管理が必要なため、患者とその家族に大きな経済的負担をもたらします。初診料は2,910円程度、再診料は750円程度ですが、定期的な検査や処置費用が加わります。
年間の治療費は、インスリン療法や合併症の有無により30万円から100万円以上に及ぶことがあります。
初期診断と定期検査の費用
初期診断時の検査費用数千円円から数万円程度です。定期的なHbA1c検査は1回約490円で、年2~6回程度必要です。
| 検査項目 | 費用 |
| 血液検査 | 5,940円(血液一般+生化学5-7項目+HbA1cの場合) |
| 尿検査 | 260円 |
インスリン療法の費用
インスリン製剤の費用は。例えば1日4回注射する場合、インスリン製剤 300単位×3本 5,197円程度です。その他、注射器やペン型注入器の費用も考慮する必要があります。
合併症管理の追加費用
合併症の検査や治療が必要になると、さらに費用が増加します。網膜症の検査は1回560円(精密眼底検査)程度、腎症の検査は3,000円程度です。
なお、上記の価格は2024年9月時点のものであり、最新の価格については随時ご確認ください。
以上