代謝疾患の一種である糖原病(GSD)とは、体内でグリコーゲンを適切に処理できない遺伝性の病気です。
グリコーゲンは、私たちの体のエネルギー源として重要な役割を果たす糖質の一種で、通常、体はグリコーゲンを必要に応じて分解しエネルギーとして利用します。
しかし、糖原病の患者さんの体ではこの過程に問題が生じ、グリコーゲンが過剰に蓄積され、肝臓や筋肉など様々な臓器に影響が及ぶことがあります。
糖原病(GSD)の多様な病型
糖原病(GSD)は複数の病型に分類され、それぞれが異なる酵素欠損や遺伝子変異に関連しています。
これらの病型は、Roman数字を用いてGSD I型からGSD XV型まで分類されており、各病型の特徴や影響を受ける臓器が異なります。
各病型はさらにサブタイプに分けられることがあり、例えばGSD I型はIa型とIb型に細分化され、より詳細な分類が行われています。
病型によって影響を受ける臓器や症状の程度が異なるため、正確な診断が患者さんの生活の質を向上させる上で重要な役割を果たし、適切な管理方針の決定につながります。
主要な糖原病病型とその特徴
GSD I型(フォン・ギールケ病)は最もよく知られた病型の一つで、肝臓と腎臓が主に影響を受け、グルコース-6-フォスファターゼ酵素の欠損が特徴的です。
GSD II型(ポンペ病)は、心臓や骨格筋に影響を与える可能性があり、乳児期から成人期まで幅広い年齢で発症することがあり、酸性α-グルコシダーゼの欠損が原因とされています。
GSD III型(コリ病またはフォーブス病)は主に肝臓と筋肉に影響を及ぼし、グリコーゲン脱分枝酵素の欠損により、異常構造のグリコーゲンが蓄積します。
| 病型 | 主な影響を受ける臓器 | 欠損酵素 |
| I型 | 肝臓、腎臓 | グルコース-6-フォスファターゼ |
| II型 | 心臓、骨格筋 | 酸性α-グルコシダーゼ |
| III型 | 肝臓、筋肉 | グリコーゲン脱分枝酵素 |
稀少な糖原病病型
一部の糖原病病型は非常に稀少であり、診断が困難な場合があります。これらの稀少な病型の理解を深めることは、適切な診断と管理につながる不可欠な要素となります。
GSD VI型(ヘルス病)やGSD IX型は肝臓に影響を与えますが、I型ほど重度ではないことが多く、肝グリコーゲンホスホリラーゼやホスホリラーゼキナーゼの欠損が原因です。
GSD VII型(タルイ病)は赤血球や筋肉に影響を与え、運動不耐性や溶血性貧血を引き起こす可能性があり、ホスホフルクトキナーゼの欠損が特徴的です。
| 病型 | 特徴 | 欠損酵素 |
| VI型 | 肝臓に影響、比較的軽度 | 肝グリコーゲンホスホリラーゼ |
| IX型 | 肝臓に影響、比較的軽度 | ホスホリラーゼキナーゼ |
| VII型 | 赤血球・筋肉に影響、貧血の可能性 | ホスホフルクトキナーゼ |
糖原病の遺伝形式
糖原病の多くは常染色体劣性遺伝形式をとりますが、一部の病型では異なる遺伝形式を示すことがあり、遺伝形式の理解は家族計画や遺伝カウンセリングにおいて大切な情報となります。
X連鎖性劣性遺伝を示すGSD VIII型や、常染色体優性遺伝を示すGSD 0型などがその例で、これらの特殊な遺伝形式は発症パターンや家族歴の解釈に影響を与えます。
以下に主な遺伝形式をまとめます:
- 常染色体劣性遺伝:多くの糖原病病型で見られる
- X連鎖性劣性遺伝:GSD VIII型など
- 常染色体優性遺伝:GSD 0型など
| 遺伝形式 | 特徴 | 例 |
| 常染色体劣性 | 両親からそれぞれ変異遺伝子を受け継ぐ | 多くの病型 |
| X連鎖性劣性 | 母親が保因者、息子が発症しやすい | GSD VIII型 |
| 常染色体優性 | 片親から変異遺伝子を受け継ぐだけで発症 | GSD 0型 |

GSDの主症状と臨床像
糖原病(とうげんびょう)は、グリコーゲン代謝に関わる酵素の欠損や機能異常により引き起こされる遺伝性疾患群で、様々な臓器に影響を及ぼす可能性があります。
患者さんの多くは、低血糖や筋力低下といった共通の症状を呈しますが、その程度や発症時期は病型によって大きく異なり、個々の患者さんで症状の現れ方が異なることがあります。
低血糖は特に小児期の患者さんにおいて顕著で、空腹時や運動後に発生しやすく、意識障害や痙攣を引き起こす危険性があり、適切な血糖管理が重要となります。
筋力低下は主に骨格筋に影響を及ぼす病型で見られ、日常生活動作の制限や運動能力の低下につながることがあり、患者さんのQOLに大きな影響を与える可能性があります。
| 共通症状 | 特徴 | 影響 |
| 低血糖 | 空腹時や運動後に発生しやすい | 意識障害、痙攣のリスク |
| 筋力低下 | 日常生活動作に影響を及ぼす可能性あり | QOLの低下、運動能力の制限 |
肝臓に関連する症状
肝臓が主に影響を受ける糖原病の病型では、肝腫大が顕著な症状として現れることがあり、腹部膨満感や不快感を引き起こし、時には呼吸困難にまで発展する可能性があります。
また、肝機能障害により、血液凝固因子の産生が低下し、出血傾向が現れることもあり、患者さんの日常生活に注意が必要となる場合があります。
さらに、一部の患者さんでは、成長遅延や思春期遅発といった発達に関する問題が生じることがあり、身体的・心理的な影響を考慮した包括的なケアが重要となります。
| 肝臓関連症状 | 影響 | 二次的な問題 |
| 肝腫大 | 腹部膨満感、呼吸困難の可能性 | 日常生活の制限、不快感 |
| 肝機能障害 | 出血傾向、成長遅延の可能性 | 活動制限、心理的ストレス |
筋肉に関連する症状
筋肉が主に影響を受ける糖原病の病型では、進行性の筋力低下や筋萎縮が主要な症状となり、これらの症状は幼少期から現れる場合もあれば、成人になってから徐々に進行する場合もあります。
運動不耐性は多くの患者さんに見られ、短時間の激しい運動後に筋痛や筋硬直が生じやすくなり、日常生活や社会活動に支障をきたすことがあります。
また、一部の病型では、心筋にもグリコーゲンが蓄積し、心肥大や心不全のリスクが高まることがあり、定期的な心機能評価が必要となる場合があります。
| 筋肉関連症状 | 特徴 | 影響 |
| 筋力低下 | 進行性、年齢によって発症時期が異なる | 日常生活動作の制限 |
| 運動不耐性 | 短時間の運動後に症状が出現 | 社会活動の制限、QOLの低下 |
| 心筋障害 | グリコーゲン蓄積による心肥大 | 心不全リスクの上昇 |
代謝異常に関連する症状
糖原病患者さんの多くは、代謝異常に起因する様々な症状を経験し、これらの症状は長期的な健康管理において重要な課題となります。
高尿酸血症は頻繁に見られる症状の一つで、痛風発作のリスクを高める可能性があり、食事制限や適切な水分摂取などの生活習慣の管理が重要となります。
また、高脂血症も多くの患者さんで認められ、動脈硬化や心血管疾患のリスク因子となりうるため、定期的な血液検査と必要に応じた治療介入が重要となります。
一部の病型では、腎機能障害が進行し、尿タンパクや腎石灰化といった症状が現れることがあり、腎臓の定期的なモニタリングと適切な管理が必要となります。
| 代謝異常関連症状 | リスク | 管理のポイント |
| 高尿酸血症 | 痛風発作 | 食事制限、水分摂取 |
| 高脂血症 | 動脈硬化、心血管疾患 | 定期的な血液検査、生活習慣改善 |
| 腎機能障害 | 尿タンパク、腎石灰化 | 腎機能モニタリング、適切な治療 |
年齢による症状の変化
糖原病の症状は、患者さんの年齢によって変化することがあり、各ライフステージに応じた適切な管理と支援が重要となります。
- 新生児期・乳児期
- 重度の低血糖
- 哺乳困難
- 筋緊張低下
- 小児期
- 成長遅延
- 運動発達遅滞
- 反復性の低血糖発作
糖原病の症状は、成人期に至っても持続または進行する可能性があり、長期的な管理が重要となるため、患者さんの生涯にわたる包括的なケアが必要です。
例えば、成人期には以下のような症状が現れることがあり、これらの症状に対する適切な対応と支援が求められます。
- 慢性的な疲労感
- 筋力低下の進行
- 心血管系の合併症
これらの症状は患者さんの生活の質に大きな影響を与える可能性があるため、適切な管理と定期的な評価が不可欠であり、医療チームと患者さん、そしてご家族との密接な連携が重要となります。

原因
原因糖原病(とうげんびょう)は遺伝子の変異に起因する代謝疾患であり、その原因は主にグリコーゲン代謝に関与する酵素をコードする遺伝子の異常にあり、これらの遺伝子異常により体内でのグリコーゲンの合成、分解、または輸送に支障をきたします。
この結果、グリコーゲンが過剰に蓄積されたり、適切に利用されなくなったりし、様々な代謝異常や臨床症状が引き起こされることになります。
糖原病の多くは常染色体劣性遺伝形式をとりますが、一部の病型ではX連鎖性劣性遺伝や常染色体優性遺伝を示すこともあり、これらの遺伝形式の違いは、疾患の発症パターンや家族内での遺伝に影響を与える重要な要因となります。
| 遺伝形式 | 特徴 | 遺伝パターン | 家族内での影響 |
| 常染色体劣性 | 両親から変異遺伝子を受け継ぐ必要がある | 25%の確率で発症 | 同胞間でのリスク評価が重要 |
| X連鎖性劣性 | 主に男性が発症、女性は保因者になりやすい | 男児の50%が発症 | 母系遺伝の傾向が強い |
| 常染色体優性 | 片親から変異遺伝子を受け継ぐと発症 | 50%の確率で発症 | 世代を超えて発症する可能性が高い |
糖原病の分子生物学的メカニズム
糖原病の各病型は、それぞれ特定の酵素の欠損または機能不全に関連しており、これらの酵素はグリコーゲン代謝経路の様々な段階で働き、その機能障害によって特定の代謝過程に問題が生じることになります。
例えば、グリコーゲンホスホリラーゼの欠損はGSD VI型(ヘルス病)を引き起こし、グルコース-6-ホスファターゼの欠損はGSD I型(フォン・ギールケ病)の原因となり、このように各病型の特徴的な代謝異常は、それぞれの酵素欠損に直接関連しています。
これらの酵素欠損により、グリコーゲンの合成・分解バランスが崩れ、エネルギー代謝や糖恒常性に影響を及ぼすことになります。
| 病型 | 欠損酵素 | 主な影響 | 代謝経路への影響 |
| GSD I型 | グルコース-6-ホスファターゼ | 肝臓でのグルコース放出障害 | 糖新生の阻害 |
| GSD II型 | α-グルコシダーゼ | リソソームでのグリコーゲン分解障害 | 細胞内グリコーゲン蓄積 |
| GSD III型 | 脱分枝酵素 | グリコーゲン構造の異常 | 不完全なグリコーゲン分解 |
| GSD V型 | 筋ホスホリラーゼ | 筋肉でのグリコーゲン分解障害 | 運動時のエネルギー不足 |
環境因子と遺伝子発現
糖原病の発症や重症度に影響を与える要因として、遺伝子変異だけでなく環境因子も考慮する必要があり、以下のような環境要因が、遺伝子発現や疾患の進行に影響を与える可能性があります。
- 食事内容と摂取パターン
- 炭水化物の質と量
- 食事のタイミング
- 運動習慣
- 運動の種類と強度
- 運動頻度
- ストレスレベル
- 心理的ストレス
- 身体的ストレス
- 感染症や他の疾患の併発
- 急性疾患の影響
- 慢性疾患との相互作用
これらの環境因子は、エピジェネティックな変化を通じて遺伝子の発現を調節し、結果として疾患の表現型に影響を与えることがあり、したがって遺伝的素因と環境要因の相互作用を理解することが、糖原病の包括的な管理において不可欠です。
遺伝子変異の種類と影響
糖原病を引き起こす遺伝子変異には様々な種類があり、それぞれが酵素機能に異なる影響を与え、これらの変異の種類や位置によって、酵素の機能喪失の程度が異なり、結果として疾患の重症度や臨床像に違いが生じることになります。
主な遺伝子変異のタイプには以下のようなものがあります。
- 点変異(ミスセンス変異、ナンセンス変異)
- 欠失または挿入
- スプライシング変異
- 大規模な遺伝子再構成
| 変異タイプ | 特徴 | 影響 | 酵素機能への影響 |
| 点変異 | 単一塩基の変化 | アミノ酸置換または早期終止 | 部分的または完全な機能喪失 |
| 欠失/挿入 | 塩基配列の欠損または追加 | フレームシフトや機能変化 | タンパク質構造の大幅な変化 |
| スプライシング変異 | mRNAの処理異常 | 異常タンパク質の産生 | 機能的ドメインの欠損や変化 |
| 大規模再構成 | 遺伝子の大きな構造変化 | 遺伝子全体の機能喪失 | 完全な酵素欠損 |
遺伝子診断と家族歴の重要性
糖原病の正確な診断において、遺伝子検査は中心的な役割を果たし、遺伝子診断により特定の変異を同定し、病型を確定することができ、これは適切な管理戦略の立案に不可欠です。
さらに、家族歴の詳細な調査は、以下の点で重要な情報を提供します。
- 遺伝形式の推定
- 家系図の作成と分析
- 発症パターンの確認
- 保因者の同定
- 遺伝カウンセリングの必要性評価
- 将来的な家族計画への影響
- 家族内の他の成員のリスク評価
- 早期スクリーニングの必要性
- 予防的介入の可能性
家族歴と遺伝子診断を組み合わせることで、糖原病の早期発見や予防的介入の機会が増え、患者さんとその家族のQOL向上につながる可能性があり、これは長期的な疾患管理において大切な要素となります。

診察と診断糖原病(GSD)の診察と診断プロセス 包括的アプローチ
糖原病(とうげんびょう)の診断プロセスは、詳細な問診から始まり、医師は患者さんの現在の状態、発達歴、家族歴などについて綿密な聞き取りを行い、糖原病を示唆する兆候がないか慎重に評価します。
特に、成長曲線の変化、運動能力の発達、食事パターンなどに注目し、これらの情報は糖原病の早期発見につながる可能性があります。
家族歴の聴取は、遺伝性疾患である糖原病の診断において不可欠な要素であり、類似症状や代謝疾患の家族内発症の有無を確認することで、遺伝的リスクの評価に役立ちます。
| 問診項目 | 着目点 | 診断的意義 |
| 成長曲線 | 成長の停滞や遅延 | 代謝異常の影響を示唆 |
| 運動発達 | 筋力低下や運動不耐性 | 筋型GSDの可能性を示唆 |
| 食事パターン | 頻回の食事摂取や特定食品への嗜好 | 血糖維持の代償機能を示唆 |
| 家族歴 | 類似症状や代謝疾患の既往 | 遺伝的要因の存在を示唆 |
身体診察と臨床所見
問診に続いて、詳細な身体診察が行われ、医師は以下のような点に注目して診察を進め、これらの臨床所見は、糖原病の病型や重症度を推測する上で重要な手がかりとなります。
- 肝臓の大きさと硬さ:触診や打診による評価
- 筋力と筋緊張:徒手筋力テストや筋緊張度の評価
- 心臓の大きさと機能:聴診や触診による評価
- 顔貌や体型の特徴:特徴的な外見の有無
身体診察の結果は、後続の検査計画の立案にも大きく影響し、特定の所見が認められた場合には、より詳細な検査が必要となることがあります。
血液検査と生化学的評価
糖原病の診断において、血液検査は欠かせない検査の一つであり、一般的な血液検査に加え、以下のような特殊な生化学的検査が実施されることがあります。
- 血糖値の日内変動:低血糖の有無や頻度を評価
- 乳酸値とピルビン酸値:代謝異常の指標
- 肝機能検査(AST、ALTなど):肝臓への影響を評価
- CK(クレアチンキナーゼ)値:筋肉への影響を評価
これらの検査結果は、糖原病の疑いを強める重要な指標となり、病型の推定や重症度の評価に役立ちます。
| 検査項目 | 異常所見 | 診断的意義 |
| 血糖値 | 低血糖傾向 | グルコース放出障害を示唆 |
| 乳酸値 | 上昇 | 代謝経路の異常を示唆 |
| 肝機能 | AST、ALTの上昇 | 肝細胞障害の存在を示唆 |
| CK値 | 筋型で上昇 | 筋細胞障害の存在を示唆 |
画像診断の役割
画像診断は、糖原病による臓器の変化を視覚化するのに有用であり、主に用いられる画像検査には以下のようなものがあり、これらの検査により、肝臓の腫大や脂肪化、心臓の肥大などを評価することができます。
- 腹部超音波検査:非侵襲的で繰り返し実施可能
- CT(コンピュータ断層撮影):詳細な臓器構造を評価
- MRI(磁気共鳴画像):軟部組織の変化を高精度で評価
画像所見は、糖原病の病型や進行度の判断に重要な情報をもたらし、経時的な変化の観察にも役立ちます。
| 画像検査 | 主な評価対象 | 特徴 |
| 腹部超音波 | 肝臓の大きさと構造 | 簡便で繰り返し実施可能 |
| CT | 臓器の詳細な形態 | 高解像度の断層画像が得られる |
| MRI | 軟部組織の変化 | 放射線被曝なしで詳細な評価が可能 |
遺伝子検査と酵素活性測定
糖原病の確定診断には、遺伝子検査や酵素活性の測定が重要であり、遺伝子検査では、糖原病に関連する特定の遺伝子変異を同定し、一方、酵素活性の測定は、生検組織や血液サンプルを用いて行われ、特定の酵素の機能を直接評価します。
これらの検査結果により糖原病の病型を確定し、適切な管理方針を決定することが可能となり、遺伝カウンセリングや家族スクリーニングの必要性の判断にも役立ちます。
| 検査 | 目的 | 方法 | 診断的意義 |
| 遺伝子検査 | 特定の遺伝子変異の同定 | 血液または組織サンプルのDNA解析 | 病型の確定、遺伝カウンセリングに有用 |
| 酵素活性測定 | 特定酵素の機能評価 | 生検組織や血液サンプルの生化学的分析 | 酵素機能の直接的評価、病型の確定に不可欠 |
鑑別診断の必要性
糖原病の診断において他の代謝疾患との鑑別は大切であり、類似した症状を呈する疾患には以下のようなものがあります。
- ミトコンドリア病:エネルギー産生障害による多様な症状
- 脂肪酸代謝異常症:脂肪酸の利用障害による低血糖や筋症状
- 先天性筋ジストロフィー:進行性の筋力低下と筋萎縮
これらの疾患との慎重な鑑別により、正確な診断が可能となり、鑑別診断の過程では、前述の各種検査に加え、必要に応じて追加の専門的検査が実施されることがあります。

GSDの画像所見
糖原病(とうげんびょう)において、肝臓は最も顕著な変化を示す臓器の一つであり、様々な画像検査で特徴的な所見が観察されます。
超音波検査では、肝臓の腫大と輝度の増加が特徴的に観察され、正常肝と比較してより明るく描出されることがあります。
CT検査では肝臓の密度が低下し、正常肝と比較してより暗く描出されることがあり、これはグリコーゲンの蓄積による組織密度の変化を反映しています。
MRI検査では、T1強調画像で肝実質の信号強度が上昇し、T2強調画像でも軽度の高信号を呈することがあり、これらの所見はグリコーゲンや脂肪の蓄積によるものと考えられています。
| 検査方法 | 主な所見 | 特徴 | 臨床的意義 |
| 超音波 | 腫大、輝度上昇 | 非侵襲的、繰り返し評価可能 | 経過観察に適している |
| CT | 密度低下 | 全体像の把握に有用 | 肝サイズや密度変化の定量的評価可能 |
| MRI | T1/T2高信号 | 組織性状の詳細な評価可能 | グリコーゲン/脂肪蓄積の鑑別に有用 |
心臓の画像所見
一部の糖原病では、心臓にもグリコーゲンが蓄積し、特徴的な画像所見を呈することがあり、これらの所見は心機能評価や治療方針の決定に重要な情報をもたらします。
心エコー検査では、心筋の肥厚や心室壁の輝度上昇が観察されることがあり、これらの所見は心筋内のグリコーゲン蓄積を反映していると考えられています。
心臓MRIでは、左室壁の肥厚やT1強調画像での信号強度上昇が認められる場合があり、さらに遅延造影像で特徴的な造影パターンを示すことがあります。
核医学検査では、糖代謝異常を反映した特異的な集積パターンが観察されることもあり、これは心筋のエネルギー代謝異常を評価する上で有用な情報となります。
| 検査方法 | 主な所見 | 臨床的意義 | 追加情報 |
| 心エコー | 心筋肥厚、輝度上昇 | 心機能評価に有用 | 非侵襲的で繰り返し評価可能 |
| 心臓MRI | 壁肥厚、T1高信号 | 組織性状評価に優れる | 遅延造影像で線維化評価も可能 |
| 核医学 | 特異的集積パターン | 代謝異常の評価に役立つ | 治療効果判定にも使用可能 |
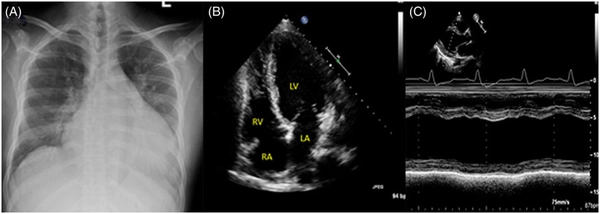
所見;GSD IV の症例。前後(AP)胸部X線写真では、心影の拡大が示されている(A)。心エコーの四腔ビュー(B)では、左心室の重度の拡張が明らかである。Mモードによる左心室中部径では、最小の短縮率が示されている(C)。LA、左心房;LV、左心室;RA、右心房;RV、右心室。
筋肉の画像所見
筋型糖原病では、骨格筋に特徴的な変化が現れることがあり、これらの画像所見は病型の診断や進行度の評価に重要な役割を果たします。
MRI検査では、T1強調画像で筋肉の信号強度が低下し、T2強調画像で高信号を呈することがあり、これらの変化は筋線維の変性や浮腫を反映していると考えられています。
筋CTでは、筋肉の密度低下や脂肪置換が観察されることがあり、これらの所見は筋力低下や萎縮の程度と相関することがあります。
超音波検査では、筋エコー輝度の上昇や筋線維の不均一性が認められることがあり、これらの所見は非侵襲的に筋肉の状態を評価する上で有用です。
これらの画像所見は、病型や進行度によって異なる特徴を示すことがあり、経時的な変化を追跡することで疾患の進行や治療効果を評価することができます。
| 検査方法 | 主な所見 | 臨床的意義 | 特徴 |
| MRI | T1低信号、T2高信号 | 筋線維変性や浮腫の評価 | 高い組織コントラスト |
| 筋CT | 密度低下、脂肪置換 | 筋萎縮の定量的評価 | 骨との関係も評価可能 |
| 超音波 | エコー輝度上昇、不均一性 | 非侵襲的な筋評価 | リアルタイム観察可能 |
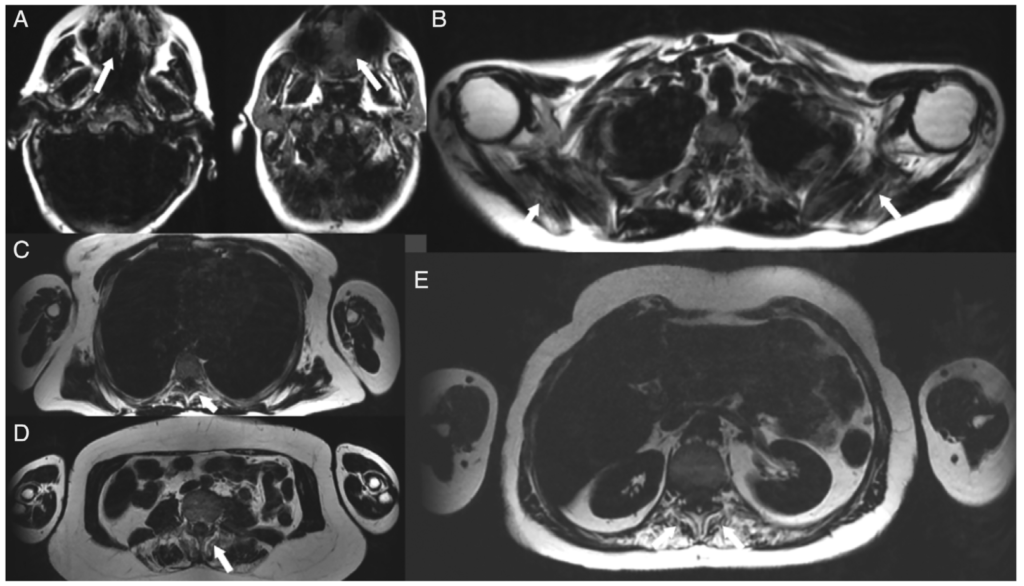
所見:糖原病III型(GSDIII)患者の上体の断面。A. 舌を含む大部分の顔面筋は保持されていた。B. 回旋筋腱板の筋肉は、病気の進行が遅い段階の患者にのみ影響を受けていた。C–E. 胸部伸筋群の関与は、腸肋筋、最長筋、および棘筋の均等な脂肪浸潤を伴う非特異的なパターンを示していた。
中枢神経系の画像所見
一部の糖原病では、中枢神経系にも影響が及ぶことがあり、特徴的な画像所見を呈することがあります。これらの所見は神経学的症状との関連性を評価する上で重要な情報となります。
頭部MRIでは、以下のような所見が観察されることがあります:
- 大脳白質の信号異常:T2強調画像やFLAIR画像での高信号域
- 小脳萎縮:小脳皮質の菲薄化や溝の開大
- 基底核の信号変化:T2強調画像での高信号や萎縮
これらの所見は、病型や進行度によって異なる特徴を示すことがあり、神経学的評価と併せて解釈することが重要です。また、経時的な変化を追跡することで、疾患の進行や治療効果を評価することができます。
| 部位 | MRI所見 | 臨床的意義 | 関連する症状 |
| 大脳白質 | T2/FLAIR高信号 | 髄鞘障害の可能性 | 認知機能障害 |
| 小脳 | 萎縮 | 運動協調障害との関連 | 歩行障害、失調 |
| 基底核 | 信号変化 | 運動障害との関連 | 不随意運動 |
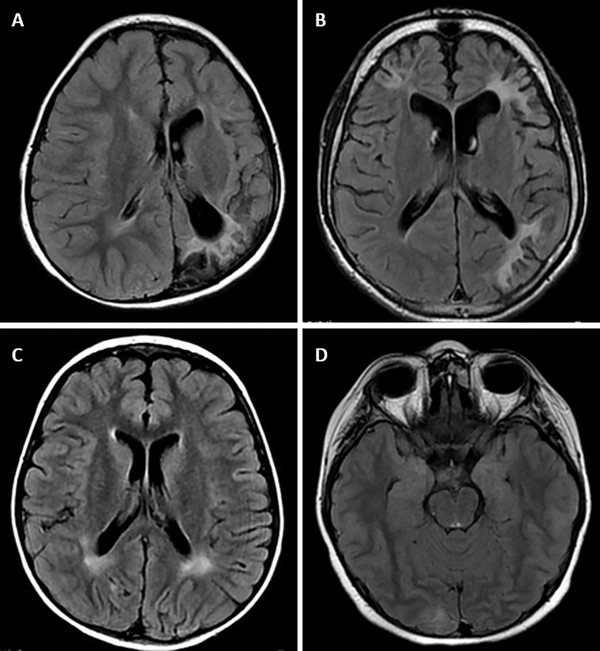
所見:GSD Ia患者における磁気共鳴画像の変化。
(A)(患者1) 左後頭葉および頭頂葉の皮質および皮質下領域、ならびに前頭頭頂移行部に沿って広範なグリオーシスおよび脳軟化の領域が観察され、これらは高い凸部を伴い、対応する部分の同側側脳室の代償的拡張を伴っている。さらに、対応する皮質脊髄路の慢性ワーラー変性の兆候を伴う核被殻後部にまで拡がる、恐らくヘモジデリン沈着に関連する病変の病巣が認められる。左半球の脳萎縮が顕著である。
(B)(患者12) 両側前頭領域および左頭頂側頭移行部の皮質および皮質下白質に影響を与える収縮した病変が明らかである。これらの変化は脳軟化症および血管後遺症を示唆している。
(C)(患者9) 中央白質および周角領域近くに投影される楕円形の高信号病巣がT2強調シーケンスで示されている。これらの非特異的変化は、脈管周囲スペース(末端髄鞘形成領域)周囲のグリオーシスを表している可能性がある。
(D)(患者10) 特に右側の体積喪失を伴う後頭極の小さな収縮した病変が、低血糖に続発する病変を示唆している。
腎臓の画像所見
一部の糖原病では、腎臓にも影響が及ぶことがあり、画像検査で特徴的な所見が認められることがあります。これらの所見は腎機能障害の早期発見や進行評価に役立ちます。
超音波検査では、以下のような所見が観察されることがあります:
- 腎臓の腫大:正常サイズを超える腎臓の増大
- 皮髄境界の不明瞭化:皮質と髄質の境界が不鮮明になる
- エコー輝度の上昇:腎実質のエコー輝度が全体的に増加する
CT検査やMRI検査でも、腎臓の形態異常や信号変化が認められることがあり、これらの所見は腎実質の構造変化や機能異常を反映している可能性があります。
これらの所見は、腎機能評価と併せて解釈することが大切であり、経時的な変化を追跡することで、腎障害の進行や治療効果を評価することができます。
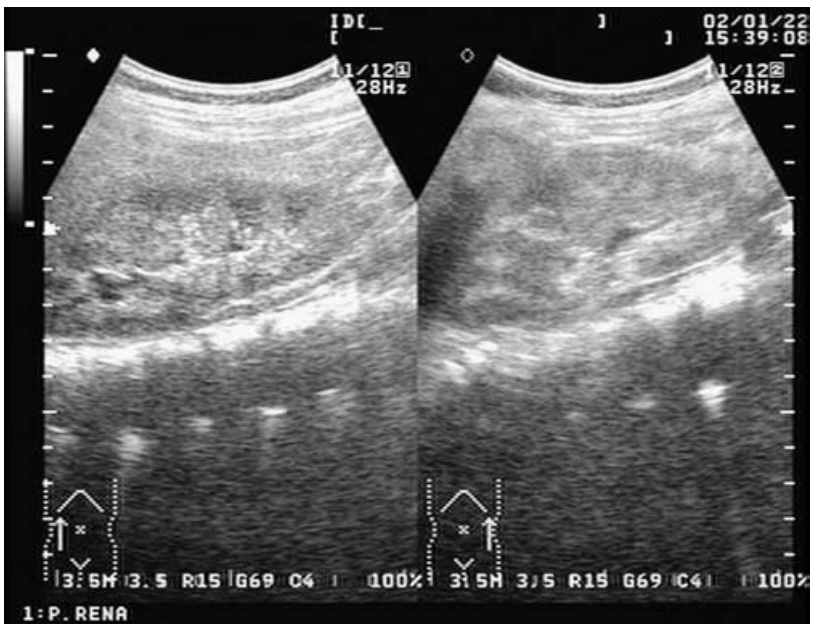
所見:GCD患者の腎臓超音波検査では、両側腎腫大とエコー輝度の増加が示されている。異常なエコー輝度は皮質と髄質の両方に影響を及ぼし、周辺部よりも中央部で顕著である。皮質と髄質の区別が失われている。
画像所見の経時的変化
糖原病の画像所見は、時間経過とともに変化することがあり、定期的な画像評価により、疾患の進行や治療効果を適切に評価することができます。
定期的な画像評価により、以下のような変化を追跡することができます:
- 臓器サイズの変化:肝臓や心臓の大きさの増減
- 組織性状の変化:信号強度や密度の変化、脂肪化の進行
- 二次的な合併症の出現:線維化や腫瘍性病変の発生
これらの経時的変化を適切に評価することは、疾患の進行度や治療効果の判定において重要であり、継続的な画像評価は、患者さんの長期的な管理において不可欠な要素となります。

治療方法と薬、治癒までの期間
糖原病(とうげんびょう)の治療は、患者さんの生活の質を向上させることを目的としており、日々の健康管理と長期的な合併症予防に重点を置いています。
根本的な治療法はまだ確立されていませんが、症状の緩和と合併症の予防に重点を置いた包括的な管理が、患者さんの状態に応じて細やかに行われています。
治療の中心となるのは食事療法と薬物療法であり、これらを組み合わせることで血糖値の安定化や肝臓などの臓器への負担軽減を図り、患者さんの全身状態の改善を目指します。
患者さんの年齢や病型によって具体的な治療内容は異なりますが、長期的な視点に立った包括的なアプローチが必要不可欠であり、専門医と患者さんが協力して最適な治療計画を立てることが重要です。
食事療法の重要性
食事療法は糖原病治療の要となり、血糖値の急激な変動を避け、安定した状態を維持することを主な目的としています。
| 食事の種類 | 摂取の目安 | 留意点 |
| 炭水化物 | 制限あり | 複合糖質を選択 |
| タンパク質 | 適度に摂取 | 良質なものを選ぶ |
| 脂質 | バランス良く | 不飽和脂肪酸を意識 |
頻回の食事摂取や夜間の経管栄養などが推奨される場合もあり、これにより肝臓での糖新生を抑制し、代謝の安定化を図ることができます。
食事内容や回数は個々の患者さんの状態に応じて調整されるため、栄養士との連携が欠かせず、定期的な見直しと調整が必要となります。
薬物療法の選択肢
薬物療法は、症状のコントロールや合併症の予防に有効であり、病型や重症度に応じて適切な薬剤が選択されます。
- コーンスターチ:緩徐放出型炭水化物として使用し、血糖値の安定化を図る
- 酵素補充療法:不足している酵素を補い、代謝機能の改善を目指す
- ビタミン剤:代謝機能のサポートとして使用し、全身状態の改善を促す
新しい治療薬の開発も進んでおり、遺伝子治療などの革新的なアプローチも研究段階にあり、将来的な治療の選択肢拡大が期待されています。
| 薬剤名 | 主な効果 | 使用上の注意 |
| アセチル-L-カルニチン | エネルギー代謝改善 | 長期使用時の副作用に注意 |
| ジアゾキサイド | インスリン分泌抑制 | 血糖値のモニタリングが必要 |
| ビタミンB複合体 | 代謝機能のサポート | 過剰摂取に注意 |
薬物療法を開始する際には、副作用のリスクや期待される効果について十分な説明を受けることが大切であり、定期的な効果の評価と用量調整が必要となります。
治療期間と経過観察
糖原病は慢性疾患であるため、生涯にわたる管理が求められ、患者さんと医療チームの継続的な協力が重要となります。
治療開始後は定期的な検査と経過観察が行われ、必要に応じて治療内容の調整が行われ、患者さんの状態に合わせた最適な治療を継続します。
| 検査項目 | 頻度 | 目的 |
| 血液検査 | 1-3ヶ月毎 | 代謝状態の評価 |
| 画像検査 | 6-12ヶ月毎 | 臓器の状態確認 |
| 成長発達評価 | 定期的 | 全身状態の把握 |
| 栄養評価 | 3-6ヶ月毎 | 食事療法の効果確認 |
症状の改善や合併症の予防効果が現れるまでには個人差があり、一般的に数週間から数ヶ月程度で一定の効果が得られることが多いようですが、長期的な管理が必要です。
生活指導と支援体制
糖原病患者さんの日常生活では、細やかな配慮が必要となり、運動や感染症への対応などについても専門家のアドバイスを受けながら管理していくことが推奨されます。
- 定期的な運動:体力維持と代謝改善を目的とし、個々の状態に合わせた運動プログラムを実施
- ストレス管理:心身の安定化を図り、ストレス関連のホルモン変動を最小限に抑える
- 感染予防:ワクチン接種や衛生管理を徹底し、感染症による代謝への悪影響を防ぐ
また、患者会や医療機関による支援プログラムなども活用することで、社会生活の質を高め、精神的なサポートを得ることができます。

糖原病(GSD)治療の副作用とリスク
糖原病の食事療法では、厳格な食事制限が必要となる場合があり、患者さんの生活の質に影響を与える可能性があるだけでなく、精神的なストレスの要因にもなりうります。
長期的な栄養バランスの偏りによって、新たな健康上の問題が生じるリスクがあり、特に成長期の子どもたちにとっては深刻な影響を及ぼす可能性があります。
| 栄養素 | 過剰摂取のリスク | 不足のリスク | 長期的な影響 |
| 炭水化物 | 肥満、体重増加 | 低血糖、成長遅延 | インスリン抵抗性 |
| タンパク質 | 腎機能への負担 | 筋力低下、免疫力低下 | 骨密度低下 |
| 脂質 | 脂質異常症 | 必須脂肪酸欠乏 | 心血管系疾患リスク増加 |
| ビタミン・ミネラル | 特定栄養素の過剰蓄積 | 欠乏症状 | 代謝異常、免疫機能低下 |
頻回の食事摂取が必要な場合、睡眠障害や社会生活への支障が生じる可能性があり、患者さんの日常生活全般に大きな影響を及ぼす可能性があります。
夜間の経管栄養を行う際には、誤嚥性肺炎のリスクや経管栄養チューブによる合併症に注意が必要であり、長期的な使用による身体的・心理的負担も考慮しなければなりません。
薬物療法の副作用
糖原病の治療に使用される薬剤にはそれぞれ特有の副作用があり、患者さんの状態に応じて慎重に使用する必要があるため、定期的なモニタリングと用量調整が欠かせません。
コーンスターチ療法では、消化器系の不快感や下痢などの症状が現れることがあり、長期使用による腸内細菌叢の変化や栄養吸収への影響も懸念されます。
| 薬剤 | 主な副作用 | 注意点 | 長期使用のリスク |
| アセチル-L-カルニチン | 嘔気、頭痛 | 長期使用時のモニタリング | 代謝バランスの変化 |
| ジアゾキサイド | 水分貯留、高尿酸血症 | 定期的な腎機能検査 | 膵臓機能への影響 |
| 酵素補充療法 | アレルギー反応 | 投与時の慎重な観察 | 免疫反応の変化 |
| ビタミンB複合体 | 神経症状、皮膚炎 | 過剰摂取に注意 | 肝機能への負担 |
酵素補充療法では、稀にアナフィラキシーショックなどの重篤なアレルギー反応が起こる可能性があり、投与開始時や用量変更時には特に注意深い観察が必要です。
長期的な薬物使用による臓器への負担や予期せぬ副作用の出現に注意を払う必要があり、定期的な全身評価と薬剤の見直しが重要となります。
治療に伴う心理的負担
糖原病の治療は長期にわたるため、患者さんやご家族に大きな心理的負担がかかる可能性があり、特に小児患者の場合は成長過程における自己認識や社会性の発達にも影響を与える可能性があります。
厳格な食事制限や生活管理の継続は精神的ストレスの原因となり、日常生活の楽しみを制限することがあるだけでなく、長期的には抑うつ症状や不安障害のリスクを高める可能性があります。
- 社会生活への影響:食事制限による外食の困難さ、学校や職場での特別な配慮の必要性
- 自己管理へのプレッシャー:血糖値維持の責任感、合併症発症への不安
- 家族関係への影響:過保護や過度の干渉、家族間のストレス増加
- 将来への不安:就職や結婚などのライフイベントに対する懸念
治療の長期化によって治療への意欲が低下し、自己管理が疎かになるリスクがあるため、患者さんの心理状態を定期的に評価し、必要に応じて心理的サポートを提供することが重要です。
定期的な通院や検査の負担も患者さんの生活に大きな影響を与える要因となり、特に遠方からの通院や頻繁な入院が必要な場合は、経済的・時間的負担が増大する可能性があります。
成長発達への影響
小児期からの治療が必要な場合、成長や発達に影響を与える可能性があることに留意する必要があり、特に急成長期における栄養管理と薬物療法のバランスには細心の注意が必要です。
| 影響を受ける可能性のある領域 | 考えられるリスク | 長期的な課題 |
| 身体的成長 | 低身長、骨密度低下 | 成人後の骨折リスク増加 |
| 知的発達 | 学習困難、認知機能への影響 | 学業・職業選択への影響 |
| 社会性の発達 | 対人関係の形成困難 | 社会適応の問題 |
| 性的発達 | 思春期遅発、性腺機能低下 | 生殖能力への影響 |
厳格な食事制限や薬物療法が骨の成長や筋肉の発達に影響を与える可能性があり、特にカルシウムやビタミンDの吸収障害による骨密度低下には注意が必要です。
頻回の低血糖エピソードの経験が脳の発達に影響を及ぼす可能性について注意深い観察が必要であり、定期的な神経心理学的評価と適切な教育支援が重要となります。
長期治療に伴うリスク
糖原病の治療は生涯にわたって継続される必要があり、長期的な視点でのリスク管理が重要不可欠です。
このため、患者さんの加齢に伴う生理的変化と治療の相互作用についても注意深く観察する必要があります。
長期の薬物療法による肝機能や腎機能への影響について定期的な評価と対策が必要となり、特に成人期以降は生活習慣病との併発リスクにも注意を払う必要があります。
| 長期的リスク | 影響を受ける可能性のある臓器 | モニタリング方法 | 予防策 |
| 臓器機能低下 | 肝臓、腎臓 | 定期的な血液検査、画像検査 | 薬剤調整、生活習慣改善 |
| 二次的合併症 | 心臓、骨 | 心機能検査、骨密度測定 | 運動療法、栄養指導 |
| 薬剤耐性 | 全身 | 薬物効果のモニタリング | 新規治療法の検討 |
| 代謝異常 | 内分泌系 | ホルモン検査、代謝産物分析 | 個別化医療の実施 |
治療の長期化に伴い新たな合併症が出現するリスクや既存の治療法の効果が減弱する可能性があるため、最新の医学知見を踏まえた治療法の定期的な見直しが必要となります。
生涯にわたる治療の継続は経済的負担も大きく、QOLの低下につながる場合があるため、社会福祉制度の活用や患者支援団体との連携など、包括的なサポート体制の構築が求められます。

GSDの再発リスクと予防戦略
糖原病(とうげんびょう)は遺伝子の変異に起因する慢性疾患であるため完治することはありませんが、適切な管理により症状のコントロールと生活の質の向上が期待でき、患者さんの日常生活をより豊かなものにすることができます。
再発というよりも症状の悪化や合併症の出現を防ぐことが長期管理の主な目標となり、この取り組みは患者さんの生涯にわたる健康維持と密接に関連しています。
継続的な医療ケアと自己管理が患者さんの健康維持にとって不可欠であり、生涯にわたる取り組みが求められるため、医療チームと患者さん、そしてご家族の協力体制が重要となります。
再発リスクを高める要因
糖原病の症状悪化や合併症発症のリスクを高める要因には様々なものがあり、これらを理解し適切に対処することが長期的な健康管理の鍵となります。
| リスク要因 | 影響 | 予防策 | 長期的な影響 |
| 不適切な食事管理 | 代謝バランスの乱れ | 栄養指導の徹底 | 成長障害、臓器障害 |
| 運動不足 | 筋力低下、代謝効率の低下 | 個別化された運動プログラム | 心血管リスクの増加 |
| ストレス | ホルモンバランスの乱れ | ストレス管理技法の習得 | 免疫機能低下、精神的問題 |
| 感染症 | 代謝負荷の増大 | 予防接種、衛生管理 | 急性増悪、入院リスク増加 |
食事療法の中断や不規則な生活習慣は症状の急激な悪化を招く可能性があり、特に成長期や思春期などの身体的変化が大きい時期には注意深い管理が必要です。
特に成長期や妊娠時などライフステージの変化に伴う代謝変動には注意が必要であり、これらの時期には医療チームとの連携をより密にし、きめ細やかな管理を心がけることが大切です。
予防のための自己管理戦略
糖原病の症状悪化を予防するためには包括的な自己管理戦略が重要であり、日々の生活習慣の中に予防的な行動を組み込むことが長期的な健康維持につながります。
- 食事管理:個別化された栄養計画の遵守、食事日記の記録、定期的な栄養カウンセリングの受診
- 運動習慣:定期的な軽度から中等度の運動の実施、理学療法士の指導に基づく筋力トレーニング
- ストレス管理:リラクゼーション技法の習得と実践、必要に応じて心理カウンセリングの利用
- 睡眠管理:十分な睡眠時間の確保と質の向上、睡眠環境の整備、睡眠障害の早期発見と対処
自己血糖測定や体重管理など日々のモニタリングを通じて早期に異常を発見することが大切であり、これらのデータを医療チームと共有することで、より効果的な予防策を講じることができます。
生活リズムの安定化と規則正しい習慣の維持が長期的な健康管理の基盤となり、これらの習慣を家族や周囲の理解と協力のもとで継続することが、症状悪化の予防に大きく寄与します。
医療チームとの連携による予防
定期的な医療機関の受診と専門医によるフォローアップは症状悪化の予防に欠かせず、患者さんと医療チームが協力して長期的な健康管理計画を立てることが重要です。
| 検査項目 | 頻度 | 目的 | フォローアップ |
| 血液生化学検査 | 3-6ヶ月毎 | 代謝状態の評価 | 栄養・薬物療法の調整 |
| 画像検査 | 年1-2回 | 臓器の状態確認 | 合併症の早期発見と対処 |
| 栄養評価 | 6-12ヶ月毎 | 食事療法の効果確認 | 栄養指導の見直し |
| 運動機能評価 | 年1回 | 筋力や持久力の確認 | 運動プログラムの調整 |
医療チームとのオープンなコミュニケーションを通じて治療計画の調整や新たな問題への対応を行うことが重要であり、患者さんの生活状況や心理的な側面も含めた総合的な評価が予防に役立ちます。
患者会や支援グループへの参加も有効な予防策の一つとなり、同じ悩みを持つ人々との情報交換が助けになることがあるため、積極的な参加を検討することをおすすめします。
ライフステージに応じた予防戦略
糖原病の管理は患者さんのライフステージによって異なるアプローチが必要となり、各段階で直面する課題に応じた予防戦略を立てることが重要です。
| ライフステージ | 主な課題 | 予防戦略 | 支援体制 |
| 小児期 | 成長発達、学校生活 | 家族全体での生活管理 | 学校との連携、家族支援 |
| 思春期 | 自己管理の確立、心理的変化 | 教育と心理的サポート | ピアサポート、移行期医療 |
| 成人期 | 就労、家族形成 | 社会資源の活用 | 就労支援、遺伝カウンセリング |
| 高齢期 | 加齢に伴う合併症 | 多面的な健康管理 | 介護サービス、在宅医療 |
成長に伴う代謝変化や社会的環境の変化に応じて予防戦略を柔軟に調整することが必要であり、患者さんの生活スタイルや価値観を尊重しながら、実行可能な計画を立てることが大切です。
特に思春期から成人期への移行期には自己管理能力の向上と医療チームとの信頼関係構築が重要となり、この時期の適切な支援が生涯にわたる健康管理の基礎となります。
新たな治療法と予防の可能性
糖原病の研究は日々進展しており、新たな治療法や予防法の開発が期待されています。
これらの革新的なアプローチが、将来的に症状悪化の予防や生活の質の向上につながる可能性があります。
遺伝子治療や新規薬剤の開発など革新的なアプローチが症状悪化の予防や生活の質の向上につながる可能性があり、これらの最新技術の進歩に注目することが重要です。
- 遺伝子編集技術:根本的な遺伝子異常の修正、長期的な症状改善の可能性
- 酵素補充療法の改良:より効果的で副作用の少ない製剤の開発、投与方法の簡便化
- バイオマーカーの発見:早期の症状悪化予測と介入、個別化された予防戦略の立案
最新の医学情報に基づいた治療法の更新と予防戦略の見直しが継続的に行われることが大切であり、医療チームと患者さんが協力して最新の知見を治療に取り入れていくことが望ましいです。
患者さん自身が積極的に情報収集を行い医療チームと協力して最適な予防法を選択することが望ましく、このような主体的な姿勢が長期的な健康管理の成功につながります。

治療費
外来診療にかかる費用
定期的な血液検査や画像診断が必要で、1回の外来で15,000円から40,000円程度かかることがあります。特殊な遺伝子検査を行う場合、50,000円以上の追加費用が発生する可能性があります。
入院治療の費用
糖原病はDPCにおいても「出来高算定 代謝性疾患(糖尿病を除く。) 手術処置等2なし」であり、非常に高額になる事があります。
急性増悪時の入院では、1日あたり30,000円から70,000円の費用が発生する場合があります。集中治療室での管理が必要になると、1日100,000円を超えることもあります。
| 項目 | 概算費用 |
| 外来検査 | 15,000-40,000円 |
| 入院費(一般病棟1日) | 30,000-70,000円 |
| 入院費(ICU1日) | 100,000円以上 |
| 特殊遺伝子検査 | 50,000円以上 |
長期的な治療費
年間の治療費は150万円から300万円に達することもあり、患者さんの経済的負担は極めて大きいです。医療費助成制度の活用が重要です。
なお、上記の価格は2024年11月時点のものであり、最新の価格については随時ご確認ください。
以上





