代謝疾患の一種である金属代謝異常症とは、体内の金属元素の代謝バランスが崩れることで引き起こされる病気の総称です。
英語では Metal metabolism disorder と呼ばれるこの疾患群は鉄、銅、亜鉛などの必須金属元素や鉛、水銀などの有害金属元素の代謝に問題が生じることで発症します。
私たちの体は正常な機能を維持するために適切な量の金属元素を必要としていますが、金属代謝異常症ではこれらの金属元素の吸収、輸送、貯蔵、排出のいずれかの過程に障害が生じます。
その結果、体内の金属濃度が過剰になったり不足したりすることで様々な臓器に影響を及ぼし、多様な症状を引き起こすのです。
金属代謝異常症の多様な病型とその特徴
銅代謝異常症の主要病型
金属代謝異常症の中でも銅代謝異常症は特に注目される病型の一つです。
銅代謝異常症には主にウィルソン病とメンケス病という二つの代表的な疾患が含まれます。
ウィルソン病は銅の排出障害により体内に銅が蓄積する遺伝性疾患です。
一方 メンケス病は銅の吸収障害により体内の銅が不足する遺伝性疾患です。
これらの疾患は 同じ銅代謝に関わるものの 、全く異なるメカニズムで発症するという特徴があります。
| 疾患名 | 銅代謝の特徴 |
| ウィルソン病 | 銅の排出障害 |
| メンケス病 | 銅の吸収障害 |
銅代謝異常症の診断には血清銅濃度や尿中銅排泄量の測定など 様々な検査が用いられます。
鉄代謝異常症の代表的疾患
鉄代謝異常症は体内の鉄バランスが崩れることで引き起こされる一群の疾患です。
代表的な鉄代謝異常症にはヘモクロマトーシスと鉄欠乏性貧血が含まれます。
ヘモクロマトーシスは体内に過剰な鉄が蓄積する遺伝性疾患です。反対に鉄欠乏性貧血は体内の鉄が不足することで引き起こされる貧血の一種です。
これらの疾患は鉄の過剰と不足という対照的な状態を示すことが特徴です。
鉄代謝異常症の主な病型には以下のようなものがあります。
- 遺伝性ヘモクロマトーシス
- 二次性ヘモクロマトーシス
- 鉄欠乏性貧血
- 鉄芽球性貧血
上記の病型はそれぞれ異なる遺伝的背景や環境要因によって引き起こされます。
亜鉛代謝異常症の特徴と影響
亜鉛代謝異常症はあまり一般的ではありませんが、重要な金属代謝異常症の一つです。
亜鉛は多くの酵素の補因子として働く必須微量元素であり、その代謝異常は様々な生理機能に影響を及ぼします。
亜鉛代謝異常症に含まれる病態は以下のようなものです。
| 病態 | 特徴 |
| 亜鉛欠乏症 | 体内の亜鉛量が不足 |
| 亜鉛過剰症 | 体内の亜鉛量が過剰 |
亜鉛欠乏症は特に発展途上国や高齢者、特定の疾患を持つ患者さんで見られることがあります。
一方、亜鉛過剰症は比較的まれですが、過剰な亜鉛摂取や特定の遺伝的要因によって引き起こされる可能性があるでしょう。
亜鉛代謝異常症の診断には血清亜鉛濃度の測定や臨床症状の評価などが用いられます。
その他の金属代謝異常症
銅、鉄、亜鉛以外にも様々な金属元素の代謝異常症が知られています。
これらの金属代謝異常症含まれるのは次のようなものです。
- マンガン代謝異常症
- セレン代謝異常症
- モリブデン代謝異常症
- コバルト代謝異常症
これらの金属代謝異常症はそれぞれ特有の臨床像を示し、診断や管理に専門的な知識が必要とされます。
例えばマンガン代謝異常症は 神経系に影響を及ぼすことがあり、パーキンソン病様の症状を引き起こす可能性が高いです。
| 金属元素 | 関連する主な機能 |
| マンガン | 酵素の補因子 抗酸化作用 |
| セレン | 抗酸化酵素の構成要素 |
| モリブデン | 酵素の補因子 |
| コバルト | ビタミンB12の構成要素 |
上記の金属代謝異常症の中には非常にまれなものも含まれており、診断に至るまでに時間を要することがあります。
主要症状と臨床像
銅代謝異常症の特徴的症状
銅代謝異常症の代表的疾患であるウィルソン病とメンケス病では 異なる臨床像が観察されます。
ウィルソン病の主な症状は以下のようなものです。
- 肝機能障害(黄疸 腹水など)
- 神経症状(振戦 構音障害 歩行障害など)
- 精神症状(うつ 不安 認知機能低下など)
- 角膜のカイザー・フライシャー輪
これらの症状は体内に蓄積した銅が様々な臓器に影響を及ぼすことで生じます。
一方メンケス病では次のような症状が特徴的です。
| 症状 | 特徴 |
| 成長障害 | 著しい発育不全 |
| 特徴的な毛髪 | 縮れて脆弱な毛髪 |
| 神経発達遅滞 | 重度の知的障害 |
| 血管異常 | 動脈瘤形成 |
メンケス病の症状は銅欠乏によって様々な酵素活性が低下することで引き起こされます。
鉄代謝異常症における多様な臨床像
鉄代謝異常症では鉄の過剰と欠乏という対照的な状態によって異なる症状が現れるのです。
ヘモクロマトーシスでは過剰な鉄が臓器に蓄積することで以下のような症状が生じます。
- 皮膚の色素沈着(ブロンズ色)
- 関節痛
- 糖尿病
- 心不全
- 肝硬変
これらの症状は長期にわたる鉄の蓄積によって徐々に進行していくというのが特徴です。
対照的に鉄欠乏性貧血では以下のような症状が観察されます。
| 症状 | 詳細 |
| 倦怠感 | 全身の疲労感 |
| 息切れ | 軽い運動でも息苦しさを感じる |
| 頭痛 | 持続的な頭痛 |
| 集中力低下 | 思考力や記憶力の低下 |
これらの症状は 体内の鉄不足によって酸素運搬能力が低下することで引き起こされるのです。
亜鉛代謝異常症の多彩な症状
亜鉛代謝異常症は亜鉛の欠乏または過剰によって様々な症状を呈します。
以下は亜鉛欠乏症の主な症状です。
- 皮膚炎(特に四肢や顔面)
- 味覚障害
- 創傷治癒の遅延
- 免疫機能の低下
これらの症状は亜鉛が関与する多くの生理機能が障害されることで生じます。
一方の亜鉛過剰症では以下のような症状が見られることがあります。
| 症状 | 特徴 |
| 消化器症状 | 嘔気 嘔吐 腹痛 |
| 貧血 | 鉄吸収阻害による二次的貧血 |
| 免疫機能低下 | 感染症のリスク上昇 |
| 神経症状 | 頭痛 めまい |
亜鉛代謝異常症の症状は非特異的なものが多いため他の疾患との鑑別が重要です。
その他の金属代謝異常症の多様な臨床像
銅、鉄、亜鉛以外の金属代謝異常症でも様々な特徴的な症状が観察されます。
マンガン代謝異常症では以下のような神経学的症状が現れることがあります。
- パーキンソン様症状(振戦 筋固縮)
- 歩行障害
- 精神症状(易刺激性 幻覚)
セレン代謝異常症の症状は欠乏と過剰で異なる様相を呈します。
| 状態 | 主な症状 |
| セレン欠乏 | 心筋症 骨格筋障害 |
| セレン過剰 | 爪の変形 脱毛 神経障害 |
モリブデン代謝異常症では代謝性アシドーシスや発達遅滞などが見られることがあります。
コバルト代謝異常症は比較的まれですが、甲状腺機能低下や貧血などの症状を引き起こす可能性があります。
これらの金属代謝異常症の症状は多岐にわたり複雑であることが多いため専門医による詳細な評価が必要です。
金属代謝異常症の症状を理解することは早期診断と適切な管理につながる重要な要素です。
各疾患の特徴的な症状を把握し、注意深く観察することで早期発見の可能性が高まります。
金属代謝異常症は多様な臨床像を呈することから個々の患者さんの症状に応じた細やかなアプローチが大切です。
原因とメカニズム
銅代謝異常症の遺伝的背景
銅代謝異常症の主要な原因は 特定の遺伝子の変異にあります。
ウィルソン病は ATP7B遺伝子の変異によって引き起こされるのです。
この遺伝子は銅を細胞外へ排出する機能を持つタンパク質をコードしており、その機能不全により銅が体内に蓄積します。
一方メンケス病はATP7A遺伝子の変異が原因です。
| 疾患名 | 原因遺伝子 |
| ウィルソン病 | ATP7B |
| メンケス病 | ATP7A |
これらの遺伝子変異は常染色体劣性遺伝または伴性劣性遺伝の形式をとります。
そのため両親から変異遺伝子を受け継ぐか母親がキャリアである場合に発症するというのが特徴です。
鉄代謝異常症の複雑な発症機序
鉄代謝異常症の原因は遺伝的要因と環境要因が複雑に絡み合っています。
ヘモクロマトーシスの主な原因には次の通りです。
| 1型ヘモクロマトーシス | HFE遺伝子の変異 |
| 2型ヘモクロマトーシス | ヘモジュベリン遺伝子の変異 |
| 3型ヘモクロマトーシス | トランスフェリン受容体2遺伝子の変異 |
| 4型ヘモクロマトーシス | フェロポルチン遺伝子の変異 |
このような遺伝子変異は鉄の吸収、輸送、貯蔵に関わるタンパク質の機能に影響を与えます。
一方、鉄欠乏性貧血の原因は次のように多岐にわたります。
| 原因 | 具体例 |
| 鉄摂取不足 | 偏食 菜食主義 |
| 鉄吸収障害 | セリアック病 胃切除後 |
| 鉄喪失 | 慢性出血 月経過多 |
これらの要因が単独または複合的に作用することで体内の鉄バランスが崩れ 鉄欠乏状態に陥るのです。
亜鉛代謝異常症の多様な要因
亜鉛代謝異常症の原因は遺伝的要因と環境要因の両方が関与します。
亜鉛欠乏症の主な原因は以下のようなものです。
- 摂取不足(偏食 栄養不良)
- 吸収障害(炎症性腸疾患 短腸症候群)
- 過剰排泄(慢性腎疾患 アルコール依存症)
- 遺伝的要因(腸性肢端皮膚炎)
これらの要因により体内の亜鉛バランスが崩れて欠乏状態に至ります。
一方で亜鉛過剰症の原因は比較的まれですが、次のような状況で生じる可能性があります。
| 原因 | 詳細 |
| 過剰摂取 | サプリメントの乱用 |
| 職業性暴露 | 亜鉛を扱う工場での曝露 |
| 医原性 | 亜鉛含有製剤の過剰投与 |
このような要因によって体内の亜鉛濃度が異常に上昇し、過剰症状が引き起こされるのです。
その他の金属代謝異常症の多彩な原因
銅、鉄、亜鉛以外の金属代謝異常症にも様々な原因が存在します。
以下はマンガン代謝異常症の主な原因です。
- 職業性暴露(鉱山労働者 溶接工)
- 環境汚染(マンガン含有農薬)
- 肝機能障害(マンガン排泄能の低下)
セレン代謝異常症の原因は地域による土壌中セレン濃度の違いや食習慣と密接に関連しています。
モリブデン代謝異常症は主に遺伝的要因によって引き起こされるのです。
| 疾患 | 原因遺伝子 |
| モリブデン補酵素欠損症 | MOCS1 MOCS2 GPHN |
| 単離性硫酸塩酸化酵素欠損症 | SUOX |
これらの遺伝子変異によってモリブデン含有酵素の機能不全が生じます。
コバルト代謝異常症は比較的まれですが、以下のような原因で生じる可能性があります。
- 職業性暴露(コバルト含有合金の製造)
- 医原性(金属人工関節からの溶出)
- ビタミンB12代謝異常(遺伝的要因)
金属代謝異常症の原因を理解することは適切な予防策や管理方法の選択につながる重要な要素です。
診察と診断アプローチ
初診時の問診と身体診察
金属代謝異常症の診断プロセスは詳細な問診と綿密な身体診察から始まります。
まずは患者さんの家族歴、既往歴、現在の状態などについて丁寧に聞き取りを行いますが、特に注目すべき問診項目は以下のようなものです。
- 家族内での類似症状や診断歴
- 職業歴(金属への曝露の可能性)
- 食生活や栄養摂取状況
- 薬剤やサプリメントの使用状況
身体診察では各金属代謝異常症に特徴的な所見を注意深く観察します。例えばウィルソン病では角膜のカイザー・フライシャー輪を確認することがあります。
これらの情報は金属代謝異常症を疑う重要な手がかりとなるのです。
血液検査による金属濃度評価
金属代謝異常症の診断において血液検査は非常に重要な役割を果たします。各金属の血中濃度を測定することで体内の金属バランスを評価します。
主な検査項目と正常値の例は以下の通りです。
| 検査項目 | 正常値(参考値) |
| 血清銅 | 70-140 μg/dL |
| 血清鉄 | 60-200 μg/dL |
| 血清亜鉛 | 65-110 μg/dL |
| 血清セレン | 5.8-23.4 μg/dL |
これらの値が基準値から大きく外れている場合に金属代謝異常症の可能性が高まります。
また、銅代謝異常症の診断ではセルロプラスミン値の測定も重要です。
尿検査と組織生検による評価
金属代謝異常症の診断では尿検査も重要な情報を提供します。
ここでは24時間蓄尿検査により各金属の尿中排泄量を測定します。
例えばウィルソン病では 尿中銅排泄量が増加していることが特徴的です。
また、必要に応じて組織生検が行われることがあります。特に肝生検はヘモクロマトーシスの診断において重要な役割を果たします。
| 検査 | 評価内容 |
| 24時間蓄尿 | 金属の尿中排泄量 |
| 肝生検 | 肝臓内の金属沈着量 |
これらの検査結果は診断の確定や病状の進行度評価に役立つでしょう。
画像診断による臓器評価
金属代謝異常症の診断過程では画像診断も重要な役割を果たします。
MRIやCTなどの画像検査によって各臓器における金属沈着の程度を視覚的に評価することが可能です。
主な画像検査とその特徴は以下の通りです。
- MRI 非侵襲的に金属沈着量を定量化可能
- CT 肝臓の密度上昇などを確認
- 超音波検査 肝臓や脾臓の形態変化を評価
特にMRIは非侵襲的に金属沈着量を定量化できる点で有用性が高いとされています。
これらの画像検査結果は診断の確定や経過観察に活用されるのです。
遺伝子検査による確定診断
金属代謝異常症の確定診断には遺伝子検査が大切な役割を果たします。
各疾患に関連する遺伝子の変異を特定することで診断の確実性が高まります。
主な検査対象遺伝子は以下の通りです。
| 疾患 | 検査対象遺伝子 |
| ウィルソン病 | ATP7B |
| メンケス病 | ATP7A |
| 遺伝性ヘモクロマトーシス | HFE HJV HAMP TFR2 SLC40A1 |
遺伝子検査の結果は患者さんの病型の特定や家族のスクリーニングにも有用となります。
ただし遺伝子検査の実施にあたっては遺伝カウンセリングなど十分な説明と同意が必要です。
鑑別診断と総合的評価
金属代謝異常症の診断には 他の疾患との鑑別が重要です。
鑑別すべき主な疾患には以下のようなものがあります。
- 自己免疫性肝炎
- アルコール性肝疾患
- 非アルコール性脂肪肝疾患
- 神経変性疾患
これらの疾患との区別を慎重に行うことで 正確な診断が可能となります。
最終的な診断は上記の様々な検査結果と臨床所見を総合的に評価して行われます。
特徴的な画像所見
MRIによる金属沈着の評価
金属代謝異常症の画像診断においてMRIは非常に重要な役割を果たします。
MRIは非侵襲的に体内の金属沈着を定量的に評価できる点で他の画像検査に比べて優れています。
金属沈着の程度によってMRI信号強度が変化するため観察される特徴的な所見は以下の通りです。
| シーケンス | 金属沈着部位の特徴 |
| T1強調画像 | 低信号〜高信号 |
| T2強調画像 | 著明な低信号 |
| T2*強調画像 | より顕著な低信号 |
特にT2*強調画像は 金属に対する感度が高く、軽度の金属沈着でも検出が可能です。
これらの所見は主に肝臓で顕著ですが、脳、心臓、膵臓などの他の臓器でも観察されることがあります。
銅代謝異常症の画像所見
ウィルソン病(Wilson Disease)では脳MRIにおいて主に次のような特徴的な所見が見られます。
- 基底核の対称性信号変化(特に被殻)
- 中脳の「パンダ徴候」
- 小脳や脳幹の信号変化
これらの所見はT2強調画像やFLAIR画像で高信号として観察されることが多いです。
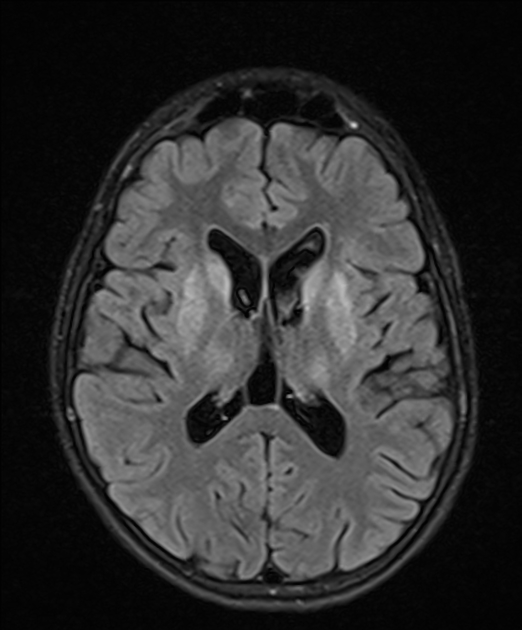
所見:Wilson病の症例。延髄、橋、両側視床および被殻、尾状核においてFLAIR高信号が認められる。
一方メンケス病(Menkes disease)では脳の発達異常や血管異常が特徴的です。
| 画像検査 | メンケス病の特徴的所見 |
| 頭部MRI | 大脳白質の髄鞘化遅延 |
| MRA | 脳血管の蛇行・拡張 |
これらの所見はメンケス病の診断や経過観察に重要な情報を提供します。
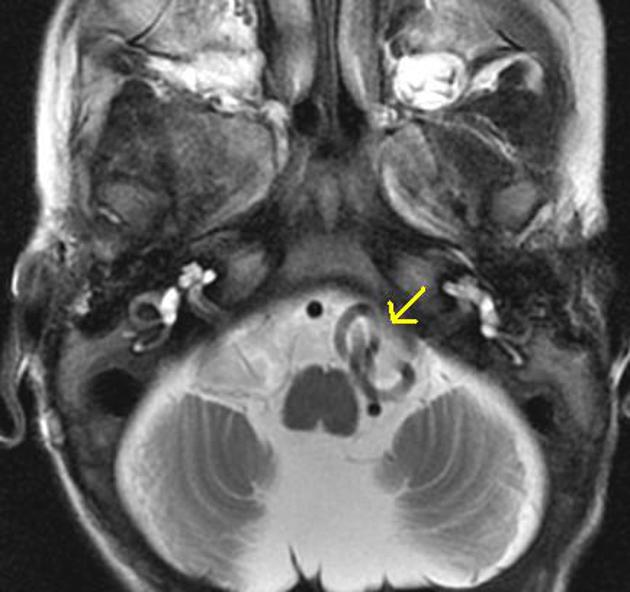
所見:Menkes病の症例。顕著な大脳および小脳の萎縮が認められる。前頭白質の髄鞘形成異常があり、脳内血管の蛇行が認められる。
鉄代謝異常症の画像所見
ヘモクロマトーシス(Hemochromatosis)では肝臓のMRI所見が特に重要です。
肝臓MRIでは以下のような特徴的な所見が見られます。
- T1強調画像での信号低下
- T2強調画像での著明な信号低下
- T2*強調画像でのさらに顕著な信号低下
これらの所見は肝臓内の鉄沈着を反映しています。
また、MRIを用いた定量的評価方法としてR2値やT2値の測定があります。
これらの値は肝臓内の鉄濃度と強い相関があり、数値化することで経時的な変化の追跡が可能です。
鉄欠乏性貧血では 特異的な画像所見は乏しいものの、骨髄MRIにおいて信号変化が観察されることがあります。
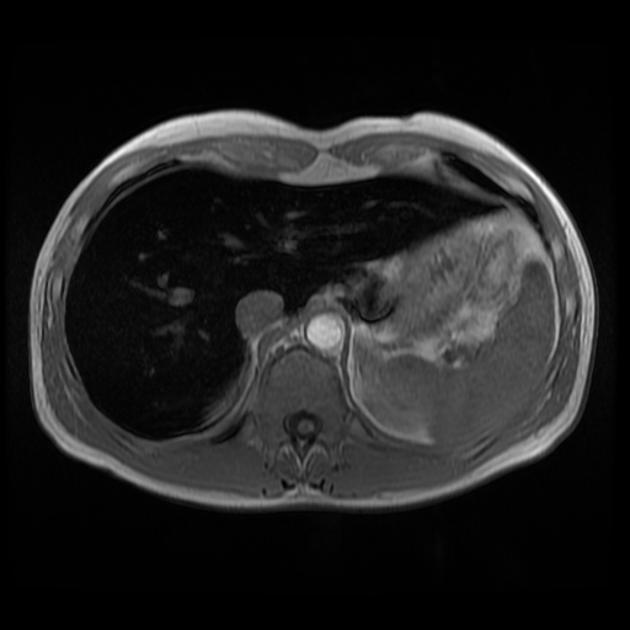
所見:肝実質における全シーケンスでの信号消失は、鉄過負荷によるものである。脾臓には影響がなく、非遺伝性ヘモシデローシスの場合に見られる所見と一致せず。よって原発性ヘモクロマトーシスと考えられる。
亜鉛代謝異常症の画像所見
亜鉛代謝異常症では特異的な画像所見は比較的少ないですが、いくつかの特徴的な所見が報告されています。
亜鉛欠乏症(Zinc deficiency)に関連する画像所見は次のようなものです。
- 脳MRIでの白質病変
- 骨密度の低下(DEXA法による評価)
一方、亜鉛過剰症(Zinc toxity)では以下のような所見が観察されることがあります。
| 臓器 | 画像所見 |
| 肝臓 | 脂肪化 線維化 |
| 膵臓 | 石灰化 |
上記のような所見は亜鉛代謝異常症の診断や合併症評価に役立つ可能性があります。
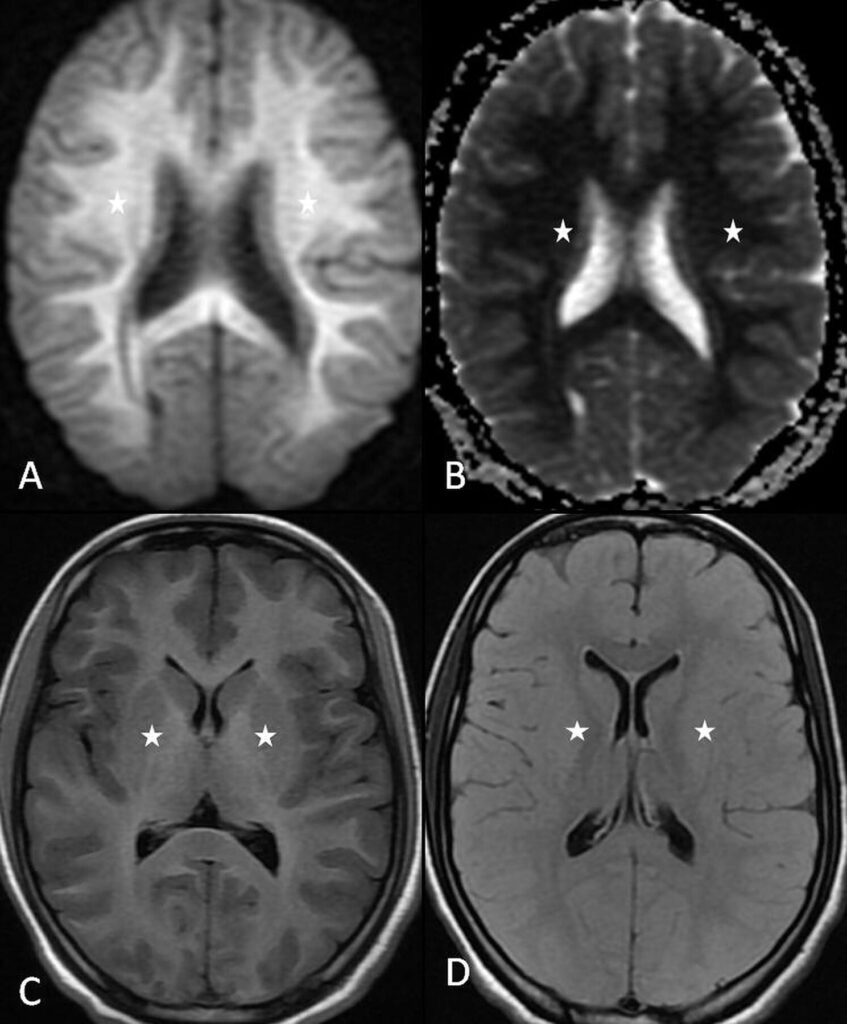
所見:亜鉛過剰症のMRI。(A, B) 両側脳室周囲テント上白質における拡散制限(白星印)が認められ、対応する表面拡散係数(ADC)画像では逆転現象が観察される。(C) T1強調画像および(D) FLAIR画像では、びまん性脳浮腫による脳回と脳溝の消失を除いて、同じ領域に異常は見られない(白星印)。
その他の金属代謝異常症の画像所見
マンガン代謝異常症(Hypermanganesemia)では脳MRIにおいて主に次のような特徴的な所見が見られます。
- 基底核(特に淡蒼球)のT1強調画像での高信号
- 白質のT2強調画像での高信号
このような所見はマンガンの脳内蓄積を反映していると考えられています。
セレン代謝異常症では以下のような画像所見が報告されています。
- 骨X線での骨端部の変化
- 心臓MRIでの心筋症所見
モリブデン代謝異常症やコバルト代謝異常症では特異的な画像所見は乏しいものの、二次的な臓器障害を反映した所見が観察されることがあります。
金属代謝異常症の画像所見を適切に解釈することは診断の確定や経過観察において不可欠です。
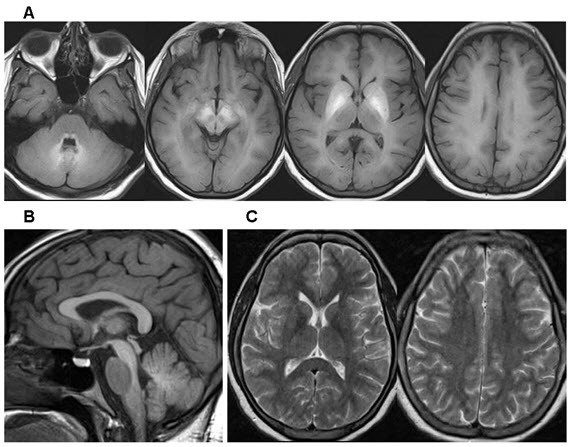
所見:高マンガン血症患者の代表的な脳MRI。
A. 横断T1強調画像。すべての白質からの異常に高い信号戻りと、両側の被殻および淡蒼球からのより顕著な信号戻りが認められる。
B. 矢状断T1強調画像。前部下垂体およびすべての白質、特に脳梁、中脳、背側橋、延髄からの異常に高い信号戻りが認められる。
C. 横断T2強調画像。淡蒼球からの異常に低い信号戻りが、T1強調画像での信号戻りが最も高い領域と同様の分布で認められる。
治療アプローチと経過
銅代謝異常症の治療戦略
銅代謝異常症の代表的疾患であるウィルソン病とメンケス病では 異なる治療アプローチが取られます。
ウィルソン病の主な治療法は次のようなものです。
- キレート剤による銅の排出促進
- 亜鉛製剤による銅吸収抑制
- 食事療法(銅制限)
キレート剤としてはD-ペニシラミンやトリエンチンが使用され、これらの薬剤は体内の過剰な銅と結合して尿中への排泄を促進します。
| 薬剤名 | 主な作用 |
| D-ペニシラミン | 銅キレート |
| トリエンチン | 銅キレート |
| 酢酸亜鉛 | 銅吸収抑制 |
一方メンケス病の治療では銅の補充が中心です。
銅ヒスチジン注射が主な治療法として用いられ、生涯にわたる継続が必要となることがあります。
これらの治療によって症状の改善や進行の抑制が期待されますが、完全な治癒は困難であり長期的な管理が必要です。
鉄代謝異常症の治療法と経過
鉄代謝異常症の治療は鉄の過剰と欠乏という対照的な状態に応じて異なるアプローチが取られます。
ヘモクロマトーシスの主な治療法は以下のようなものです。
- 瀉血療法
- キレート療法
- 食事療法(鉄制限)
瀉血療法は定期的に血液を採取することで体内の過剰な鉄を除去する方法です。
初期は週1〜2回の頻度で行われ、血清フェリチン値が正常化するまで継続されます。
一方、鉄欠乏性貧血の治療は鉄剤の投与が中心です。
| 投与経路 | 代表的な製剤 |
| 経口 | クエン酸第一鉄ナトリウム |
| 静注 | カルボキシマルトース第二鉄 |
経口鉄剤では 3〜6ヶ月の継続投与が一般的ですが、静注鉄剤ではそれよりも短期間で改善が見られることがあるでしょう。
これらの治療によって多くの場合で数ヶ月から1年程度で症状の改善が期待されますが、原因に応じて長期的な管理が必要となることも考えられるのです。
亜鉛代謝異常症の治療アプローチ
亜鉛代謝異常症の治療は亜鉛の過剰と欠乏に応じて異なるアプローチが取られます。
亜鉛欠乏症の治療は以下のような方法です。
- 亜鉛製剤の投与
- 食事指導(亜鉛豊富な食品の摂取)
亜鉛製剤には酢酸亜鉛や硫酸亜鉛などがあり、経口投与が一般的です。
一方、亜鉛過剰症の治療では以下のような対応が取られます。
- 亜鉛摂取の制限
- キレート療法(重症例)
亜鉛代謝異常症の治療期間は原因や重症度によって異なりますが、多くの場合数週間から数ヶ月程度で改善が見られます。
ただし継続的な管理が必要となることもあり、定期的な検査と適切な対応が重要です。
その他の金属代謝異常症の治療
マンガン、セレン、モリブデンなどの金属代謝異常症の治療はそれぞれの病態に応じて個別化されます。
マンガン中毒の治療は主に以下の通りです。
- 曝露源からの隔離
- キレート療法(EDTAなど)
セレン代謝異常症の治療は 欠乏と過剰で異なります。
| 状態 | 治療アプローチ |
| セレン欠乏 | セレン補充療法 |
| セレン過剰 | 摂取制限 対症療法 |
モリブデン欠乏症ではモリブデン補充が行われますが、非常にまれな疾患で専門的な管理が必要です。
これらの金属代謝異常症の治療期間は個々の症例や原因によって大きく異なり、一概に言及することは困難です。
多くの場合で長期的な経過観察と管理が必要となります。
治療に伴う副作用とリスク
銅代謝異常症治療の副作用
ウィルソン病の治療に用いられるキレート剤にはいくつかの副作用が報告されています。
D-ペニシラミンの主な副作用は以下のようなものです。
- 皮疹や掻痒感
- 味覚異常
- 白血球減少
- 血小板減少
- 蛋白尿
これらの副作用は投与初期に比較的高頻度で見られることがあります。
トリエンチンの副作用はD-ペニシラミンと比較して軽度とされていますが、以下のような事象が報告されています。
| 副作用 | 頻度 |
| 消化器症状 | 比較的多い |
| 貧血 | まれ |
| 神経症状 | まれ |
亜鉛製剤の副作用としては主に消化器症状が挙げられます。
メンケス病の治療で用いられる銅ヒスチジン注射では 注射部位反応や過敏症が生じる可能性があるのです。
このような副作用は患者さんのQOLに影響を与えることがあるため注意深いモニタリングが必要です。
鉄代謝異常症治療のリスク
ヘモクロマトーシスの主な治療法である瀉血療法にはいくつかのリスクが伴います。
瀉血療法に関連する主なリスクには以下のようなものがあります。
- 貧血
- めまいや立ちくらみ
- 血管迷走神経反射
- 静脈炎
これらのリスクは特に高齢者や心疾患を有する患者さんで顕著になる可能性があります。
一方、鉄欠乏性貧血の治療で用いられる鉄剤にも副作用が存在します。
経口鉄剤の主な副作用は次の通りです。
- 便秘や下痢
- 吐き気
- 腹痛
- 歯の着色
静注鉄剤ではさらに重篤な副作用が報告されています。
| 副作用 | 重症度 |
| アナフィラキシー | 重度 |
| 低リン血症 | 中等度〜重度 |
| 頭痛 | 軽度〜中等度 |
上記のような副作用のリスクを十分に考慮して個々の患者さんの状態に応じた投与経路の選択が重要です。
亜鉛代謝異常症治療の課題
亜鉛代謝異常症の治療に用いられる亜鉛製剤にはいくつかの副作用が報告されています。
以下は亜鉛製剤の主な副作用です。
- 悪心・嘔吐
- 腹痛
- 味覚異常
- 銅欠乏(長期投与時)
これらの副作用は多くの場合一過性ですが、患者さんの服薬アドヒアランスに影響を与えることがあります。
特に銅欠乏については長期投与時に注意が必要です。
| 副作用 | 発現時期 |
| 消化器症状 | 投与初期 |
| 銅欠乏 | 長期投与時 |
亜鉛過剰症の治療では キレート剤が用いられることがありますが、これらの薬剤にも固有の副作用があることに留意が必要です。
その他の金属代謝異常症治療のデメリット
マンガン セレン モリブデンなどの金属代謝異常症の治療にもそれぞれ固有のリスクが存在します。
マンガン中毒の治療に用いられるキレート剤(EDTA)の主なリスクは次の通りです。
- 腎毒性
- 電解質異常
- 骨髄抑制
セレン代謝異常症の治療では過剰投与によるセレン中毒のリスクに注意が必要です。
セレン中毒の症状には以下のようなものがあります。
- 爪の変形
- 脱毛
- 神経障害
モリブデン代謝異常症の治療は非常に専門的であり、副作用のリスクについても十分な知見が蓄積されていません。
これらの金属代謝異常症の治療に伴うリスクは個々の症例や原因によって大きく異なるため、慎重な管理が必要です。
長期治療に伴う心理的負担
金属代謝異常症の多くは長期にわたる治療や管理が必要となるため 患者さんに心理的な負担をもたらすことがあります。
長期治療に伴う心理的影響は次のようなものです。
- 治療の継続に対する不安
- 薬剤の副作用への懸念
- 社会生活への影響
- 経済的負担
このような心理的負担は治療のアドヒアランスに影響を与える可能性があるため適切な支援が重要です。
| 心理的側面 | 支援方法 |
| 不安・抑うつ | 心理カウンセリング |
| 社会的孤立 | 患者会への参加 |
長期的な視点に立って患者さんの心理面にも配慮した包括的なアプローチが求められます。
金属代謝異常症の治療に伴う副作用やリスクを理解して適切に管理することは患者さんのQOL維持と長期的な予後改善にとって大切です。
医療者と患者さんが密接に連携して個々の状況に応じた最適なアプローチを選択することが、副作用やリスクの最小化につながる可能性があります。
治療の利益とリスクを慎重に比較衡量し、患者さんと十分な情報共有を行いながら最適な治療方針を決定することが重要です。
再発リスクと予防戦略
銅代謝異常症の長期管理と再発予防
銅代謝異常症における「再発」は 一度改善した体内の銅バランスが再び崩れることを指します。
ウィルソン病では継続的な管理が再発予防の鍵です。
再発リスクを低減するための主な方策には以下のようなものがあります。
- 定期的な血液検査(血清銅 セルロプラスミン)
- 24時間蓄尿検査による尿中銅排泄量の確認
- 食事中の銅摂取量の管理
これらのモニタリングと生活管理を通じて体内の銅バランスを適切に保つことが大切です。
| 検査項目 | 推奨頻度 |
| 血清銅 | 3〜6ヶ月毎 |
| 尿中銅排泄量 | 6〜12ヶ月毎 |
| 肝機能検査 | 3〜6ヶ月毎 |
メンケス病では遺伝的要因が強いため「再発」という概念はあまり適用されませんが、継続的な管理が重要です。
鉄代謝異常症の再発リスクと予防策
鉄代謝異常症では病型によって再発リスクと予防策が異なります。
ヘモクロマトーシスでは 以下のような予防策が推奨されます。
- 定期的な血清フェリチン値のチェック
- 必要に応じたメンテナンス瀉血
- アルコール摂取の制限
- 鉄分強化食品の過剰摂取を避ける
これらの対策により体内の鉄バランスを適切に保つことが可能とるでしょう。
一方、鉄欠乏性貧血では次のような再発予防策が考えられます。
| 予防策 | 詳細 |
| 食事指導 | 鉄分豊富な食品の摂取 |
| 定期検査 | 血液検査による経過観察 |
| 原因対策 | 出血源の特定と管理 |
これらの対策を個々の患者さんの状況に応じて適切に実施することが大切です。
亜鉛代謝異常症の再発予防と生活管理
亜鉛代謝異常症の再発予防には継続的なモニタリングと生活管理が重要です。
亜鉛欠乏症の再発を予防するための主な方策には以下のようなものがあります。
- 定期的な血清亜鉛濃度の測定
- 亜鉛豊富な食品の適切な摂取
- 吸収阻害因子(フィチン酸など)の過剰摂取を避ける
一方、亜鉛過剰症の再発予防では 以下のような点に注意が必要です。
- サプリメントの適切な使用
- 職業性曝露の管理
- 定期的な尿中亜鉛排泄量の確認
| 状態 | モニタリング項目 |
| 亜鉛欠乏 | 血清亜鉛濃度 |
| 亜鉛過剰 | 尿中亜鉛排泄量 |
これらのモニタリングと生活管理を通じて体内の亜鉛バランスを適切に保つことが可能となります。
その他の金属代謝異常症の再発管理
マンガン、セレン、モリブデンなどの金属代謝異常症でも再発予防のための管理が重要です。
マンガン中毒の再発予防には以下のような対策が考えられます。
- 職業性曝露の厳重な管理
- 定期的な血中・尿中マンガン濃度の測定
- 脳MRIによる経過観察
セレン代謝異常症の再発予防策は欠乏と過剰で異なります。
| 状態 | 予防策 |
| セレン欠乏 | 適切な食事指導 セレン含有食品の摂取 |
| セレン過剰 | 環境要因の管理 サプリメント使用の注意 |
モリブデン代謝異常症では 遺伝的要因が強いため「再発」という概念はあまり適用されませんが、継続的な管理が重要です。
ライフスタイル管理と環境要因の制御
金属代謝異常症の再発予防にはライフスタイル全般にわたる管理が重要です。
主な管理項目には以下のようなものがあります。
- バランスの取れた食事
- 適度な運動
- ストレス管理
- 十分な睡眠
また、環境要因の制御も再発予防に重要な役割を果たします。
職業性曝露や環境汚染による金属摂取を最小限に抑えるための対策が必要です。
これらのライフスタイル管理と環境要因の制御は金属代謝異常症の長期的な管理において不可欠な要素となります。
金属代謝異常症の治療費
金属代謝異常症の治療費は長期的な管理が必要なため高額になる可能性があります。
初診料や検査費用、薬剤費、定期的な処置費用など様々な要素が含まれます。
公的医療保険や高額療養費制度の利用で患者負担を軽減できますが、それでも経済的負担は大きいと考えておいてよいでしょう。
初診・再診料と検査費用
初診料は2,910円~5,410円、再診料は750円~2,660円程度です。
血液検査費用は1回あたり5,000円から10,000円程度かかることがあります。
薬剤費と処置費用
ウィルソン病の治療薬であるD-ペニシラミンは月額1,161~3,483円程度です。瀉血療法は1回あたり2,500円です。
| 項目 | 費用 |
| 初診料 | 2,910円~5,410円 |
| 再診料 | 750円~2,660円 |
| 血液検査 | 4,200円(血液一般+生化学5-7項目の場合) +110円(鉄)+230円(銅)+270点(マンガン) |
| D-ペニシラミン | メタルカプターゼカプセル100mg 38.7円 (100mg1カプセル)× 1~3回 × 30日 =1,161~3,483円 |
入院費と長期管理費用
合併症治療のための入院が必要な場合、1日あたり10,000円から30,000円程度の負担が発生します。
長期的な管理費用は年間数十万円に及ぶ可能性も考えられます。
詳しく説明すると、日本の入院費計算システムは、「DPC(診断群分類包括評価)」という方式で入院費を算出します。これは患者さんの病気や治療内容に応じて費用を決める仕組みです。
DPCの特徴:
- 約1,400種類の病気グループに分類
- 1日ごとの定額制
- 一部の特殊な治療は別途計算
昔の「出来高」方式と比べると、DPCでは多くの診療行為が1日の定額に含まれます。
DPCと出来高方式の違い:
・出来高で計算されるもの:手術、リハビリ、特定の処置など
・DPCに含まれるもの:薬、注射、検査、画像診断など
計算方法:
(1日の基本料金) × (入院日数) × (病院ごとの係数) + (別途計算される治療費)
医療費の支払いについて、もう少し詳しく説明します。
1. 健康保険の適用
・保険が使える場合、患者さんが支払う金額は全体の10%から30%になります。
・年齢や収入によって、この割合が変わります。
2. 高額医療費制度
・医療費が一定額を超えると、この制度が適用されます。
・結果として、実際に支払う金額がさらに少なくなることがあります。
3. 料金の変更について
・ここでお話しした金額は2024年8月時点のものです。
・医療費は状況によって変わることがあるので、最新の情報は病院や健康保険組合に確認するのがよいでしょう。
経済的支援制度
難病医療費助成制度の活用により自己負担額の上限が設定される場合があります。また、民間の医療保険や生命保険の活用も経済的負担軽減に役立つでしょう。
| 支援制度 | 概要 |
| 難病医療費助成 | 自己負担上限額の設定 |
| 民間医療保険 | 入院・手術費用の補償 |
以上