感染症の一種である溶血性尿毒症症候群(HUS)は、主に大腸菌などの細菌感染によって引き起こされる重篤な疾患(しっかん)です。
この病気の特徴は、赤血球の破壊、血小板の減少、そして腎臓の機能障害です。
HUSは珍しい病気ですが、特に幼児や高齢者の健康に深刻な影響を及ぼす可能性があります。
症状は多くの場合突然現れ、下痢、腹痛、発熱などから始まります。重症化すると、貧血や出血傾向が見られ、さらには腎不全に至ることもあります。

溶血性尿毒症症候群(HUS)の主症状
溶血性尿毒症症候群の主要な症状について詳細に解説し、患者様とそのご家族の理解を深めることを目的としています。
初期症状
HUSの初期段階では、一般的な胃腸炎に類似した症状が出現します。
患者様は、激烈な腹痛や頻回な水様性下痢を経験し、これらの症状は数日間持続する傾向にあります。
下痢に血液が混入する血便が観察されることもあり、これはHUSを疑う重要な指標となります。
また、多くの事例で38度以上の高熱や嘔吐、全身倦怠感といった症状も併発します。
これらの初期症状は、HUSの進行を示す重要な警告サインであり、早期発見につながります。
| 症状 | 特徴 |
| 下痢 | 水様性、頻回 |
| 腹痛 | 激烈 |
| 血便 | 下痢に血液混入 |
| 発熱 | 38度以上 |
血液学的症状
HUSの進行に伴い、患者様の血液系統に顕著な変化が現れます。
溶血性貧血(赤血球が異常に破壊される状態)は、HUSの主要な特徴の一つです。
この状態では、患者様は極度の疲労感や息切れ、めまい、頭痛などを感じます。
さらに、血小板減少症も発症し、これにより出血傾向が強まります。
患者様は、皮膚や粘膜に点状出血や紫斑が現れたり、鼻出血や歯肉出血が起こりやすくなったりします。
2019年に発表された研究によると、HUS患者の約95%が血小板減少を呈し、その程度は疾患の重症度と相関することが明らかになりました。
これらの血液学的症状は、HUSの診断において非常に重要な指標となります。
腎機能障害の症状
HUSの最も危険な合併症の一つが急性腎不全(腎臓の機能が急激に低下する状態)です。
腎臓の機能が急激に低下することで、患者様はさまざまな症状を経験します。
尿量の減少や無尿は、腎機能障害の初期サインとして現れ、患者様やご家族が気づきやすい症状の一つです。
また、体内に水分や老廃物が蓄積することで、急激な体重増加や浮腫(むくみ)が観察されます。
特に、目の周りや手足のむくみは顕著に現れやすく、患者様が自覚しやすい症状です。
さらに、尿毒症(腎臓が老廃物を十分に排出できない状態)による症状として、吐き気や食欲不振、倦怠感の増強なども現れます。
| 症状 | 原因 |
| 尿量減少・無尿 | 腎機能低下 |
| 浮腫 | 水分貯留 |
| 急激な体重増加 | 水分・老廃物蓄積 |
| 吐き気・食欲不振 | 尿毒症 |
神経系症状
HUSの進行に伴い、神経系にも影響が及びます。
患者様は、以下のような神経系の症状を経験します。
- 意識レベルの変化(傾眠やせん妄)
- けいれん発作
- 頭痛
- めまい
- 視力の一時的な低下
これらの症状は、脳への血流低下や電解質バランスの乱れ、尿毒症性脳症(尿毒症によって引き起こされる脳機能障害)などによって起こります。
神経系症状の出現は、HUSの重症化を示す重要なサインであり、迅速な医学的対応が求められます。
循環器系症状
HUSは、循環器系にも影響を及ぼし、患者様の全身状態に深刻な影響を与えます。
貧血や腎機能障害の進行により、心臓に負担がかかり、様々な循環器系の症状が現れます。
高血圧は、HUSに伴う腎機能障害の結果として生じることが多く、患者様は頭痛や胸痛、動悸を感じます。
また、重症例では、うっ血性心不全(心臓のポンプ機能が低下し、体液が貯留する状態)や心膜炎(心臓を覆う膜の炎症)などの合併症が生じ、呼吸困難や胸痛、浮腫の悪化といった症状が現れます。
| 症状 | 関連する状態 |
| 高血圧 | 腎機能障害 |
| 動悸 | 貧血、心臓負担 |
| 呼吸困難 | うっ血性心不全 |
| 胸痛 | 心膜炎 |
これらの循環器系症状は、HUSの重症度を反映する重要な指標となり、患者様の全身管理において慎重なモニタリングを行います。
HUSの症状は年齢によっても現れ方が異なります。
特に小児や高齢者では、症状が非典型的であったり、急速に進行したりするため、注意深い観察を行います。
HUSの症状に気づいた場合や疑わしい症状がある場合は、速やかに医療機関を受診し、適切な診断と対応を受けることが重要です。

HUSの発症メカニズム
溶血性尿毒症症候群(HUS)は、複雑な病態を呈する重篤な疾患です。本稿では、HUSの主要な原因と発症のトリガーとなる要因について詳細に解説いたします。
HUSの発症メカニズムを把握することで、予防や早期発見に役立つ知見を獲得できます。
細菌感染によるHUS
HUSの最も一般的な原因は、特定の細菌感染です。
志賀毒素産生性大腸菌(STEC)として知られる病原性大腸菌の一種が、HUS発症の主たる要因となります。
この細菌には、O157:H7型を筆頭に様々な血清型が存在し、汚染された食品や水を介して人体に侵入します。
STECは腸管内で増殖し、志賀毒素を産生することで腸管上皮細胞を損傷し、血中に毒素を放出します。
| 細菌名 | 主な感染源 |
| STEC O157:H7 | 生肉、未加熱の食品 |
| STEC O26 | 乳製品、野菜 |
| STEC O111 | 飲料水 |
志賀毒素の作用機序
志賀毒素は、HUS発症において中心的な役割を果たす毒素です。
この毒素は小腸から吸収され、血流に乗って全身を循環し、特に腎臓の血管内皮細胞に強い親和性を示します。
毒素が血管内皮細胞と結合すると、細胞死を誘発し、血管壁の損傷や炎症反応を惹起します。
この過程により、血小板の活性化や凝固系の亢進が起こり、微小血栓が形成されます。
血栓形成は腎臓の微小血管を閉塞させ、腎機能障害を引き起こすと同時に、赤血球の破壊(溶血)を促進します。
- 志賀毒素の作用過程
- 血管内皮細胞への結合
- 細胞死の誘導
- 炎症反応の惹起
- 血小板活性化と凝固亢進
非典型的HUSの原因
一方で、細菌感染とは無関係に発症する非典型的HUSも存在します。
この型のHUSは、補体系(体内の防御機構の一つ)の異常によって発症します。
補体系の制御因子である補体H因子や補体I因子などの遺伝子変異が、主たる原因となります。
これらの変異により、補体系の過剰な活性化が生じ、血管内皮細胞が傷害されます。
非典型的HUSは遺伝性であることが多く、家族歴のある患者さんは特に注意します。
| 遺伝子 | 関連する補体因子 |
| CFH | 補体H因子 |
| CFI | 補体I因子 |
| MCP | 膜補助因子 |
環境要因とHUS
HUSの発症には、環境要因も重要な役割を果たします。
食品衛生の不備や水質汚染は、STEC感染のリスクを高める主要な要因となります。
特に夏季は細菌の増殖が活発になるため、HUSの発症リスクが上昇します。
また、集団生活の場(保育園や学校など)では感染が拡大しやすいため、細心の注意を払います。
さらに、抗生物質の不適切な使用は腸内細菌叢のバランスを崩し、STECの増殖を促進します。
| 環境要因 | リスク |
| 夏季 | 細菌増殖の活性化 |
| 集団生活 | 感染拡大のリスク |
| 抗生物質使用 | 腸内細菌叢の乱れ |
免疫系の関与
HUSの発症には、患者の免疫系も深く関与しています。
志賀毒素による組織傷害は、免疫系を活性化し、炎症反応を誘発します。
この過剰な免疫応答が、血管内皮細胞のさらなる損傷を招き、病態を悪化させます。
また、自己免疫疾患を有する患者さんでは、HUSの発症リスクが上昇すると報告されています。
免疫抑制剤の使用や臓器移植後の患者さんも、HUS発症のハイリスク群に分類されます。
- HUS発症リスクの高い患者群
- 自己免疫疾患患者
- 免疫抑制剤使用者
- 臓器移植後の患者
HUSの原因は複雑で多岐にわたります。細菌感染、遺伝的要因、環境要因、そして免疫系の関与など、様々な要素が相互に作用して発症に至ります。
これらの要因を理解することは、HUSの予防や早期発見において極めて重要です。
特に感染源となりうる食品や水の衛生管理に留意し、自身の健康状態や家族歴を把握しておくことが大切です。

診察と診断
溶血性尿毒症症候群(HUS)は迅速な診断と対応を要する深刻な疾患です。
初期評価と問診
HUSが疑われる患者様に対しては、まず詳細な病歴聴取と綿密な身体診察を実施します。
医師は患者様の最近の食事内容、特に生肉や未殺菌の乳製品の摂取歴について慎重に聴取します。
加えて、家族や周囲の人々における類似症状の有無も、診断の手がかりとなる重要な情報です。
身体診察では、皮膚や粘膜の蒼白、黄疸、出血傾向などを注意深く観察し、HUSを示唆する徴候を探ります。
| 聴取項目 | 確認内容 |
| 食事歴 | 生肉、未殺菌乳製品 |
| 周囲の状況 | 類似症状の有無 |
| 既往歴 | 自己免疫疾患、臓器移植 |
血液検査
HUSの診断において、血液検査は中核をなす重要な役割を担います。
完全血球計算(CBC)では、赤血球数、ヘモグロビン値、血小板数の減少が特徴的な所見となり、HUSを強く示唆します。
末梢血塗抹標本の顕微鏡観察では、破砕赤血球(schisocytes)の存在が重要な診断の手がかりとなり、微小血管障害性溶血を裏付けます。
生化学検査では、血清クレアチニン値やBUN(血中尿素窒素)の上昇が腎機能障害を示し、LDH(乳酸脱水素酵素)の上昇は溶血の程度を反映します。
- 主要な血液検査項目
- 完全血球計算(CBC)
- 末梢血塗抹標本
- 血清クレアチニン、BUN
- LDH(乳酸脱水素酵素)
尿検査と培養検査
尿検査もまた、HUSの診断において欠かせない重要な検査です。
尿検査では、血尿やタンパク尿の有無を確認し、腎臓への影響を評価します。
さらに、尿沈渣の顕微鏡検査で赤血球円柱や顆粒円柱の存在を確認することで、腎臓の障害をより詳細に把握できます。
便培養検査は、志賀毒素産生性大腸菌(STEC)の検出に不可欠であり、HUSの原因菌を特定する上で極めて重要です。
STECが検出された場合、さらに毒素遺伝子型の同定を行い、より詳細な病原体の特徴を明らかにします。
| 検査項目 | 確認内容 |
| 尿検査 | 血尿、タンパク尿 |
| 尿沈渣 | 赤血球円柱、顆粒円柱 |
| 便培養 | STECの検出 |
画像診断
HUSの診断過程では、腹部超音波検査やCTスキャンなどの画像診断も実施します。
これらの検査は、腎臓の腫大や浮腫、腸管の肥厚などの所見を評価し、HUSによる臓器への影響を視覚的に確認します。
また、腹水の有無や他の臓器への影響を確認する上でも、画像診断は重要な役割を果たします。
ドップラー超音波検査は、腎血流の評価に特に有用で、HUSによる腎機能障害の程度を判断する上で貴重な情報をもたらします。
補体系検査と遺伝子解析
非典型的HUS(aHUS)が疑われる際には、補体系(体内の防御機構の一つ)の機能評価が重要となります。
血清中の補体成分(C3、C4など)の測定や補体制御因子の活性評価を行い、補体系の異常を詳細に調べます。
また、補体制御因子の遺伝子解析も、aHUSの診断に大切な役割を果たし、遺伝的背景を明らかにします。
これらの検査結果は、治療方針の決定や長期的な予後予測にも大きな影響を与えるため、慎重に解釈します。
| 検査項目 | 目的 |
| 補体成分測定 | C3、C4の評価 |
| 補体制御因子活性 | 機能異常の検出 |
| 遺伝子解析 | 変異の同定 |
鑑別診断
HUSの診断においては、類似の臨床像を呈する他の疾患との鑑別が極めて重要です。
特に、血栓性血小板減少性紫斑病(TTP)は、HUSと酷似した症状を示すため、慎重な鑑別を要します。
TTPでは、ADAMTS13(血液凝固に関与する酵素)活性の著明な低下が特徴的であり、この検査がHUSとTTPの鑑別診断の決め手となります。
その他、播種性血管内凝固症候群(DIC)や他の溶血性貧血疾患も鑑別の対象となり、総合的な判断が求められます。
- HUSの主な鑑別疾患
- 血栓性血小板減少性紫斑病(TTP)
- 播種性血管内凝固症候群(DIC)
- 他の溶血性貧血疾患
HUSの診断は、複数の検査結果と臨床所見を総合的に評価して行われます。
迅速かつ正確な診断は患者様の予後を大きく左右するため、疑わしい症例に遭遇した際には、速やかに専門医への相談を検討することが望ましいでしょう。

溶血性尿毒症症候群(HUS)の画像所見:診断と経過観察を支える視覚的指標
超音波検査(エコー)所見
超音波検査は、HUSの初期評価や経過観察に広く用いられる非侵襲的な検査法として、臨床現場で重宝されています。
腎臓の超音波所見では、腎臓の腫大や皮髄境界(腎臓の外側と内側の境目)の不明瞭化が特徴的に観察されます。
急性期には腎臓のechogenicity(エコー輝度、超音波の反射強度)が上昇し、皮質が髄質よりも明るく描出される傾向が見られます。
ドプラ超音波を用いると、腎血流の低下や抵抗指数(RI、血管抵抗の指標)の上昇が確認されることが多く、腎機能障害の程度を推測する手がかりとなります。
| 超音波所見 | 特徴 |
| 腎臓サイズ | 腫大 |
| 皮髄境界 | 不明瞭化 |
| Echogenicity | 皮質で上昇 |
| 血流 | 低下、RI上昇 |

CT(コンピュータ断層撮影)所見
CT検査は、HUSによる腎臓や他の臓器への影響を詳細に評価するのに有用で、三次元的な情報を提供します。
単純CTでは、腎臓の腫大や皮髄境界の不明瞭化が観察され、超音波検査の所見を裏付けます。
造影CTでは、腎実質の造影不良や楔状の造影欠損が特徴的な所見となり、血流障害の範囲や程度を視覚化します。
さらに、腸管壁の肥厚や浮腫、腹水の存在なども確認され、HUSの全身への影響を包括的に評価できます。
- CT検査で確認される主な所見
- 腎臓の腫大
- 皮髄境界の不明瞭化
- 腎実質の造影不良
- 楔状の造影欠損
- 腸管壁の肥厚・浮腫
- 腹水の存在
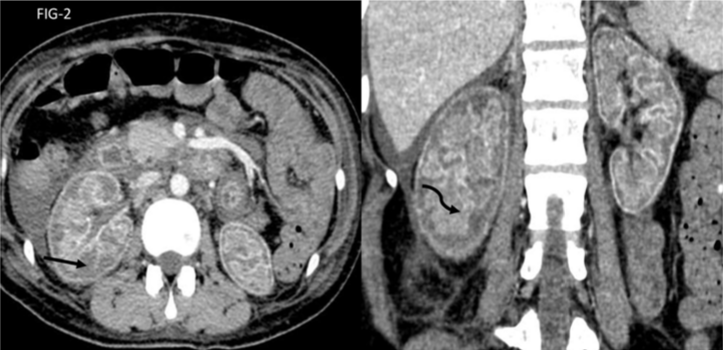
所見:「腎皮質壊死の症例。造影CT(CECT)の軸位および冠状断画像では、正常な造影効果を示す腎髄質(黒い曲線矢印)と、造影効果のない腎皮質(黒い直線矢印)が認められ、reverse rim signを呈している。」
MRI(磁気共鳴画像)所見
MRIは、放射線被曝がなく軟部組織のコントラスト分解能に優れているため、HUSの詳細な評価に適しており、特に小児患者や妊婦の検査に適しています。
T2強調画像では、腎臓の信号強度が上昇し、皮質と髄質のコントラストが低下する様子が観察されます。
拡散強調画像(DWI、水分子の拡散運動を可視化する撮像法)では、急性期の腎障害部位が高信号を示すことがあり、早期の病変検出に役立ちます。
造影MRIでは、CTと同様に、腎実質の造影不良や楔状の造影欠損が観察され、血流障害の詳細な評価が可能です。
| MRI所見 | 特徴 |
| T2強調画像 | 腎臓信号上昇 |
| DWI | 障害部位高信号 |
| 造影MRI | 造影不良・欠損 |
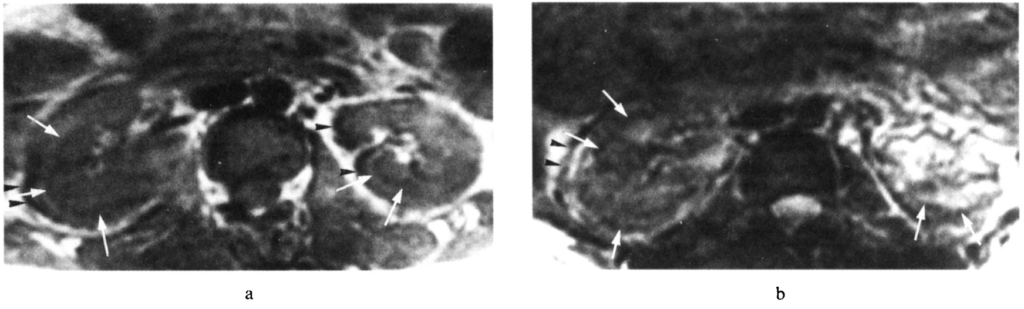
所見:「発症10日目の腎臓のMR画像。a) T1強調画像(TR/TE 500/30 ms)では、皮質髄質接合部領域に低信号のリム(—►)に囲まれた腎皮質の高信号が示されている。腎臓の右縁に沿った薄い低信号リム(►)は、おそらく化学シフトアーチファクトを表している。b) T2強調画像(TR/TE 2000/80 ms)では、腎皮質の信号強度が増加しているが、皮質髄質接合部では低信号が持続している(—>)。」
腹部X線検査所見
腹部X線検査は、HUSの診断に特異的ではありませんが、合併症の評価に役立つことがあり、迅速かつ簡便な検査法として活用されています。
腸管の拡張や、腸管壁の肥厚による thumb printing sign(拇印様陰影、腸管壁の肥厚による特徴的な陰影)が観察されることがあります。
また、遊離ガス像が見られる場合は、腸管穿孔を疑う重要な所見となり、緊急対応が必要となることがあります。
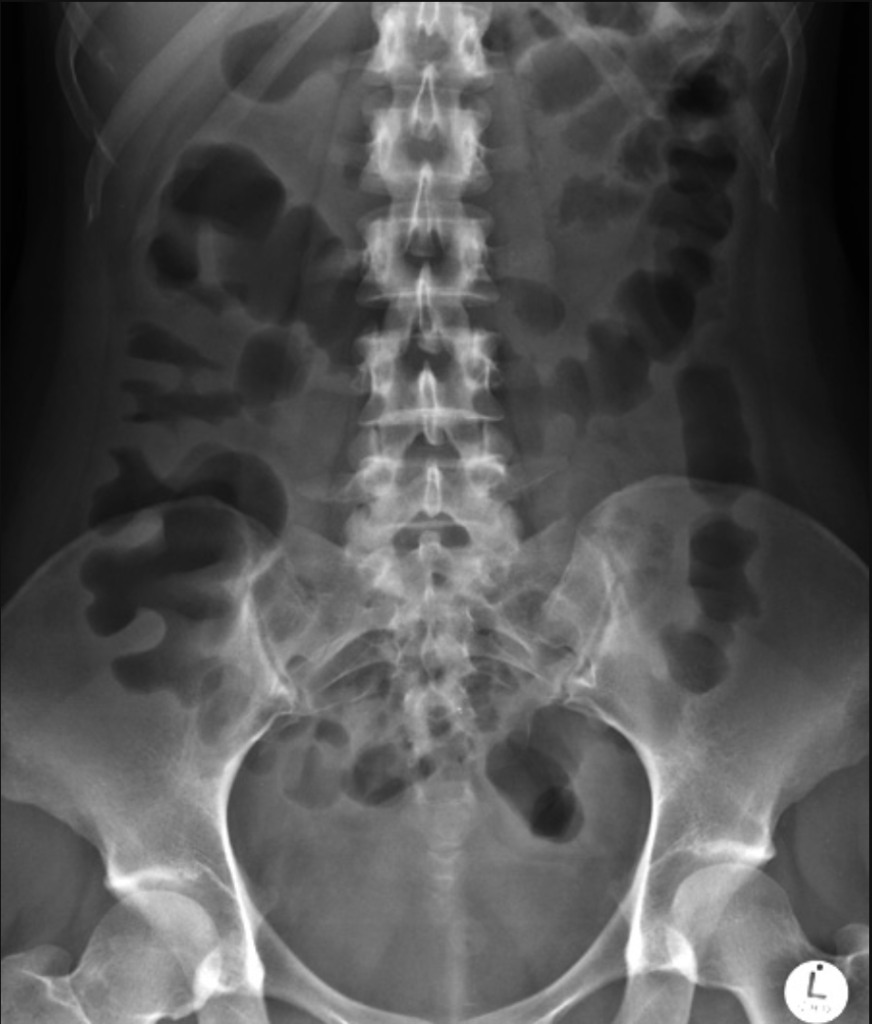
所見:「潰瘍性腸炎の症例であるが、このような母趾圧痕像が認められる場合がある。」
核医学検査所見
核医学検査は、HUSによる腎機能障害の程度を定量的に評価するのに有用で、治療効果の判定にも活用されています。
99mTc-DTPA(ジエチレントリアミン五酢酸)シンチグラフィでは、糸球体濾過率(GFR、腎臓の濾過機能を示す指標)の低下が確認されます。
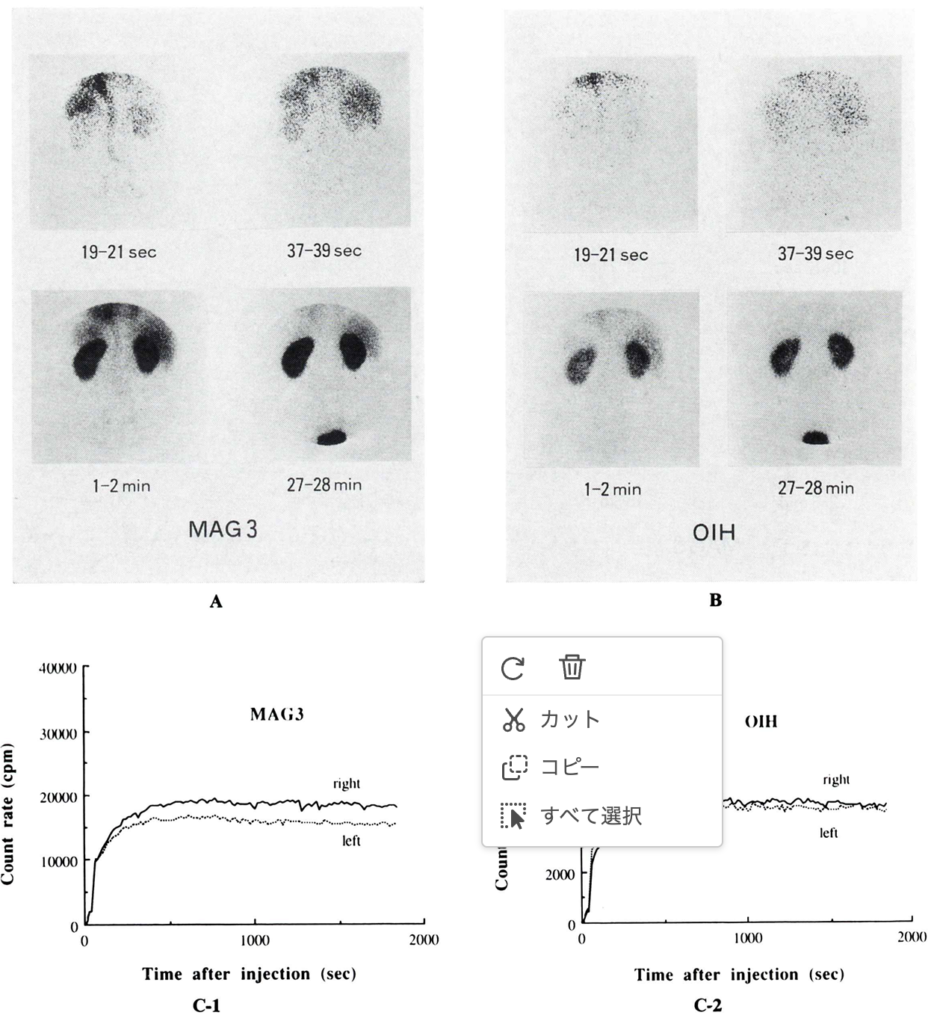
99mTc-MAG3(メルカプトアセチルトリグリシン)シンチグラフィでは、腎血流の低下や排泄遅延が観察され、腎臓の血流動態と排泄機能を評価できます。
これらの検査は、腎機能の回復過程を経時的に評価する際にも有用で、治療方針の決定や予後予測に貢献します。
| 核医学検査 | 評価項目 |
| 99mTc-DTPA | GFR |
| 99mTc-MAG3 | 腎血流・排泄 |
血管造影所見
血管造影は侵襲的な検査のため、HUSの一般的な診断には用いられませんが、特殊な状況下で実施されることがあります。
腎動脈造影では、小葉間動脈や弓状動脈の狭小化や閉塞、皮質の造影不良などが特徴的な所見として認められます。
また、腸間膜動脈造影では、腸管壁の血流低下や血管の攣縮が観察されることがあり、腸管虚血の評価に役立ちます。
- 血管造影で観察される所見
- 腎小葉間動脈・弓状動脈の狭小化・閉塞
- 腎皮質の造影不良
- 腸間膜動脈の血流低下
- 血管の攣縮
HUSの画像所見は、疾患の進行度や個々の患者の状態によって変化するため、単一の画像検査だけでなく、複数のモダリティを組み合わせて総合的に評価することが大切です。

HUSの治療戦略と回復への道筋
溶血性尿毒症症候群(HUS)は、迅速かつ的確な治療介入を要する重篤な疾患です。
本稿では、HUSに対する主要な治療アプローチ、使用される薬剤、そして回復までの過程について詳細に解説いたします。
支持療法:全身状態の安定化
HUSの治療において、支持療法は基盤となる極めて重要な役割を担います。
水分バランスの綿密な管理、電解質レベルの細やかな調整、そして血圧の厳密なコントロールなどが含まれ、患者様の全身状態の安定化を図ります。
重症例では、人工透析や血漿交換療法といった高度な医療介入が必要となる場合もあります。
| 支持療法 | 主たる目的 |
| 水分管理 | 循環動態の最適化 |
| 電解質補正 | 代謝バランスの維持 |
| 血圧管理 | 臓器灌流の確保 |
薬物療法:病態の制御と改善
HUSの治療には、様々な薬剤が使用され、病態の制御と改善を目指します。
抗菌薬は、原因となる細菌感染の制御に用いられますが、使用のタイミングや薬剤の選択には細心の注意を払います。
補体阻害薬であるエクリズマブは、非典型HUSの治療に顕著な効果を示し、腎機能の改善や血小板数の回復を促進します。
2019年に発表された大規模臨床試験では、エクリズマブによる治療を受けた非典型HUS患者の約70%で完全寛解が達成されたという画期的な結果が報告されています。
- HUS治療に用いられる主要な薬剤
- 抗菌薬(感染源の制御と抑制)
- エクリズマブ(補体系の過剰活性化を抑制)
- 降圧薬(血圧の適正管理)
- 利尿薬(体内水分バランスの調整)
血液浄化療法:体内環境の改善
重症のHUS患者では、血液浄化療法が不可欠となることがあります。
血液透析は、腎機能が著しく低下した際に、老廃物の除去や電解質バランスの調整を行い、体内環境の正常化を図ります。
血漿交換療法は、血漿中の有害物質を除去し、新鮮な血漿成分を補充することで、病態の改善を促進します。
| 血液浄化法 | 主たる目的 |
| 血液透析 | 老廃物除去と電解質調整 |
| 血漿交換 | 有害物質除去と血漿成分補充 |
栄養管理:回復を支える基盤
HUS患者の回復には、適切な栄養管理が欠かせず、治療の重要な柱の一つとなります。
急性期には、経静脈栄養が中心となりますが、回復期に入ると、経腸栄養や経口摂取へと段階的に移行し、患者様の状態に応じて栄養摂取方法を最適化します。
たんぱく質や電解質の摂取量は、患者様の状態に応じて慎重に調整され、栄養状態の改善と臓器機能の回復を支援します。
リハビリテーション:機能回復への道筋
HUSからの回復期には、リハビリテーションが重要な役割を果たし、患者様の生活の質の向上に寄与します。
長期入院による筋力低下や運動機能の低下を防ぐため、早期からのリハビリテーション介入が推奨され、患者様の状態に応じて段階的に進めていきます。
理学療法や作業療法を通じて、日常生活動作の改善や身体機能の回復を目指し、患者様の自立と社会復帰をサポートします。
| リハビリ種類 | 主たる目的 |
| 理学療法 | 運動機能の回復と向上 |
| 作業療法 | 日常生活動作の改善 |
治癒までの期間:個別性を考慮した回復過程
HUSの治癒までの期間は、患者様の状態や治療への反応によって大きく異なり、個別性の高い回復過程をたどります。
典型的なHUSでは、適切な治療により、多くの患者様が2〜3週間程度で急性期を脱します。
しかし、完全な回復には数ヶ月を要することもあり、特に腎機能の回復には比較的長い時間を要する場合があります。
非典型HUSでは、より長期の治療が必要となり、場合によっては生涯にわたる治療継続を要することもあります。
- HUSからの回復に影響を与える要因
- 発症時の重症度と臓器障害の程度
- 治療開始のタイミングと初期対応の適切さ
- 患者様の年齢や基礎疾患の有無
- HUSのタイプ(典型的か非典型的か)と遺伝的背景
HUSの治療は、個々の患者様の状態に応じて細やかに調整され、オーダーメイドの医療アプローチが求められます。

治療の副作用やデメリット(リスク)
抗菌薬使用に伴うリスク
HUS治療で使用される抗菌薬には、いくつかの潜在的なリスクが存在し、患者様の健康に影響を与える場合があります。
一部の抗菌薬は、腸内細菌叢(腸内の微生物のバランス)を乱し、下痢や腹痛などの消化器症状を引き起こします。
また、長期にわたる抗菌薬の使用は、耐性菌(抗菌薬が効きにくい細菌)の出現リスクを高める可能性があり、将来の感染症治療を困難にする恐れがあります。
稀ではありますが、重度のアレルギー反応や肝機能障害などの深刻な副作用が生じる場合もあり、慎重なモニタリングが求められます。
| 抗菌薬関連リスク | 発生頻度 |
| 消化器症状 | 比較的高い |
| 耐性菌出現 | 中程度 |
| 重度アレルギー | 稀 |
血漿交換療法のデメリット
血漿交換療法は効果的な治療法ですが、いくつかのデメリットを伴い、患者様に負担をかける場合があります。
この治療法は侵襲的であり、中心静脈カテーテル(太い血管に挿入する管)の挿入が必要となるため、感染症のリスクが増加します。
また、血漿交換中に血圧低下やアレルギー反応が起こる可能性があり、患者様の体調に急激な変化をもたらすことがあります。
長期的には、免疫グロブリン(体を守る抗体タンパク質)などの重要なタンパク質が過度に除去されるリスクもあり、免疫機能の低下につながる恐れがあります。
- 血漿交換療法の主なリスク
- 感染症(カテーテル関連)
- 血圧変動(特に低下)
- アレルギー反応(新鮮凍結血漿に対して)
- 重要タンパク質の過剰除去(免疫機能への影響)
補体阻害薬の副作用
補体阻害薬(エクリズマブなど)は、非典型HUSの治療に有効ですが、重大な副作用のリスクがあり、患者様の生活に影響を与える可能性があります。
最も懸念されるのは、髄膜炎菌感染のリスク増加です。
このため、補体阻害薬の使用前にはワクチン接種が必要となりますが、完全な予防は困難であり、患者様は常に感染のリスクに注意を払う必要があります。
また、頭痛や悪心、筋肉痛などの一般的な副作用も報告されており、日常生活の質に影響を及ぼす可能性があります。
| 補体阻害薬の副作用 | 重症度 |
| 髄膜炎菌感染 | 重度 |
| 頭痛 | 軽度〜中等度 |
| 悪心 | 軽度 |
腎代替療法のリスク
重症HUS患者に対して行われる腎代替療法(透析など)にも、いくつかのリスクが伴い、患者様の身体に大きな負担をかける可能性があります。
血液透析では、カテーテル関連感染症や血栓形成(血液の固まり)のリスクが増加し、患者様の健康状態を脅かす恐れがあります。
また、透析中の血圧低下や不整脈などの循環器系合併症が生じる可能性があり、患者様に不快感や危険をもたらすことがあります。
長期的には、透析アミロイドーシス(透析に伴うタンパク質沈着症)などの合併症リスクも考慮する必要があり、患者様のQOL(生活の質)に影響を与える可能性があります。
ステロイド療法の副作用
一部のHUS患者に使用されるステロイド療法には、多くの潜在的な副作用があり、患者様の全身に様々な影響を及ぼす可能性があります。
短期的には、高血糖や消化性潰瘍、精神症状などが生じる可能性があり、患者様の日常生活に支障をきたすことがあります。
長期使用では、骨粗鬆症や白内障、易感染性などのリスクが増加し、患者様の健康状態に長期的な影響を与える恐れがあります。
また、ステロイドの急激な中止は副腎不全を引き起こす可能性があるため、慎重な減量が必要となり、患者様には長期にわたる注意深い管理が求められます。
| ステロイド副作用 | 発現時期 |
| 高血糖 | 短期 |
| 骨粗鬆症 | 長期 |
| 易感染性 | 短期〜長期 |
免疫抑制療法のデメリット
重症または再発性HUSの患者に対して行われる免疫抑制療法には、重大なリスクが伴い、患者様の健康に深刻な影響を及ぼす可能性があります。
免疫機能の低下により、重篤な感染症のリスクが大幅に増加し、患者様は日常生活において特別な注意を払う必要があります。
また、一部の免疫抑制剤では、悪性腫瘍の発生リスクが上昇する可能性が報告されており、長期的な健康への影響が懸念されます。
さらに、肝機能障害や腎機能障害などの臓器毒性も懸念され、患者様の全身状態に影響を与える可能性があります。
- 免疫抑制療法の主なリスク
- 重症感染症(細菌、ウイルス、真菌など)
- 悪性腫瘍(特にリンパ増殖性疾患)
- 臓器毒性(肝臓、腎臓への影響)
- 骨髄抑制(血球製造の低下)
HUSの治療に関連する副作用やリスクは、患者様の状態や使用する薬剤によって大きく異なります。

HUSの治療費
処方薬の薬価
HUS治療に使用される薬剤の中には、高額なものが含まれており、患者様の経済的負担が大きくなる可能性があります。
特に、補体阻害薬であるエクリズマブ(HUSの治療に用いられる特殊な薬剤)は、1回の投与で薬剤費だけで615,752円であり、患者様やそのご家族に大きな経済的インパクトを与えかねません。
抗菌薬や免疫抑制剤などの他の薬剤も、使用量や投与期間によって費用が大きく変動するため、治療計画に応じて事前に費用の見積もりを行うことが望ましいでしょう。
1か月の治療費
HUSの治療費は、症状の重症度や必要とされる医療処置によって大きく異なり、患者様ごとに個別の見積もりが必要となります。
血液透析(体内の老廃物を人工的に除去する治療法)や血漿交換療法(血液中の異常な成分を除去し、正常な成分と置換する治療法)などの特殊治療を要する際は、さらに高額になることが予想されます。
- 1か月の治療費の目安(あくまで参考値であり、実際の費用は大きく異なる場合があります)
- 軽症例:50万円〜100万円(外来治療中心の場合)
- 中等症例:100万円〜300万円(短期入院を含む場合)
- 重症例:300万円以上(長期入院や特殊治療を要する場合)
治療が長期に渡った場合の治療費
HUSの治療期間は患者様の状態や治療への反応によって大きく異なりますが、長期化すると総額で数千万円に達する事例も報告されています。
非典型HUS(遺伝的要因や自己免疫疾患が関与するHUSの一型)では、生涯にわたる治療が必要となることもあり、継続的な経済的負担を考慮に入れた長期的な財政計画を立てることが重要です。
| 治療期間 | 想定される総額(参考値) |
| 3ヶ月 | 300万円〜1000万円 |
| 6ヶ月 | 600万円〜2000万円 |
| 1年以上 | 1000万円〜5000万円 |
これらの費用は、あくまで概算であり、実際の治療費は患者様の状態や治療内容、医療機関によって大きく変動する点にご留意ください。
また、高額医療制度などの医療費削減を図ることで大幅に支払いを減らすことが出来ます。
なお、上記の価格は2024年10月時点のものであり、最新の価格については随時ご確認ください。
以上

- 参考にした論文




