内分泌疾患の一種であるSIADH(バソプレシン分泌過剰症)とは、体内の水分バランスを調整する重要なホルモンであるバソプレシン(抗利尿ホルモン)が過剰に分泌される状態を指します。
この病気ではバソプレシンの過剰分泌によって体内に必要以上の水分が蓄積されてしまいます。
その結果、血液中のナトリウム濃度が低下して低ナトリウム血症と呼ばれる状態が引き起こされるのです。
SIADHは様々な原因で発症する可能性がありますが、多くの場合は他の疾患に伴って二次的に発症することが知られています。
患者さんの症状や重症度は個人差が大きく、軽度の場合は無症状のこともありますが、重症化すると深刻な合併症を引き起こす危険性もあるのです。
主症状と臨床的特徴
SIADH(バソプレシン分泌過剰症)の主症状は体内の水分バランスの乱れに起因する多様な症状群として現れます。
この疾患ではバソプレシンの過剰分泌により体内に水分が貯留し、血清ナトリウム濃度の低下(低ナトリウム血症)が引き起こされます。
症状の程度は低ナトリウム血症の進行度や発症の急性度によって大きく異なり、無症状から生命を脅かす重篤な状態まで幅広い臨床像を呈するでしょう。
患者さんの多くは初期段階では特異的な症状を自覚しないことがあるため、定期的な健康診断や血液検査で偶然発見されることもあるのです。
初期症状と軽度の症状
SIADHの初期段階や軽度の場合は症状が非特異的であったり、まったく症状が現れないこともあります。
しかし、以下のような軽度の症状が現れることがあるのです。
- 倦怠感
- 食欲不振
- 頭痛
- 吐き気
これらの症状は日常生活での些細な変化として感じられることがあり、患者さん自身が気づきにくいことも多いでしょう。
| 初期症状 | 特徴 |
| 倦怠感 | 全身のだるさ |
| 頭痛 | 軽度から中等度 |
中等度の症状
低ナトリウム血症が進行すると、より顕著な症状が現れる可能性があります。
中等度の症状には以下のようなものがあります。
- 筋力低下
- 易刺激性
- 気分の変化
- 集中力の低下
- 記憶障害
これらの症状は患者様の日常生活に支障をきたすレベルまで進行することがあります。
| 中等度症状 | 日常生活への影響 |
| 筋力低下 | 歩行困難 |
| 集中力低下 | 作業効率の低下 |
重度の症状
重度の低ナトリウム血症では神経系統に深刻な影響を及ぼす可能性があります。
重度のSIADHでは以下のような危険な症状が現れることがあるでしょう。
- 錯乱
- けいれん発作
- 意識障害
- 昏睡
これらの症状は緊急の医療介入を必要とし、生命を脅かす危険性も否めません。
症状の進行と変動
SIADHの症状は低ナトリウム血症の進行速度によって異なる経過をたどることがあります。
急性の低ナトリウム血症では症状が急速に悪化するケースも生じます。
一方、慢性的に進行した場合は体が徐々に適応するため、重度の低ナトリウム血症でも比較的軽度の症状にとどまることも多いです。
| 進行速度 | 症状の特徴 |
| 急性 | 急速な悪化 |
| 慢性 | 緩徐な進行 |
年齢による症状の違い
SIADHの症状は患者様の年齢によって異なる現れ方をすることがあります。
高齢者では以下のような特徴が見られることがあります。
- 転倒リスクの増加
- 認知機能の低下
- せん妄
一方、若年者では以下のような症状が目立つでしょう。
- 頭痛
- 吐き気
- 筋肉のけいれん

原因とメカニズム
SIADH(バソプレシン分泌過剰症)は体内のバソプレシン(抗利尿ホルモン)が過剰に分泌されることで引き起こされる複雑な内分泌疾患です。
この状態は様々な要因によって引き起こされる可能性があり、その原因は多岐にわたります。
原因は大きく分けて中枢神経系の障害、肺疾患、悪性腫瘍、薬剤性、その他の要因に分類されますが、時に明確な原因が特定できない特発性のケースも存在します。
中枢神経系の障害によるSIADH
中枢神経系の障害はSIADHの主要な原因の一つです。
この分野では以下のような要因がSIADHを引き起こす可能性があります。
- 脳腫瘍
- 脳出血
- 髄膜炎
- 脳炎
これらの状態ではバソプレシンの産生や分泌を制御する脳の領域が直接的または間接的に影響を受けることがあります。
| 中枢神経系の障害 | SIADHとの関連性 |
| 脳腫瘍 | 高 |
| 脳出血 | 中〜高 |
| 髄膜炎 | 中 |
肺疾患とSIADH
肺疾患もSIADHの重要な原因となることがあります。以下はSIADHが原因で起こりうる主な肺疾患関連です。
- 肺炎
- 肺結核
- 慢性閉塞性肺疾患(COPD)
- 急性呼吸窮迫症候群(ARDS)
これらの疾患では肺組織の炎症や低酸素状態がバソプレシンの過剰分泌を誘発する可能性があります。
悪性腫瘍とSIADH
悪性腫瘍もSIADHの重要な原因の一つとされ、特に以下のような腫瘍でSIADHが発症するリスクが高いとされています。
| 悪性腫瘍 | SIADHの発症リスク |
| 小細胞肺癌 | 非常に高い |
| 頭頸部癌 | 高い |
| 膵臓癌 | 中程度 |
これらの腫瘍では腫瘍細胞自体がバソプレシンを産生したり、腫瘍による間接的な影響でバソプレシン分泌が促進されたりすることがあるでしょう。
薬剤性SIADH
多くの薬剤がSIADHを引き起こす可能性があります。以下は主なSIADH関連薬剤です。
- 抗うつ薬(特に選択的セロトニン再取り込み阻害薬:SSRI)
- 抗てんかん薬
- 抗癌剤
- 利尿薬(特にチアジド系)
これらの薬剤は直接的にバソプレシンの分泌を促進したり、腎臓でのバソプレシンの作用を増強したりすることがあります。
その他のSIADH原因
上記の主要な原因カテゴリー以外にもSIADHを引き起こす可能性のある要因があります。
これらには以下のようなものが含まれます。
- 遺伝性SIADH
- 運動誘発性SIADH
- 痛み
- ストレス
これらの要因はバソプレシン分泌に影響を与える複雑な生理学的メカニズムを通じてSIADHを引き起こす可能性が考えられます。
| その他の要因 | 特徴 |
| 遺伝性SIADH | 稀だが家族性に発症 |
| 運動誘発性 | マラソンなどの長時間運動後 |
SIADHの原因は多岐にわたり、時に複数の要因が組み合わさって発症することもあります。

SIADHの診察と診断プロセス
SIADH(バソプレシン分泌過剰症)の診断は詳細な病歴聴取と身体診察から始まり、一連の検査を経て総合的に行われます。
この過程では低ナトリウム血症の存在を確認し、他の低ナトリウム血症の原因を除外することが重要です。
診断には血液検査や尿検査が不可欠であり、時には画像診断や特殊検査が追加されることもあるでしょう。
SIADHの診断基準を満たすかどうかを慎重に評価し、原因となる基礎疾患の特定も並行して行われます。
これらの診断プロセスを通じて患者さんの状態を正確に把握し、最適な管理方針を決定することが可能となります。
初診時の問診と身体診察
SIADHの診断において詳細な問診は極めて重要で、特に以下のような点について丁寧に聴取します。
| 問診項目 | 着目点 |
| 症状 | 発症時期、経過 |
| 既往歴 | 中枢神経系疾患や肺疾患の有無 |
| 薬剤歴 | SIADH誘発薬の使用 |
| 手術歴 | 術後の変化 |
身体診察では液量の評価や神経学的異常の有無を確認します。
血液検査と尿検査
SIADHの診断には血液検査と尿検査が不可欠で、以下は主な検査項目です。
- 血清ナトリウム濃度
- 血漿浸透圧
- 尿中ナトリウム濃度
- 尿浸透圧
これらの検査結果を総合的に評価してSIADHの可能性を判断します。
特に低ナトリウム血症と血漿浸透圧の低下、尿浸透圧の相対的な上昇がSIADHを示唆する重要な所見です。
| 検査項目 | SIADHでの典型的な値 |
| 血清Na | 135 mEq/L未満 |
| 血漿浸透圧 | 275 mOsm/kg未満 |
SIADH診断基準の評価
SIADHの診断には特定の診断基準を満たすことが求められます。主な診断基準には以下のようなものがあります。
- 血清ナトリウム濃度の低下(135 mEq/L未満)
- 血漿浸透圧の低下(275 mOsm/kg未満)
- 尿中ナトリウム濃度の上昇(40 mEq/L超)
- 尿浸透圧の相対的な上昇(血漿浸透圧より高値)
- 正常な副腎機能と甲状腺機能
- 利尿薬非使用
これらの基準を慎重に評価し、他の低ナトリウム血症の原因を除外することでSIADHの診断が確定します。
鑑別診断
SIADHの診断では他の低ナトリウム血症を引き起こす疾患との鑑別が重要です。
主な鑑別疾患には以下のようなものがあります。
- 副腎不全
- 甲状腺機能低下症
- 心不全
- 肝硬変
これらの疾患を除外するために、追加の内分泌機能検査や画像診断が必要となる場合もあるでしょう。
| 鑑別疾患 | 鑑別のポイント |
| 副腎不全 | 血中コルチゾール |
| 甲状腺機能低下症 | TSH, fT4 |
画像診断と特殊検査
SIADHの原因特定のために画像診断が行われることがあります。以下は主な画像検査です。
- 胸部X線検査
- 頭部MRI/CT
- 腹部CT
また、特殊な状況下では以下のような特殊検査が考慮されることもあります。
- バソプレシン負荷試験
- 制限試験
これらの検査はSIADHの確定診断や原因疾患の特定に役立つケースも見られるでしょう。

SIADHの画像所見と診断的意義
SIADH(バソプレシン分泌過剰症)の画像診断は主に原因疾患の特定や合併症の評価を目的として行われます。
この疾患自体に特異的な画像所見はありませんが、様々な画像検査が診断過程で重要な役割を果たすのです。
胸部X線、頭部MRI/CT、腹部CTなどの画像検査により、SIADHの背景にある病態や二次的な影響を評価することができます。
画像所見の適切な解釈は、SIADHの原因特定や治療方針の決定において極めて重要です。
これらの画像検査を通じて得られる情報は、患者さんの総合的な評価と長期的な管理計画の立案に不可欠な要素となります。
胸部X線検査の所見
胸部X線検査はSIADHの原因となりうる肺疾患や悪性腫瘍の評価に用いられます。
主な着目点には以下のようなものがあります。
- 肺炎像
- 肺結核の痕跡
- 肺癌(特に小細胞肺癌)の存在
また、体内の水分貯留状態を反映する所見として、以下のような点にも注意が払われます。
- 肺うっ血像
- 胸水貯留
| 胸部X線所見 | 関連する病態 |
| 浸潤影 | 肺炎 |
| 結節影 | 肺癌 |

所見:進行性の体重減少を呈した57歳男性の小細胞肺癌(SCLC)。(a) 後前胸部X線写真では、右側傍気管線の著しい肥厚が見られ(矢印)、縦隔リンパ節腫大または縦隔腫瘤を示唆している所見である。(b) 限定された造影CT画像では、右側縦隔に軟部組織腫瘤が示されている。CTでは肺病変は認められなかった。気管支鏡下生検によりSCLCが明らかになった。この病変は、原発性肺腫瘍の有無にかかわらず、縦隔腫瘤または縦隔リンパ節腫大として現れることがある。
頭部MRI/CTの所見
頭部MRI/CTは、SIADHの原因となる中枢神経系の異常を評価するために重要です。
主な着目点には以下のようなものがあります。
- 脳腫瘍
- 脳出血
- 髄膜炎/脳炎の所見
特に以下のような領域の異常所見は注意深く評価されます。
- 視床下部
- 下垂体
これらの領域の異常はバソプレシン分泌調節機構の障害を示唆する可能性があります。
| 頭部画像所見 | 評価対象 |
| 造影効果 | 腫瘍、炎症 |
| 出血像 | 脳出血 |
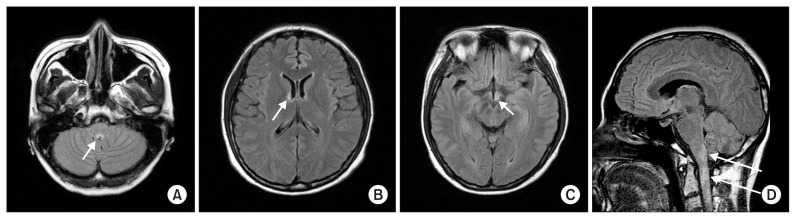
所見:SIADHの症例。(A) T2 FLAIR画像では延髄下部に焦点性の高信号域が認められる(矢印)。(B, C) T2高信号病変が視床下部および疑わしい左視交叉を巻き込んでいる(矢印)。(D) 矢状断T2強調画像では、頸髄上部に多発するT2高信号病変が示されている(矢印)。
腹部CTの所見
腹部CTはSIADHの原因となりうる腹部臓器の異常を評価するために用いられ、特に以下のような点にな着目します。
- 膵臓癌
- 副腎腫瘍
- その他の腹部悪性腫瘍
また、SIADHに伴う体液貯留の評価として、以下のような所見にも注意を払わなければなりません。
- 腹水貯留
- 臓器浮腫

所見:SIADHと低ナトリウム血症を呈した48歳の女性が発作を訴えて来院。(A) 初回診察時の脳の軸方向造影CT(CECT)画像では、側脳室の狭窄および溝の消失(矢印)により軽度の脳浮腫が認められる。血清ナトリウムレベルは120 mEq/L未満であった。(B) 低ナトリウム血症を1時間あたりナトリウム濃度0.5 mmol/Lの速度でゆっくりと是正した後の脳の軸方向CECT画像では、浮腫の解消が示されている。(C) 胸部の軸方向CECT画像では、左下葉に生検結果でSCLC(小細胞肺癌)と確認された棘状の腫瘤(矢印)が示されている。(D) 腹部の軸方向CECT画像では、数多くの肝転移病変(矢頭)および両側副腎転移が示されている。著しい腸間膜リンパ節腫大(黒矢印)および腹膜癌症(白矢印)も認められる。
全身PET-CTの役割
全身PET-CTはSIADHの原因となる悪性腫瘍の検索に有用です。この検査では以下のような点が評価されます。
- 原発巣の同定
- 転移巣の検索
- 炎症性病変の評価
PET-CTは特に原因不明のSIADHケースにおいて潜在的な悪性腫瘍の発見に役立つことがあるのです。
| PET-CT所見 | 意義 |
| 局所的高集積 | 腫瘍疑い |
| 多発性集積 | 転移疑い |
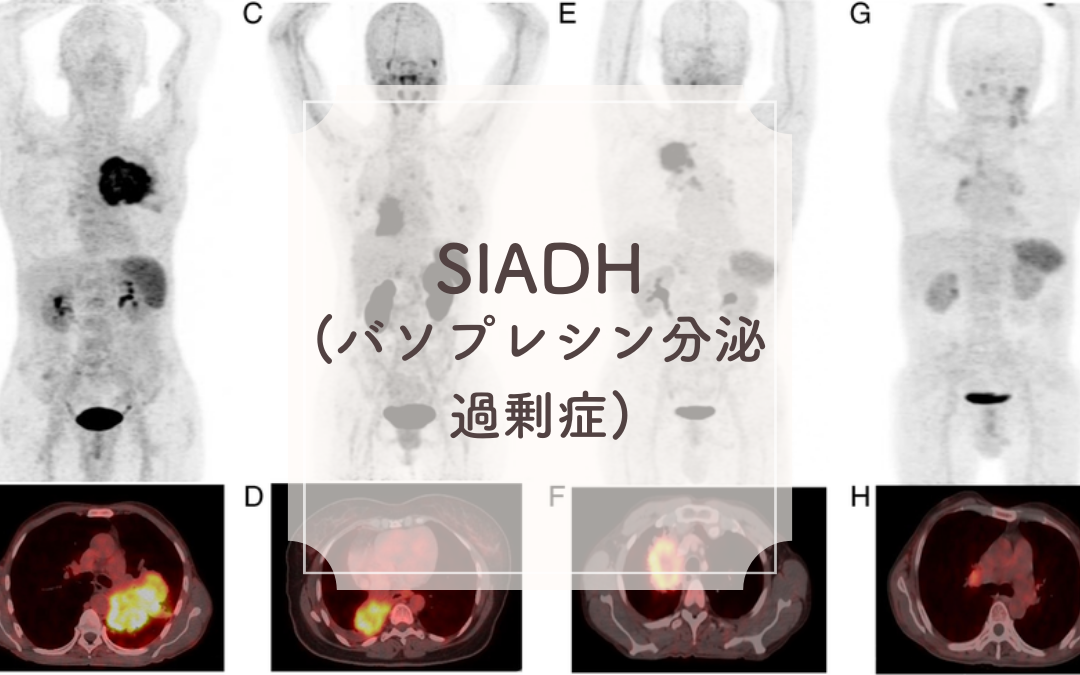
![[⁶⁸Ga]Ga-Pentixafor MIP and axial-fused PET/CT images in one patient each of SCLC (A, B) with SUVmax = 13.2, NSCLC adenocarcinoma (C, D) with SUVmax = 12.2, NSCLC squamous (E, F) with SUVmax = 7.2, and lung NET (G, H) with SUVmax = 5.2 respectively](https://www.researchgate.net/publication/366155578/figure/fig1/AS:11431281120650910@1676602219310/GaGa-Pentixafor-MIP-and-axial-fused-PET-CT-images-in-one-patient-each-of-SCLC-A-B.png)
所見:[⁶⁸Ga]Ga-Pentixafor MIPおよびフュージョンPET/CT画像が、それぞれ以下の患者で示されています。(A, B) 小細胞肺癌(SCLC)で、SUVmax = 13.2。(C, D) 非小細胞肺癌(NSCLC)腺癌で、SUVmax = 12.2。(E, F) 非小細胞肺癌(NSCLC)扁平上皮癌で、SUVmax = 7.2。(G, H) 肺神経内分泌腫瘍(NET)で、SUVmax = 5.2。
低ナトリウム血症に伴う二次的画像所見
重度の低ナトリウム血症が持続する場合、二次的な臓器障害を示唆する画像所見が現れることがあります。
特に以下のような所見に注意が必要です。
- 脳浮腫
- 浸透圧性脱髄症候群(橋中心髄鞘崩壊症)
これらの所見はSIADHの重症度や治療の緊急性を判断する上で重要な情報となります。
これらの画像検査を通じてSIADHの背景にある病態を明らかにし、適切な治療方針の決定につなげることが大切です。
また、低ナトリウム血症に伴う二次的な臓器障害の評価も画像診断の重要な役割の一つです。
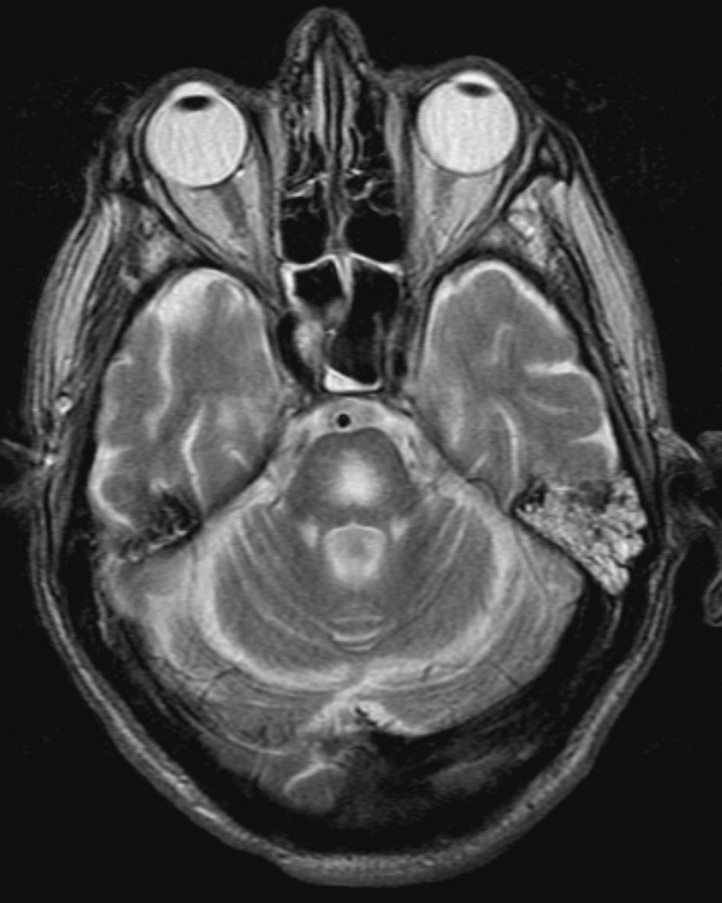
所見:T2WI高信号域が橋に認められ、周辺部は正常である。脳萎縮が見られ、特に小脳で顕著である。信号異常が正中線を越えていることに注目する必要があり、これは橋の穿通枝動脈が終末動脈であり、正中線を越えないため、虚血の可能性が低いことを示唆している。

SIADHの治療アプローチと経過
SIADH(バソプレシン分泌過剰症)の治療は低ナトリウム血症の是正と原因疾患への対応を中心に進められます。
治療方法は症状の重症度や発症の急性度によって異なり、水分制限、薬物療法、そして時に高張食塩水の投与などを組み合わせるのが一般的です。
使用される薬剤にはバソプレシン受容体拮抗薬や利尿薬などがあり、患者さんの状態に応じて選択されるでしょう。
治療期間は原因や重症度によって大きく異なり、数日から数週間、時には数ヶ月以上に及ぶこともあります。
SIADHの管理は長期的な視点が重要であり、原因疾患の治療と並行して慎重に進められます。
水分制限療法
水分制限はSIADHの基本的な治療法の一つです。
この方法では患者様の1日の水分摂取量を制限することで体内の水分過剰状態を改善します。
水分制限の程度は以下のような要因に基づいて決定されるでしょう。
- 低ナトリウム血症の重症度
- 尿量
- 体重
通常1日の水分摂取量を800-1000ml程度に制限することが多いですが、個々の患者さんの状態に応じて調整されます。
| 水分制限レベル | 1日の摂取量 |
| 軽度 | 1000-1200ml |
| 中等度 | 800-1000ml |
| 重度 | 600-800ml |
薬物療法
SIADHの薬物療法には様々な選択肢がありますが、主な薬剤には以下のようなものになります。
- バソプレシン受容体拮抗薬(トルバプタンなど)
- 利尿薬(フロセミドなど)
- 尿素
バソプレシン受容体拮抗薬は腎臓でのバソプレシンの作用を阻害し、水利尿を促進します。
利尿薬は尿量を増加させることで体内の水分量を減少させます。尿素は浸透圧利尿を引き起こし、水分排泄を促進する効果が期待できるのです。
| 薬剤 | 主な作用機序 |
| トルバプタン | バソプレシン受容体阻害 |
| フロセミド | Na再吸収阻害 |
高張食塩水療法
重症の低ナトリウム血症や急性発症のケースでは、高張食塩水の投与が考慮されます。
この治療法は以下のような状況で用いられることがあります。
- 意識障害がある場合
- けいれん発作がみられる場合
- 急速な血清ナトリウム値の低下がある場合
高張食塩水の投与は慎重な監視下で行われ、血清ナトリウム値の補正速度には細心の注意が払われなければなりません。
原因疾患の治療
SIADHの根本的な治療には原因となっている基礎疾患への対応が不可欠です。原因疾患の種類によって治療アプローチは大きく異なります。
例えば以下のような対応が考えられます。
- 悪性腫瘍の場合 抗癌治療
- 薬剤性の場合 原因薬剤の中止や変更
- 中枢神経系疾患の場合 それぞれの疾患に応じた治療
原因疾患の治療が成功すればSIADHも改善する可能性が高くなります。
| 原因疾患 | 治療アプローチ |
| 肺小細胞癌 | 化学療法、放射線療法 |
| 薬剤性 | 原因薬剤の中止 |
治療効果の評価と経過観察
SIADHの治療効果は主に以下のような指標で評価されます。
- 血清ナトリウム値の改善
- 尿量の変化
- 臨床症状の改善
治療開始後これらの指標を定期的にモニタリングし、必要に応じて治療内容を調整します。
経過観察の頻度は患者さんの状態や治療方法によって異なりますが、特に治療初期は頻回な評価が必要でしょう。
治療期間は原因や重症度によって大きく異なり、数日から数ヶ月以上に及ぶことがあります。
完全な「治癒」という概念よりも長期的な管理が重要となる疾患であり、定期的な経過観察と適切な治療調整が不可欠です。
原因疾患の治療が成功すればSIADHも改善する可能性が高くなりますが、一部のケースでは長期的な管理が必要となることもあります。

治療の副作用とリスク
SIADH(バソプレシン分泌過剰症)の治療は患者さんの生活の質を大きく改善する一方で、いくつかの副作用やリスクを伴う可能性があります。
これらのリスクは用いられる治療法や薬剤によって異なり、また患者さんの個別の状況によっても変化します。
主な副作用には急速な血清ナトリウム値の補正に伴う浸透圧性脱髄症候群、水分制限による脱水、薬物療法に伴う電解質異常などがあります。
また、長期的な治療に伴うリスクや原因疾患の治療に関連する副作用についても考慮することが必要がです。
これらの副作用やリスクを理解し、適切に管理することで、より安全で効果的な治療が期待できるでしょう。
急速な血清ナトリウム値補正のリスク
SIADHの治療において最も注意すべき副作用の一つが急速な血清ナトリウム値の補正に伴う浸透圧性脱髄症候群です。
この合併症は以下のような状況で発生するリスクが高まります。
- 24時間以内に血清ナトリウム値が12mEq/L以上上昇した場合
- 48時間以内に18mEq/L以上上昇した場合
浸透圧性脱髄症候群の症状には以下のようなものがあります。
- 構音障害
- 嚥下障害
- 四肢の麻痺
- 意識障害
| 補正速度 | リスク |
| 12mEq/L/日以上 | 高 |
| 8-12mEq/L/日 | 中 |
| 8mEq/L/日未満 | 低 |
水分制限療法の副作用
水分制限療法はSIADHの基本的な治療法ですが、いくつかの副作用を伴う可能性があります。
主な副作用には以下のようなものがあります。
- 脱水
- 口渇感
- 便秘
- 皮膚乾燥
特に高齢者や基礎疾患を持つ患者様では脱水のリスクに注意が必要です。
また、厳格な水分制限は患者様のQOLを低下させる可能性があるため個々の状況に応じた柔軟な対応が求められます。
| 副作用 | 対策 |
| 脱水 | 定期的な体重測定 |
| 口渇感 | 氷片の使用 |
薬物療法の副作用
SIADHの薬物療法に用いられる薬剤にもいくつかの副作用があります。
バソプレシン受容体拮抗薬(トルバプタンなど)の主な副作用には以下のようなものが挙げられるでしょう。
- 口渇
- 多尿
- 肝機能障害
以下は利尿薬(フロセミドなど)の副作用です。
- 電解質異常(低カリウム血症など)
- 脱水
- 血圧低下
これらの副作用は定期的な血液検査や身体所見の評価によってモニタリングされます。
高張食塩水療法のリスク
重症例で用いられる高張食塩水療法には以下のような特有のリスクがあります。
中心静脈カテーテル挿入に伴う合併症(感染、血栓など)
急速な血清ナトリウム値の上昇 ・体液量過剰
高張食塩水療法は厳重な監視下で行われ、頻回な電解質測定が必要です。
| リスク | 対策 |
| 感染 | 無菌操作の徹底 |
| 急速な補正 | 頻回な電解質測定 |
長期治療に伴うリスク
SIADHの長期治療にはいくつかの潜在的なリスクがあり、特に以下のような点に注意が必要です。
- 骨密度低下
- 転倒リスクの増加
- 薬剤耐性の発現
これらのリスクは定期的な評価と必要に応じた予防策によって管理されます。
また、長期的な水分制限や薬物療法が患者さんの生活の質に与える影響についても考慮する必要があります。

再発リスクと予防策
SIADH(バソプレシン分泌過剰症)の再発リスクはその原因や患者様の個別の状況によって大きく異なります。
一部のケースでは完全に改善する一方で、再発や慢性化のリスクがある場合もあります。
再発を予防するためには原因疾患の管理、生活習慣の改善、定期的なフォローアップなど多面的なアプローチが必要です。
また、薬剤調整や水分摂取の管理も再発予防において重要な役割を果たします。
これらの予防策を適切に実施することで多くの患者さんが安定した状態を長期的に維持できる可能性が高まるでしょう。
原因別の再発リスク
SIADHの再発リスクはその原因によって大きく異なります。例えば以下のような傾向が見られます。
・悪性腫瘍が原因の場合 腫瘍の再発や進行に伴うリスクがある
・薬剤性の場合 原因薬剤の再投与で再発する可能性がある
・特発性の場合 再発リスクは比較的低いとされる
これらのリスクを考慮して個々の患者様に応じた予防策を講じることが重要です。
| 原因 | 再発リスク |
| 悪性腫瘍 | 中〜高 |
| 薬剤性 | 中 |
| 特発性 | 低〜中 |
生活習慣による再発予防
SIADHの再発予防には日常生活における注意点があります。特に以下のような生活習慣の管理が再発予防に役立つでしょう。
- 適切な水分摂取量の維持
- 塩分摂取量の管理
- アルコール摂取の制限
- 規則正しい生活リズムの維持
これらの習慣は体内の水分バランスを安定させ、再発リスクを低減するのに役立ちます。
特に水分摂取量の管理は極めて重要で、過剰摂取を避けつつ脱水にも注意する必要があります。
定期的なフォローアップの重要性
SIADHの再発や悪化を早期に発見し、予防するためには定期的なフォローアップが不可欠です。
フォローアップでは、以下のような項目がチェックされます。
- 血液検査(電解質、腎機能など)
- 尿検査
- 体重の変化
- 臨床症状の評価
これらの定期的な評価により、潜在的な問題を早期に発見して対策を講じることが可能です。
| フォローアップ項目 | 頻度 |
| 血液検査 | 1-3ヶ月ごと |
| 尿検査 | 3-6ヶ月ごと |
| 体重測定 | 毎日〜週1回 |
薬剤調整による再発予防
SIADHの管理に使用されている薬剤の適切な調整も再発予防に重要な役割を果たします。
特に以下のような点に注意が必要です。
- 定期的な薬剤効果の評価
- 副作用のモニタリング
- 必要に応じた用量調整
長期使用している薬剤の効果が低下したり、副作用が現れたりした場合には速やかな対応が大切になります。
ストレス管理と心理的サポート
ストレスはSIADHの症状を悪化させる可能性があるため効果的なストレス管理が再発予防に役立つことがあります。
以下のようなストレス管理法が有効かもしれません。
- リラクゼーション技法の習得
- 規則的な軽度の運動
- 十分な睡眠
また、患者会などのサポートグループに参加することで心理的なサポートを得られることが期待できます。
これらの活動は患者さんの全体的な健康状態を改善し、再発リスクを低減するのに役立つ可能性があります。

治療費について
SIADH(バソプレシン分泌過剰症)の治療費は、患者の状態や治療内容によって大きく異なります。長期的な管理が必要なため、総治療費は数十万円から数百万円に及ぶことも考えられるでしょう。
一般的に検査費用は血液検査で4,000円から13,000円、画像診断で14,500円から30,200円程度です。
入院が必要な場合は1日あたり30,000円から50,000円の費用がかかる可能性があります。
検査費用
血液検査や尿検査は定期的に必要です。
| 検査項目 | 費用 |
| 血液検査 | 4,000円から13,000円 |
| 尿検査 | 260円 |
薬剤費
使用する薬剤により費用が変わりますが、月額5,000円から20,000円ほどかかることがあります。
入院費用
重症度により入院期間が異なります。
詳しく説明すると、日本の入院費はDPC(診断群分類包括評価)システムを使用して計算されます。このシステムは、患者の病名や治療内容に基づいて入院費を決定する方法です。以前の「出来高」方式とは異なり、DPCシステムでは多くの診療行為が1日あたりの定額に含まれます。
DPCシステムの主な特徴
約1,400の診断群に分類される
1日あたりの定額制
一部の治療は従来通りの出来高計算が適用される
DPCシステムと出来高計算の比較表
DPC(1日あたりの定額に含まれる項目)出来高計算項目投薬手術注射リハビリ検査特定の処置画像診断入院基本料
DPCシステムの計算方法
計算式は以下の通りです:
「1日あたりの金額」×「入院日数」×「医療機関別係数」+「出来高計算分」
*医療機関別係数は各医療機関によって異なります。
例えば、患者が14日間入院した場合の計算は以下のようになります。
DPC名: 尿崩症
日数: 14
医療機関別係数: 0.0948 (例:神戸大学医学部附属病院)
入院費: ¥444,080 +出来高計算分
保険が適用されると、自己負担額は1割から3割になります。また、高額医療制度の対象となる場合、実際の自己負担額はさらに低くなります。
なお、上記の価格は2024年7月時点のものであり、最新の価格については随時ご確認ください。
以上

- 参考にした論文