内分泌疾患の一種である褐色細胞腫・パラガングリオーマ(PPGL)とは、副腎や交感神経節に発生する稀な腫瘍の総称です。
これらの腫瘍はカテコールアミンと呼ばれるホルモンを過剰に分泌することが特徴として挙げられます。
カテコールアミンには主にアドレナリンとノルアドレナリンがあり、通常はストレス時に分泌される物質です。
褐色細胞腫(かっしょくさいぼうしゅ)は副腎髄質に、パラガングリオーマは副腎外の交感神経節に発生します。
これらの腫瘍ではカテコールアミンが常に過剰に作られるため、様々な症状が引き起こされます。
病型と特徴
PPGLの基本分類
褐色細胞腫・パラガングリオーマ(PPGL)は発生部位によって大きく二つの病型に分類されます。
副腎髄質に発生する腫瘍を褐色細胞腫(PCC)と呼びます。
一方、副腎外の交感神経節に発生する腫瘍をパラガングリオーマ(PGL)と呼びます。
両者は組織学的には類似していますが、発生部位の違いにより特徴が異なるのです。
| 病型 | 発生部位 |
| 褐色細胞腫 | 副腎髄質 |
| パラガングリオーマ | 副腎外交感神経節 |
PCCの特徴
褐色細胞腫は副腎髄質に発生する腫瘍で全PPGLの約80-85%を占めます。
この腫瘍はカテコールアミンを過剰に産生し分泌することが特徴です。
褐色細胞腫の大部分は良性ですが、約10%は悪性の経過をたどる可能性があります。
腫瘍のサイズはさまざまで数センチから10センチを超えるものまで報告されています。
PGLの特徴
パラガングリオーマは副腎外の交感神経節に発生する腫瘍でPPGLの約15-20%を占めます。
発生部位は多岐にわたり、頸部腹部骨盤内など様々な場所に見られる傾向です。
パラガングリオーマは褐色細胞腫と比較して悪性化する割合が高く、約20-25%が転移や浸潤を示すことがあります。
| 発生部位 | 頻度 |
| 腹部 | 約60% |
| 骨盤 | 約20% |
| 胸部 | 約10% |
| 頭頸部 | 約10% |
機能性と非機能性PPGLの区別
PPGLはホルモン産生能の有無によって機能性と非機能性に分類されます。
機能性PPGLはカテコールアミンを過剰に産生し様々な臨床症状を引き起こしますが、非機能性PPGLはホルモン産生が乏しく臨床症状が現れにくい傾向です。
- 機能性PPGLの特徴
- カテコールアミン過剰産生
- 典型的な臨床症状の出現
- 生化学的検査で異常値
- 非機能性PPGLの特徴
- ホルモン産生が乏しい
- 臨床症状が乏しいまたは無症状
- 画像検査で偶発的に発見されることが多い
遺伝性と散発性PPGLの区別
PPGLは遺伝性と散発性に分類されます。
遺伝性PPGLは特定の遺伝子変異に関連して発生し家族性に見られることがあります。散発性PPGLは遺伝的素因が明らかでなく孤発的に発生します。
| 分類 | 特徴 |
| 遺伝性PPGL | 特定遺伝子変異関連家族性発生 |
| 散発性PPGL | 遺伝的素因不明孤発的発生 |

PPGLの主症状
褐色細胞腫・パラガングリオーマは特徴的な症状を引き起こすことで知られています。
この疾患の主症状を理解することは早期発見や適切な対応につながる可能性があるため極めて重要です。
高血圧
PPGLの代表的な症状として高血圧が挙げられます。
この高血圧は持続性または発作性に現れることがあり、患者さんの生活に大きな影響を与えかねません。
持続性高血圧の場合は常に血圧が高い状態が続くのに対し、発作性高血圧では突然の血圧上昇が起こります。
発作性高血圧は数分から数時間続くこともあり、患者さんに強い不安や恐怖を与えることがあるでしょう。
| 高血圧の種類 | 特徴 |
| 持続性高血圧 | 常に血圧が高い |
| 発作性高血圧 | 突然の血圧上昇 |
動悸・頭痛・発汗
PPGLの患者さんがよく経験する症状として動悸・頭痛・発汗があります。このような症状は単独で現れることもありますが、多くの場合は複合的に発生します。
動悸は心臓がドキドキする感覚として表現されることが多く、患者さんを不安にさせる要因となります。
頭痛は強い痛みを伴うことがあり日常生活に支障をきたすほどのケースもあります。
発汗は特に夜間や安静時に生じることが多く、寝具を濡らすほどの多量の汗をかくこともあります。
上記のような症状は患者さんのQOL(生活の質)を著しく低下させる可能性があるため医療機関での適切な評価が必要です。
その他の症状
PPGLでは他にも以下のようなさまざまな症状が現れる可能性があります。
- 不安感や焦燥感
- めまいや立ちくらみ
- 体重減少
- 便秘や下痢などの消化器症状
これらの症状は患者さんによって異なり個人差が大きいのが特徴です。また症状の強さや頻度も人それぞれで一定ではありません。
| 症状 | 特徴 |
| 不安感・焦燥感 | 理由のない不安や落ち着かなさ |
| めまい・立ちくらみ | 急な体位変換時に多い |
| 体重減少 | 代謝亢進による |
| 消化器症状 | 便秘や下痢が交互に現れることも |
無症状の場合
PPGLの中には全く症状を示さないケースも存在します。これらは「無症候性PPGL」と呼ばれ、他の検査や健康診断で偶然発見されることも少なくありません。
無症状であっても体内では異常な状態が続いている場合があるため注意が必要です。
定期的な健康診断や血圧測定が早期発見につながる可能性があります。
| 発見のきっかけ | 具体例 |
| 健康診断 | 血圧異常の指摘 |
| 画像検査 | CT・MRIでの偶発的発見 |
| 血液検査 | ホルモン値の異常 |
症状の変動
PPGLの症状は日によって大きく変動することがあります。これは腫瘍から分泌されるホルモンの量が一定ではないためです。
ある日は激しい症状に悩まされるのに別の日はほとんど症状がないということもあります。
このような症状の変動は患者さんを混乱させ診断を難しくする要因となることがあるでしょう。
症状の記録をつけることで医療機関での適切な評価につながる可能性があります。
- 症状の種類
- 症状の強さ
- 症状の持続時間
- 症状が現れた状況や時間帯
以上のように内分泌疾患の一種である褐色細胞腫・パラガングリオーマ(PPGL)の主症状は多岐にわたり個人差も大きいのが特徴です。

原因やきっかけ
褐色細胞腫・パラガングリオーマ(PPGL)の原因やきっかけは複雑で多岐にわたります。
遺伝的要因と環境因子が複雑に絡み合い発症に至ると考えられていますが、未だ不明な点も多く存在します。
遺伝的要因
PPGLの発症には遺伝的要因が重要な役割を果たしています。
全体の約40%が何らかの遺伝子変異と関連があるとされていて、主な遺伝子変異は以下のようなものです。
- RET遺伝子
- VHL遺伝子
- SDHB遺伝子
- SDHD遺伝子
これらの遺伝子変異は細胞の増殖や分化に関わる重要なタンパク質の機能を変化させ、PPGLの発症リスクを高めると考えられています。
| 遺伝子 | 関連疾患 |
| RET | 多発性内分泌腫瘍症2型 |
| VHL | フォンヒッペル・リンドウ病 |
| SDHB/D | 遺伝性パラガングリオーマ症候群 |
遺伝性PPGLの場合家族歴が認められることがありますが、散発性の場合も存在します。
細胞内シグナル伝達の異常
PPGLの発症には細胞内シグナル伝達の異常が関与していると考えられています。
特に以下のような経路の異常が指摘されています。
- RAS/RAF/MEK/ERK経路
- PI3K/AKT/mTOR経路
これらの経路の異常活性化は細胞の異常増殖やアポトーシス(細胞死)の回避につながり腫瘍形成を促進する可能性があるのです。
| シグナル経路 | 主な機能 |
| RAS/RAF/MEK/ERK | 細胞増殖制御 |
| PI3K/AKT/mTOR | 細胞生存制御 |
これらのシグナル伝達経路の異常は遺伝子変異や環境因子によって引き起こされる可能性があります。
環境因子
PPGLの発症には環境因子も関与している可能性が指摘されています。
以下のような要因が疑われていますがその詳細なメカニズムは未だ不明な点が多いです。
- 慢性的なストレス
- 化学物質への曝露
- 放射線被曝
- 特定の薬剤の長期使用
これらの環境因子が遺伝的素因と相互作用しPPGLの発症リスクを高める可能性が考えられています。
| 環境因子 | 想定されるメカニズム |
| ストレス | カテコールアミン産生亢進 |
| 化学物質 | DNA損傷 |
| 放射線 | 遺伝子変異誘発 |
ただしこれらの環境因子とPPGLの直接的な因果関係は現時点では明確には証明されていません。
発生学的要因
PPGLの原因を理解するうえで発生学的な観点も重要です。
褐色細胞腫(PCC)とパラガングリオーマ(PGL)はともに神経堤由来の細胞から発生します。
神経堤細胞は胎生期に広範囲に移動し様々な組織に分化する能力を持っています。
この過程で何らかの異常が生じるとPPGLの発症につながるとされているのです。
具体的には以下のような段階での異常が想定されます。
- 神経堤細胞の移動
- 細胞の分化
- 細胞死の制御
これらの過程に関与する遺伝子の変異や環境因子の影響がPPGLの発症リスクを高める可能性があります。
| 発生段階 | 関連する遺伝子例 |
| 細胞移動 | RET GDNF |
| 細胞分化 | ASCL1 PHOX2B |
| 細胞死制御 | BCL2 BAX |
エピジェネティクス
近年PPGLの発症メカニズムを理解するうえでエピジェネティクスの重要性が注目されています。
エピジェネティクスとはDNA配列の変化を伴わない遺伝子発現の制御機構のことを指します。
PPGLにおいては以下のようなエピジェネティックな変化が報告されているのです。
- DNAメチル化の異常
- ヒストン修飾の変化
- マイクロRNAの発現異常
これらの変化は遺伝子の発現パターンを変化させPPGLの発症や進展に関与する可能性があります。
| エピジェネティック変化 | 影響 |
| DNAメチル化亢進 | 遺伝子発現抑制 |
| ヒストンアセチル化 | 遺伝子発現亢進 |
| マイクロRNA発現変化 | mRNA分解制御 |

PPGLの診察と診断
褐色細胞腫・パラガングリオーマ(PPGL)の診察と診断は慎重かつ綿密に行われる必要があります。
この疾患の特性上、早期発見と正確な診断が患者さんの予後に大きく影響するため医療機関での適切な評価が不可欠です。
初診時の問診
PPGLの診察では詳細な問診が重要な役割を果たします。
まずは患者さんの自覚症状や生活習慣家族歴などについて丁寧に聞き取りを行います。
特に高血圧の有無やその性質(持続性か発作性か)について重点的に確認することが多いです。
問診では以下のような項目が含まれることがあります。
- 症状の種類と頻度
- 症状が出現する状況や時間帯
- 家族歴(特に内分泌疾患の有無)
- 日常生活習慣(食事運動睡眠など)
これらの情報は診断の手がかりとなるだけでなく後の検査計画にも影響を与えます。
| 問診項目 | 確認内容 |
| 症状 | 種類頻度持続時間 |
| 家族歴 | 内分泌疾患の有無 |
| 生活習慣 | 食事運動睡眠パターン |
身体診察
問診に続いて行われる身体診察ではPPGLに特徴的な所見を見逃さないよう注意深く行われます。
血圧測定は両上肢で行われることが多く場合によっては立位や臥位など異なる体位でも測定されます。
脈拍の確認や体重測定も重要な項目です。
さらに患者さんの皮膚の状態(蒼白や発汗の有無)にも注目しますし、時には腹部の触診を行い腫瘤の有無を確認することもあります。
これらの身体診察結果は総合的に評価され診断の一助となります。
| 身体診察項目 | 確認内容 |
| 血圧測定 | 両上肢異なる体位 |
| 脈拍確認 | 規則性頻脈の有無 |
| 皮膚状態 | 蒼白発汗の有無 |
血液・尿検査
PPGLの診断において血液検査と尿検査は極めて重要な役割を果たします。これらの検査では主にカテコールアミンとその代謝産物の測定が行われます。
血液検査ではノルアドレナリンアドレナリンドーパミンの血中濃度が測定されます。
尿検査では24時間蓄尿によるメタネフリンノルメタネフリンの排泄量が調べられることが多いです。
これらの検査結果はPPGLの診断基準の一部となっており、異常高値を示す場合には画像検査へと進むことになります。
| 検査項目 | 測定対象 |
| 血液検査 | カテコールアミン濃度 |
| 尿検査 | メタネフリン排泄量 |
画像検査
血液・尿検査で異常が疑われた場合画像検査が実施されます。
PPGLの診断で用いられる画像検査は次の通りです。
- CT(コンピュータ断層撮影)
- MRI(磁気共鳴画像)
- MIBG(メタヨードベンジルグアニジン)シンチグラフィ
- PET(陽電子放射断層撮影)
CTやMRIは腫瘍の位置や大きさを確認するのに適していますし、MIBGシンチグラフィやPETは腫瘍の機能的な特徴を評価するのに役立ちます。
これらの画像検査を組み合わせることでPPGLの存在診断だけでなく局在診断も可能となります。
遺伝子検査
近年PPGLの診断において遺伝子検査の重要性が増しています。
特に若年発症や両側性多発性の腫瘍家族歴がある場合には遺伝子検査が推奨されることがあります。
以下は主な検査対象遺伝子です。
- RET遺伝子
- VHL遺伝子
- SDHB遺伝子
- SDHD遺伝子
これらの遺伝子変異が確認されることでPPGLの診断確定や家族性の評価に役立つ可能性があります。
| 遺伝子 | 関連疾患 |
| RET | 多発性内分泌腫瘍症2型 |
| VHL | フォンヒッペル・リンドウ病 |
| SDHB/D | 遺伝性パラガングリオーマ症候群 |

PPGLの画像所見
褐色細胞腫・パラガングリオーマ(PPGL)の診断において画像検査は極めて重要な役割を果たします。
PPGLの画像所見を正確に理解し解釈することが早期発見や適切な治療方針の決定につながる可能性があるため医療従事者にとって不可欠なスキルです。
CT(コンピュータ断層撮影)所見
CTはPPGLの局在診断に広く用いられる画像検査の一つです。PPGLはCT上で一般的に境界明瞭な腫瘤として描出されます。
腫瘍の内部は不均一な濃度を示すことが多く時に嚢胞変性や出血壊死を反映した低吸収域が混在することがあります。
造影CTでは腫瘍は強い造影効果を示すのが特徴的です。
| CT所見 | 特徴 |
| 境界 | 明瞭 |
| 内部濃度 | 不均一 |
| 造影効果 | 強い |
大きさは様々ですが多くの場合3cm以上の腫瘤として認められます。
副腎原発の褐色細胞腫(PCC)では副腎の形状を保ったまま全体が腫大する「副腎腫大型」と副腎から突出するように発育する「副腎外突出型」が存在します。
一方パラガングリオーマ(PGL)は好発部位である傍大動脈領域や骨盤内に腫瘤として描出されます。
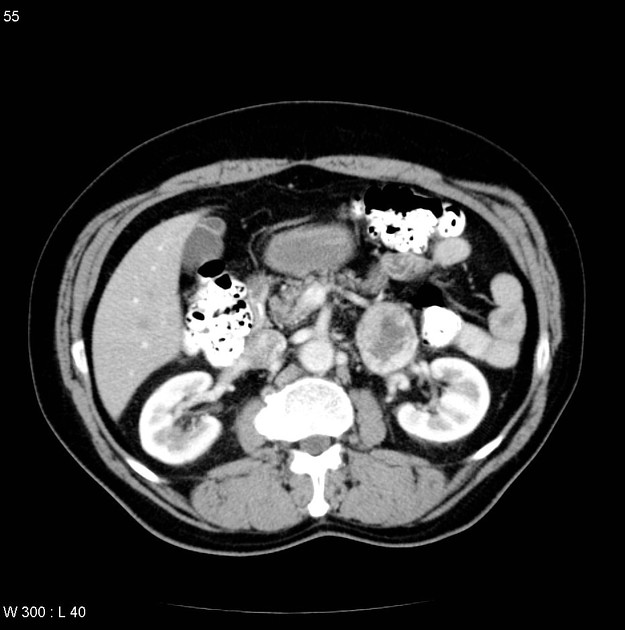
所見:左副腎の前肢から発生する3〜4 cmの円形の腫瘤があり、辺縁部に造影効果が認められる。この腫瘤は正常に見える左腎の前に位置している。右副腎は正常である。褐色細胞腫が疑われる。
MRI(磁気共鳴画像)所見
MRIはPPGLの質的診断に優れた画像検査モダリティです。
T1強調画像では腫瘍は一般的に低信号を示します。T2強調画像では特徴的な高信号を呈することが多く「light bulb sign」と呼ばれることがあります。
造影MRIではCTと同様に強い造影効果が認められます。
MRIは放射線被曝がないことや軟部組織のコントラスト分解能が高いことが利点です。
| MRI所見 | 特徴 |
| T1強調画像 | 低信号 |
| T2強調画像 | 高信号 |
| 造影効果 | 強い |
PPGLの診断においてMRIは以下のような点で有用です。
- 腫瘍の内部構造の詳細な評価
- 周囲臓器との関係の把握
- 多発病変の検出
特に造影剤アレルギーや腎機能障害のある患者さんではCTの代替として重要な役割を果たします。
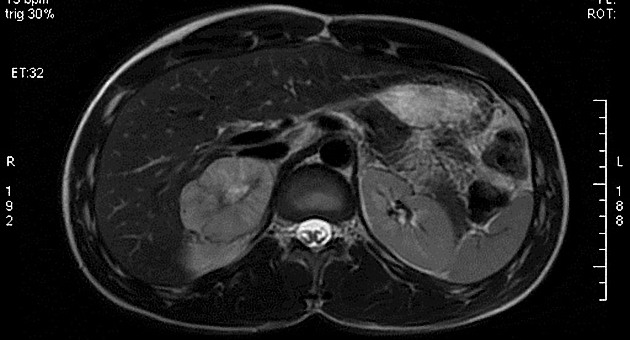
所見:腫瘤はT1強調画像で低信号、T2強調画像で高信号を示しており、in-phaseおよびout-of-phase画像間での有意な信号低下がないため、細胞内脂肪の有意な存在は示されていない。
MIBG(メタヨードベンジルグアニジン)シンチグラフィ所見
MIBGシンチグラフィはPPGLの機能的画像診断法として広く用いられています。
MIBGはカテコールアミンのアナログであり腫瘍細胞に特異的に取り込まれる性質があります。
PPGLではMIBGの異常集積として描出されるのが典型的な所見です。
全身の撮像が可能であるため多発病変や転移巣の検出に優れています。
| MIBG所見 | 意義 |
| 異常集積 | 腫獋の存在 |
| 多発集積 | 多発病変の可能性 |
| 遠隔集積 | 転移の可能性 |
MIBGシンチグラフィの感度は80-90%程度とされていますが、偽陰性例も存在するため注意が必要です。特に小さな腫瘍や分化度の低い腫獋では集積が乏しいことがあります。
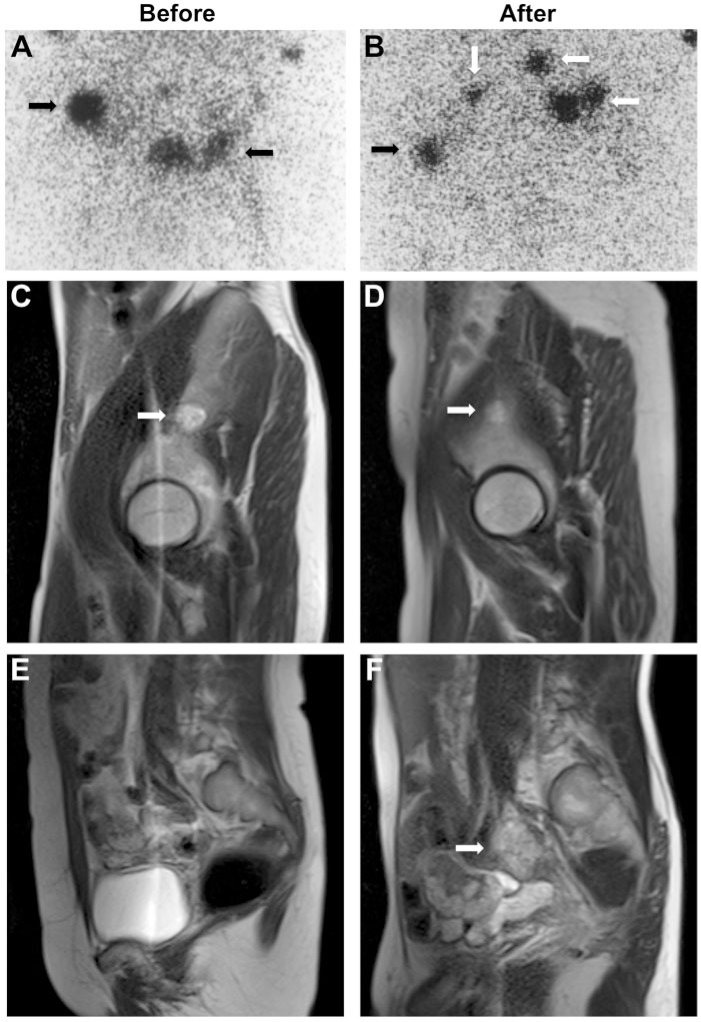
所見:悪性褐色細胞腫のMIBGスキャンの骨盤前面画像。(A) 化学療法前には、右腸骨翼および左寛骨臼におけるトレーサーの集積増加が認められる(黒矢印)。右および左腸骨鎖の複数のリンパ節および近位大腿骨にかすかな集積が見られる。(B) 化学療法後には、右腸骨翼での集積が減少(矢印)し、左寛骨臼および大腿骨での集積は消失している。右大腿骨での集積は変わらず、右および左腸骨鎖の複数のリンパ節での集積が増加している(白矢印)。
右腸骨翼の矢状断T2強調ターボスピンエコーMRI画像:(C) 化学療法前には、2 cmの高信号病変が見られる(白矢印)。(D) 化学療法後には、病変のサイズが1 cmに減少している(白矢印)。
左骨盤の矢状断T2強調ターボスピンエコーMRI画像:(E) 化学療法前には異常は見られない。(F) 化学療法後には、3 cmを超える大きさの腸骨リンパ節腫大の一部が検出可能である(白矢印)。
PET(陽電子放射断層撮影)所見
近年PPGLの診断においてPETの有用性が注目されています。
18F-FDG PETでは腫瘍の糖代謝を反映した集積が認められます。
PPGLは一般的に強い集積を示すことが多く悪性度の評価にも役立つ可能性があります。
また18F-FDOPA PETはカテコールアミン産生腫瘍に特異的な集積を示すため診断精度が高いとされています。
以下はPETの利点です。
- 高い空間分解能
- 定量評価が可能
- 全身検索が可能
| PET種類 | 特徴 |
| FDG-PET | 糖代謝反映 |
| FDOPA-PET | カテコールアミン特異的 |
以上のように内分泌疾患の一種である褐色細胞腫・パラガングリオーマ(PPGL)の画像所見は多岐にわたります。
CTMRIMIBGシンチグラフィPETなど様々な画像モダリティを組み合わせることでPPGLの局在診断機能評価、さらには悪性度評価まで幅広い情報を得ることが可能です。
これらの画像所見を総合的に判断することがPPGLの正確な診断と適切な治療方針の決定につながる重要な要素となります。
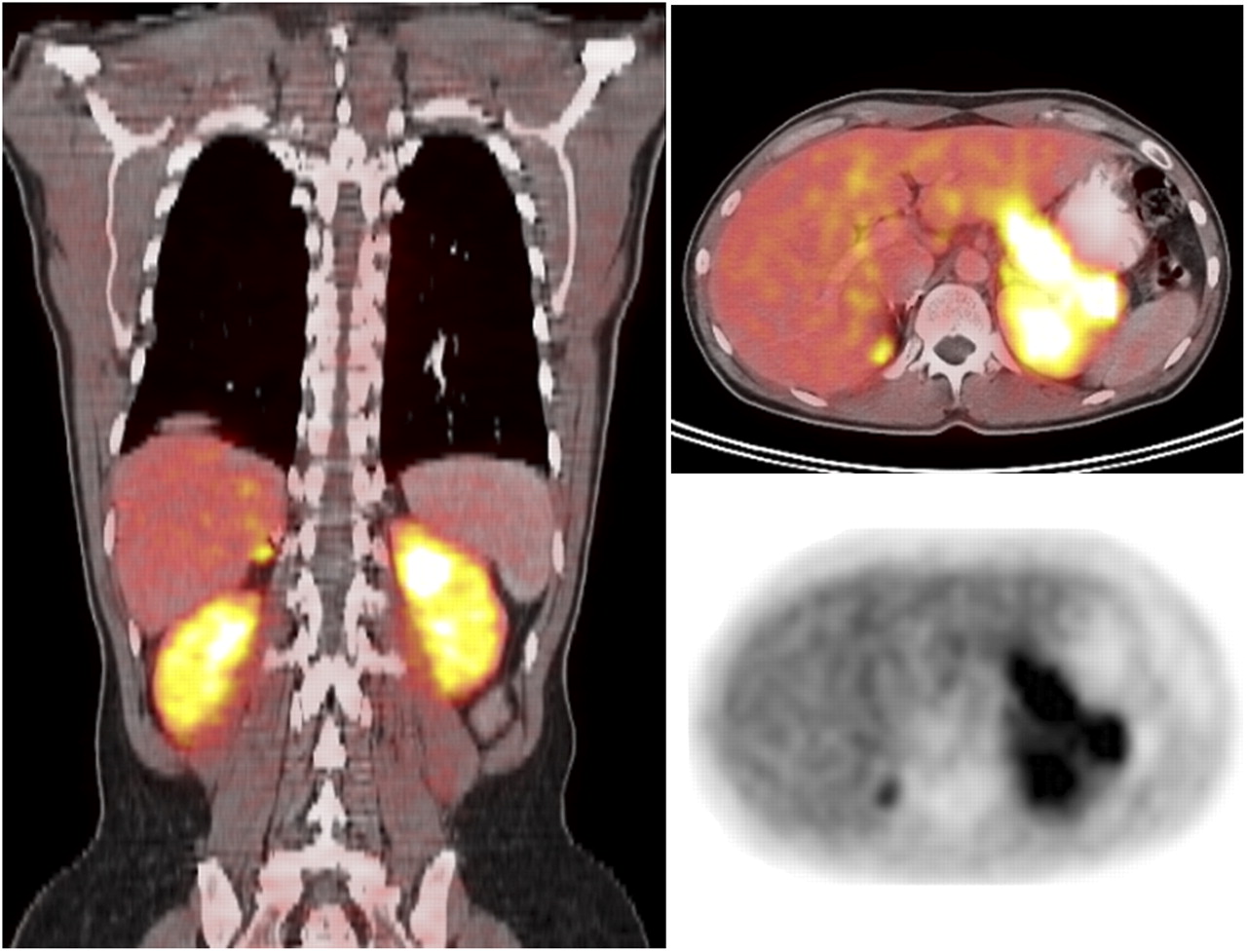
所見:右副腎床に残存または再発した褐色細胞腫が認められる。

PPGLの治療方法と薬 治癒までの期間
褐色細胞腫・パラガングリオーマ(PPGL)の治療は多岐にわたり個々の患者さんの状態に応じて慎重に選択されます。
PPGLの治療方針を適切に決定し実行することが患者さんの予後改善と生活の質向上につながる重要な要素となるのです。
外科的治療
PPGLの根治的治療として外科的切除が第一選択となることが多いです。腫瘍の完全切除を目指し術式は腫瘍の局在や大きさに応じて決定されます。
褐色細胞腫(PCC)の場合副腎摘出術が行われることが一般的です。
一方パラガングリオーマ(PGL)では腫瘍の発生部位に応じた切除術が選択されます。
| 腫瘍の種類 | 主な手術法 |
| PCC | 副腎摘出術 |
| PGL | 腫瘍切除術 |
近年では腹腔鏡下手術や後腹膜鏡下手術など低侵襲な術式も積極的に導入されています。
これらの術式選択は腫瘍の大きさ局在悪性度などを考慮して慎重に判断されるでしょう。
術前の薬物治療
PPGLの手術に際しては術前の薬物治療が不可欠で、この治療の主な目的は以下の通りです。
- 血圧のコントロール
- 心拍数の安定化
- 循環血液量の是正
α遮断薬が第一選択薬として用いられることが多く代表的な薬剤にはドキサゾシンやフェノキシベンザミンがあります。
これらの薬剤は通常手術の10〜14日前から開始され徐々に増量されていきます。
| 薬剤名 | 分類 |
| ドキサゾシン | α1遮断薬 |
| フェノキシベンザミン | 非選択的α遮断薬 |
α遮断薬投与後必要に応じてβ遮断薬が追加されることがあります。
β遮断薬は頻脈や不整脈の管理に効果的ですがα遮断薬による十分な前処置なしに使用すると危険な血圧上昇を引き起こす可能性があるため注意が必要です。
手術中の管理
PPGL手術中の血行動態管理は極めて重要です。
腫瘍操作に伴うカテコールアミンの急激な放出により血圧の急上昇や不整脈が生じる可能性があるためです。
手術中は以下のような点に注意が払われます。
- 持続的な動脈圧モニタリング
- 中心静脈圧の管理
- 適切な輸液管理
必要に応じて短時間作用性のα遮断薬(フェントラミンなど)やβ遮断薬(エスモロールなど)が静脈内投与されます。
| 管理項目 | 使用薬剤例 |
| 血圧上昇時 | フェントラミン |
| 頻脈時 | エスモロール |
術後管理と経過観察
PPGL手術後は慎重な経過観察が必要となります。術後早期には急激な血圧低下や低血糖に注意が必要です。
これらは腫瘍摘出後のカテコールアミン分泌急減によるものと考えられているのです。
術後の回復期間は個人差が大きいものの多くの場合1〜2週間程度で退院可能となるでしょう。
長期的な経過観察も重要であり定期的な血圧測定や血液検査画像検査が行われます。
| 術後合併症 | 対応 |
| 低血圧 | 輸液管理昇圧剤 |
| 低血糖 | ブドウ糖投与 |
術後の治癒判定と予後
PPGLの手術後治癒判定には一定の期間を要します。一般的には術後6ヶ月〜1年程度経過した時点で以下の項目を確認し総合的に判断されます。
- 血圧の正常化
- 血中・尿中カテコールアミン値の正常化
- 画像検査での腫瘍再発所見の有無
良性のPPGLであれば完全切除により治癒が期待できますが、悪性例では長期的な経過観察が必要となります。
治癒後も5年以上にわたる定期的なフォローアップが推奨されることが多いです。

治療の副作用やデメリット(リスク)
PPGLの治療には様々な副作用やデメリットが伴う可能性があります。
これらのリスクを理解し適切に対処することが患者さんの安全と治療の成功につながる重要な要素となります。
術前薬物療法のリスク
PPGLの術前管理で用いられるα遮断薬には特有の副作用が存在します。
ドキサゾシンやフェノキシベンザミンなどのα遮断薬使用時には以下のような副作用に注意が必要です。
- 起立性低血圧
- めまい
- 倦怠感
- 鼻閉
これらの副作用は薬剤の用量調整により軽減できることが多いですが、患者さんの日常生活に影響を与える可能性があります。
| 薬剤 | 主な副作用 |
| ドキサゾシン | 起立性低血圧めまい |
| フェノキシベンザミン | 倦怠感鼻閉 |
また必要に応じて使用されるβ遮断薬にも気管支喘息の悪化や末梢循環不全などのリスクがあります。
これらの薬剤使用時には慎重なモニタリングが不可欠です。
手術に伴うリスク
PPGLの外科的治療には一般的な手術リスクに加え特有のデメリットが存在します。
腹腔鏡下手術や後腹膜鏡下手術などの低侵襲手術でのリスクは次の通りです。
- 出血
- 感染
- 周辺臓器の損傷
特にPPGLの手術では腫瘍操作に伴う急激な血圧変動が問題となることが報告されています。
腫瘍からのカテコールアミン大量放出により危険な高血圧クリーゼを引き起こす可能性があるためです。
| 手術リスク | 対処法 |
| 出血 | 輸血準備 |
| 感染 | 予防的抗生剤 |
| 血圧変動 | 厳密な循環管理 |
また褐色細胞腫(PCC)で副腎全摘出を行った場合副腎不全のリスクが生じ、この場合ステロイド補充療法が必要となることがあります。
術後合併症のリスク
PPGL手術後には特有の合併症リスクが存在します。
代表的なものとして以下が挙げられます。
- 低血圧
- 低血糖
- 電解質異常
これらは腫瘍摘出後のカテコールアミン急減に伴う変化と考えられています。特に術後早期には注意深いモニタリングと迅速な対応が求められます。
| 術後合併症 | 発生機序 |
| 低血圧 | カテコールアミン急減 |
| 低血糖 | インスリン感受性亢進 |
また長期的には腫瘍の再発や転移のリスクも存在するため定期的なフォローアップが大切です。
画像検査に伴うリスク
PPGLの診断や経過観察で行われる各種画像検査にもデメリットが存在します。
CTでは放射線被曝のリスクがあります。MRIは被曝の心配はありませんが閉所恐怖症の方には負担となる可能性があります。
核医学検査(MIBGシンチグラフィやPETなど)では放射性同位元素を用いるため被曝や薬剤アレルギーのリスクが考えられます。
| 検査 | 主なリスク |
| CT | 放射線被曝 |
| MRI | 閉所恐怖症 |
| 核医学検査 | 被曝アレルギー |
これらの検査におけるリスクは比較的低いものの、患者さんの状態や希望に応じて適切な検査法を選択することが重要です。
心理社会的リスク
PPGLの診断や治療過程では心理社会的なデメリットも生じる可能性があります。
具体的には以下のようなものが挙げられます。
- 病気に対する不安や恐怖
- 治療に伴う日常生活の制限
- 就労や社会活動への影響
- 経済的負担
これらの問題は患者さんのQOL(生活の質)に大きな影響を与える可能性があります。

再発の可能性と予防の仕方
褐色細胞腫・パラガングリオーマ(PPGL)は治療後も再発のリスクが存在する疾患として知られています。
再発の可能性を理解し適切な予防策を講じることが患者さんの長期的な健康維持にとって重要です。
再発の可能性
PPGLの再発率は様々な要因によって異なりますが一般的に5〜15%程度とされています。
再発のリスクは腫瘍の性質や手術の完全性などによって変動しますが、特に多発性や家族性の場合遺伝的要因が関与しているため再発リスクが高くなる傾向です。
| 再発リスク因子 | 影響 |
| 腫瘍の大きさ | 大きいほど高リスク |
| 多発性 | リスク増加 |
| 家族性 | リスク増加 |
再発までの期間も個人差が大きく数ヶ月から数十年後に再発が確認されることもあるため、長期にわたる経過観察が不可欠となります。
定期的なフォローアップ
再発の早期発見のためには定期的なフォローアップが極めて重要です。
フォローアップでは以下のような項目がチェックされます。
- 血圧測定
- 血液検査(カテコールアミン関連物質)
- 尿検査(カテコールアミン代謝産物)
- 画像検査(CT MRI など)
これらの検査を定期的に受けることで再発の兆候を早期に捉えることができます。
フォローアップの頻度は個々の患者さんの状況に応じて決定されますが、一般的には以下のようなスケジュールが推奨されることが多いです。
| 術後経過期間 | フォローアップ頻度 |
| 1年目 | 3〜6ヶ月毎 |
| 2〜5年目 | 6〜12ヶ月毎 |
| 5年以降 | 年1回 |
生活習慣の改善
PPGLの再発予防には日々の生活習慣の改善も重要な役割を果たします。
特に以下のような点に注意を払うことが推奨されます。
- バランスの取れた食事
- 適度な運動
- ストレス管理
- 十分な睡眠
これらの生活習慣は全身の健康維持に寄与するだけでなくホルモンバランスの安定化にも効果があると考いえるでしょう。
| 生活習慣 | 効果 |
| バランス食 | 栄養状態改善 |
| 適度運動 | 代謝促進 |
| ストレス管理 | ホルモン安定化 |
遺伝性PPGLへの対応
一部のPPGLには遺伝性のものが存在し、再発リスクが高くなることがあります。そのため遺伝性PPGLが疑われる場合には遺伝子検査を受けることが推奨されることがあります。
代表的な遺伝子変異は以下のようなものです。
- RET遺伝子
- VHL遺伝子
- SDHB遺伝子
- SDHD遺伝子
これらの遺伝子変異が確認された場合には、より厳密なフォローアップが必要となる可能性があります。
また家族のスクリーニングも考慮されることがあります。
ホルモンバランスの管理
PPGLの再発予防においてホルモンバランスの管理は大切な要素となります。
特にストレスホルモンであるコルチゾールの管理が重要視されています。過度のストレスはコルチゾール分泌を促進し内分泌系全体のバランスを崩す可能性があるためです。
ストレス管理のテクニックとしては以下のようなものが挙げられます。
- 瞑想
- ヨガ
- 深呼吸法
- マインドフルネス
これらの実践により自律神経系のバランスを整えホルモン分泌の安定化を図りやすくなるでしょう。
| ストレス管理法 | 期待効果 |
| 瞑想 | 精神安定 |
| ヨガ | 身体リラックス |
| 深呼吸法 | 自律神経調整 |
環境因子への注意
PPGLの再発予防には環境因子にも注意を払わなければなりません。
特に以下のような要素が影響を与える可能性があると考えられています。
- 過度の暑さ寒さ
- 高地環境
- 過激な運動
- アルコール摂取
上記のような環境因子はカテコールアミン分泌を刺激する可能性があるため注意が必要です。
日々の生活の中でこれらの要素に過度にさらされないよう心がけることが推奨されます。

PPGLの治療費
褐色細胞腫・パラガングリオーマ(PPGL)の治療費は診断から手術、術後管理まで含めると100万円以上になることがあります。
個々の状況により金額は変動するため、医療機関に相談することが重要です。
初診・再診料
初診料は通常2,910円~5,410円、再診料は750円~2,660円です。専門医療機関では若干高くなる傾向があります。
検査費用
血液検査や尿検査、画像診断などの費用は合計で1万円から10万円ほどかかることがあります。
| 検査項目 | 概算費用 |
| 血液検査 | 4,200円(血液一般+生化学5-7項目の場合) +カテコールアミン分画 1,650円 |
| CT検査 | 14,500円~21,000円 |
| MRI検査 | 19,000円~30,200円 |
手術費用
手術費用は、「腹腔鏡下副腎髄質腫瘍摘出術(褐色細胞腫)」 470,300円や「副腎腫瘍摘出術 2 髄質腫瘍(褐色細胞腫)」470,200円となります。
入院費用
入院期間や個室利用の有無により変動しますが、1日あたり1万円から3万円程度です。
| 入院タイプ | 1日あたりの概算費用 |
| 大部屋 | 10,000円〜15,000円 |
| 個室 | 20,000円〜30,000円 |
詳しく説明すると、日本の入院費計算システムは、「DPC(診断群分類包括評価)」という方式で入院費を算出します。これは患者さんの病気や治療内容に応じて費用を決める仕組みです。
DPCの特徴:
- 約1,400種類の病気グループに分類
- 1日ごとの定額制
- 一部の特殊な治療は別途計算
昔の「出来高」方式と比べると、DPCでは多くの診療行為が1日の定額に含まれます。
DPCと出来高方式の違い:
・出来高で計算されるもの:手術、リハビリ、特定の処置など
・DPCに含まれるもの:薬、注射、検査、画像診断など
計算方法:
(1日の基本料金) × (入院日数) × (病院ごとの係数) + (別途計算される治療費)
例えば、14日間入院した場合、この公式に当てはめて計算すると以下のようになります。
DPC名: 褐色細胞腫、パラガングリオーマ 手術あり 手術処置等2なし
日数: 14
医療機関別係数: 0.0948 (例:神戸大学医学部附属病院)
入院費: ¥343,820 +出来高計算分
医療費の支払いについて、もう少し詳しく説明します。
- 健康保険の適用
- 保険が使える場合、患者さんが支払う金額は全体の10%から30%になります。
- 年齢や収入によって、この割合が変わります。
- 高額医療費制度
- 医療費が一定額を超えると、この制度が適用されます。
- 結果として、実際に支払う金額がさらに少なくなることがあります。
- 料金の変更について
- ここでお話しした金額は2024年8月時点のものです。
- 医療費は状況によって変わることがあるので、最新の情報は病院や健康保険組合に確認するのがよいでしょう。
このように、実際の支払額は保険や制度によって大きく変わる可能性があります。自分の状況に合わせて、詳しい情報を得ることをおすすめします。
以上





