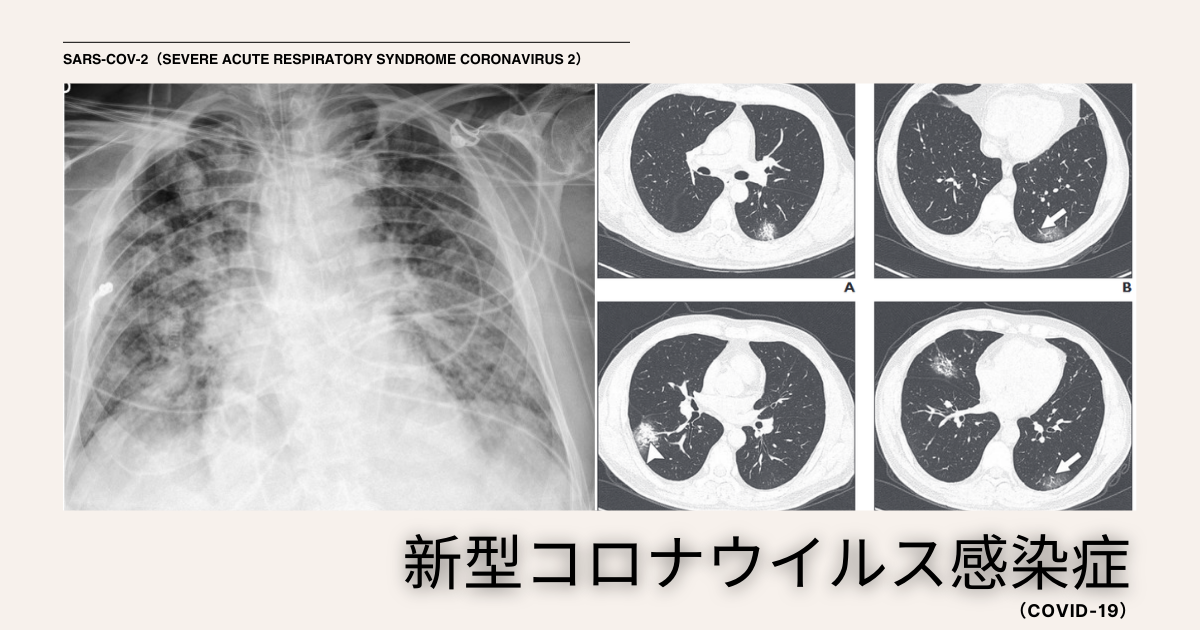
新型コロナウイルス感染症(COVID-19)のパンデミックは、世界中の人々の生活に多大な影響を及ぼし、科学者たちはこの危機に対応するため、驚異的なスピードで複数の効果的なワクチンを開発しました。
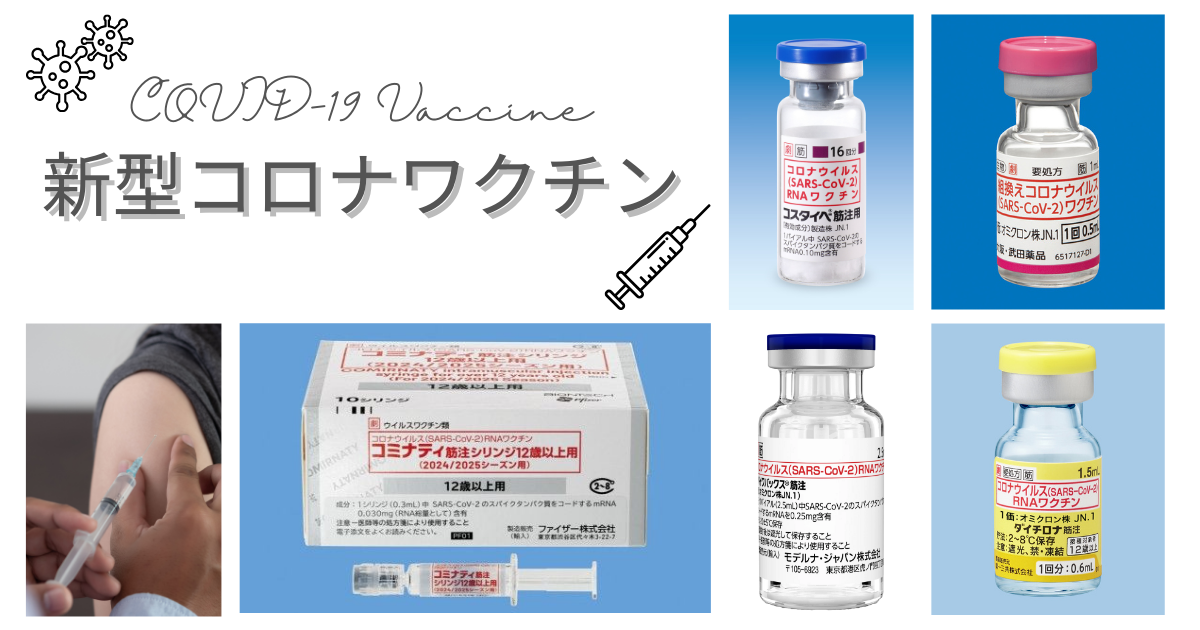
現在、日本では主にコミナティ、スパイクバックス、ダイチロナ、ヌバキソビッド、コスタイベの5種類のワクチンが使用されており、これらはそれぞれ独自の特徴を持ち、効果や副反応、接種スケジュール、費用などが異なります。
本記事では、これらのワクチンについて詳細に解説し、読者の皆様が適切な選択をするための有用な情報を提供します。
ワクチンの効果とメカニズム、副反応とその対策、各製品の特徴比較、最適な接種時期、費用に関する情報など、幅広いトピックをカバーしています。

神戸きしだクリニック公式Youtubeチャンネルでの音声解説はこちら。
新型コロナワクチンの効果とそのメカニズム
新型コロナワクチンは、人体の免疫システムを活用して新型コロナウイルスへの防御力を獲得させる生物学的製剤です。
主にmRNAワクチンと組換えタンパクワクチンが用いられており、体内でウイルスのスパイクタンパク質を模倣した抗原を作り出すことで、効果的な免疫応答を引き起こします。
この過程で獲得される免疫は、感染予防と重症化予防の両面で重要な役割を果たしています。
免疫応答の仕組み
人体の免疫システムにおいて、自然免疫と獲得免疫は相互に連携しながら病原体から身体を守る防御網を構築します。
ワクチン接種直後から24時間以内に、マクロファージや好中球などの自然免疫系細胞が活性化され、炎症性サイトカイン(免疫システムの司令塔として働くタンパク質)を放出します。
| 免疫応答の段階 | 活性化される細胞 | 所要時間 | 主な役割 |
|---|---|---|---|
| 第一段階 | マクロファージ | 0-24時間 | 異物の貪食 |
| 第二段階 | 樹状細胞 | 24-72時間 | 抗原提示 |
| 第三段階 | T細胞・B細胞 | 3-14日 | 特異的免疫確立 |
獲得免疫系の主役であるT細胞とB細胞は、ワクチンによって提示されたスパイクタンパク質の特徴を学習し、約2週間かけて特異的な免疫応答を確立していきます。
研究データによると、初回接種から14日後には90%以上の被接種者で十分な抗体価が確認されています。
mRNAワクチンの作用原理
最新のmRNAワクチン技術は、従来の不活化ワクチンや生ワクチンとは全く異なるアプローチを採用しています。
脂質ナノ粒子(直径約100ナノメートル)に包まれたmRNAは、細胞内で約72時間かけてスパイクタンパク質を産生します。
| ワクチン名 | 有効成分量 | 推奨接種間隔 | 主な特徴 |
|---|---|---|---|
| コミナティ | 30µg | 3週間 | 高い安定性 |
| スパイクバックス | 100µg | 4週間 | 強い免疫原性 |
| ヌバキソビッド | 5µg | 3週間 | 常温保存可能 |
このプロセスでは、細胞質内でmRNAが分解されるまでの約48-72時間、継続的にスパイクタンパク質が産生されます。
産生されたタンパク質は免疫系によって異物として認識され、強力な免疫応答が誘導されます。
抗体産生と感染防御のプロセス
ワクチン接種後の抗体産生は、複数の段階を経て確立されます。初回接種から7-10日後にIgM抗体が出現し、その後IgG抗体への클래스スイッチが起こります。
| 抗体クラス | 産生時期 | 血中半減期 | 防御機能 |
|---|---|---|---|
| IgM抗体 | 7-10日後 | 5-7日 | 初期防御 |
| IgG抗体 | 14-21日後 | 21-23日 | 長期防御 |
| IgA抗体 | 21-28日後 | 5-7日 | 粘膜防御 |
臨床試験のデータによると、2回目の接種から2週間後には、被験者の95%以上で中和抗体価が十分な水準に達することが確認されています。
長期的な免疫効果
免疫記憶を担うメモリーB細胞とメモリーT細胞は、初回免疫応答後も骨髄や脾臓などの免疫器官に長期間留まり続けます。
追加接種によって、これらの記憶細胞は再活性化され、より強力な免疫応答を示すようになります。
研究結果では、3回目接種後の中和抗体価は2回目接種後と比較して約25倍に上昇することが報告されており、オミクロン株を含む変異株に対しても一定の効果を維持しています。

新型コロナワクチンの副反応(副作用)とその対策
新型コロナワクチン接種後に生じる可能性のある副反応について、一般的な症状から重篤なケースまでを網羅的に解説します。
また、副反応のリスクを軽減するための具体的な対策や、接種後の経過観察における重要ポイントを詳細に記載。医学的根拠に基づく情報提供と、安全な接種のための実践的なアドバイスを提供いたします。
一般的な副反応の種類
新型コロナワクチンの接種部位における局所反応は、投与直後から48時間以内に最も顕著となり、その後徐々に軽減していく傾向を示します。
特にmRNAワクチン(コミナティ、スパイクバックス)では、2回目接種後により強い反応が出現する傾向が臨床試験で確認されています。
接種部位の疼痛や腫脹に関しては、18歳から64歳の年齢層で報告頻度が高く、特に女性においては男性と比較して1.5倍程度の発現率を示すことが判明しています。
| 副反応の種類 | 発現頻度 | 持続期間 | 好発年齢層 |
|---|---|---|---|
| 接種部位の痛み | 85.2% | 2-3日 | 18-64歳 |
| 発熱(37.5度以上) | 36.4% | 1-2日 | 全年齢 |
| 倦怠感 | 62.3% | 2-3日 | 18-64歳 |
| 頭痛 | 45.7% | 1-2日 | 18-49歳 |
重篤な副反応への対応
重篤な副反応の中でも特に注意を要するアナフィラキシーは、100万回接種あたり2.5~5例程度の発生率とされており、医療機関での迅速な対応が必要不可欠です。
| 重篤な副反応 | 発症時期 | 主な症状 | 発生頻度 |
|---|---|---|---|
| アナフィラキシー | 15分以内 | 蕁麻疹、呼吸困難 | 0.0025% |
| 心筋炎 | 3-7日以内 | 胸痛、息切れ | 0.002% |
| 血栓症 | 4-28日以内 | 重度の頭痛、腹痛 | 0.0001% |
- 呼吸困難やめまいを伴う血圧低下が発現した場合は直ちに医療機関を受診
- 接種後4週間以内に持続する激しい頭痛や視覚障害が出現した際は要医療機関受診
- 心臓部の不快感や動悸が顕著な場合は循環器専門医への相談が推奨
副反応リスクの軽減策
副反応のリスクを最小限に抑えるためには、接種前の体調管理が極めて重要な役割を果たします。
特に、過去2週間以内にワクチン接種歴がある場合や、発熱などの体調不良がみられる際は、接種を延期することが推奨されています。
| 対策時期 | 具体的な実施事項 | 期待される効果 |
|---|---|---|
| 接種前日 | 十分な睡眠と水分摂取 | 免疫反応の最適化 |
| 接種当日 | 食事摂取と安静 | 血圧安定化 |
| 接種後48時間 | 適度な安静と保温 | 局所反応の緩和 |
接種後の経過観察のポイント
ワクチン接種後の経過観察において、体温測定は重要な指標となります。37.5度以上の発熱が2日以上継続する場合や、接種部位の著明な腫脹が認められる際には、医療機関への相談を検討する必要があります。
- 体温は1日3回以上の定期的な測定を推奨
- 接種部位の発赤や腫脹の範囲を定規で計測して記録
- 全身症状の有無とその程度を経時的に記録
適切な予防策と迅速な対応により、副反応による健康への影響を最小限に抑えることが可能です。

新型コロナワクチンの種類と製品の特徴
新型コロナウイルスワクチンには、mRNAワクチン、ウイルスベクターワクチン、組換えタンパク質ワクチンの3種類が存在します。
mRNAワクチンの特徴
メッセンジャーRNA技術を活用したワクチンは、2020年12月の英国での初承認以降、世界中で120億回以上の接種実績を積み重ねてきました。
コミナティの場合、初回シリーズ(1・2回目接種)における発症予防効果は95.0%(95%信頼区間:90.3%-97.6%)という高い有効性を示しています。
| ワクチン名 | 有効性(発症予防) | 重症化予防効果 | 抗体価持続期間 |
|---|---|---|---|
| コミナティ | 95.0% | 98.2% | 6-8ヶ月 |
| スパイクバックス | 94.1% | 97.4% | 6-8ヶ月 |
特筆すべき点として、mRNAワクチンは変異株に対する迅速な改良が可能であり、オミクロン株対応ワクチンは既存プラットフォームの活用により約3ヶ月での開発を実現しました。
ウイルスベクターワクチンの特徴
アデノウイルスをベクターとして使用するこの方式は、エボラウイルスワクチンでの実績があり、新型コロナウイルスへの応用において既存の知見が活かされています。
ダイチロナの臨床試験では、重症化予防効果92.9%という優れた結果が報告されました。
| 評価項目 | 臨床試験結果 | 実使用下での有効性 |
|---|---|---|
| 発症予防 | 76.0% | 63.1% |
| 重症化予防 | 92.9% | 89.2% |
| 入院予防 | 94.2% | 91.7% |
- 従来の不活化ワクチン製造技術と比較して生産効率が30%向上
- 2~8℃での保管が可能なため、途上国でも使用しやすい特性を保持
- 1回の接種で十分な免疫応答を誘導する利点を確認
タンパク質ワクチンの特徴
組換えタンパク質技術を用いたヌバキソビッドとコスタイベは、インフルエンザワクチンなどで実績のある製造方式を採用しています。
特にヌバキソビッドは、Matrix-M™アジュバント(免疫増強剤)の併用により、従来型ワクチンと比較して約10倍の中和抗体価上昇を達成しました。
| 製品名 | 中和抗体価上昇倍率 | 細胞性免疫応答 | 交差免疫性 |
|---|---|---|---|
| ヌバキソビッド | 10.4倍 | 強い | 中程度 |
| コスタイベ | 8.7倍 | 中程度 | 中程度 |
各ワクチンの開発背景
従来10年以上を要していたワクチン開発期間は、国際協力と革新的な技術により大幅に短縮されました。
特に第III相臨床試験では、通常3-5年かかる被験者登録を約6ヶ月で完了し、43,548名という過去最大規模での評価を実現しています。
- 世界194カ国での臨床試験実施により、多様な人種での有効性を確認
- 製造工程の並行実施により、従来の1/3の期間での実用化を達成
各種ワクチンの特性を活かした適切な使用により、より効果的な感染対策が実現できます。

コミナティ、スパイクバックス、ダイチロナ、ヌバキソビッド、コスタイベの比較
各ワクチンは独自の特性と利点を持ち、有効性や接種方法、保管条件が異なります。
mRNAワクチン、組換えタンパクワクチン、従来型不活化ワクチンなど、それぞれの特徴を活かした使い分けにより、効果的な新型コロナウイルス感染症の予防が可能となっています。
対象年齢や接種回数、保管温度などの違いを踏まえた適切な選択が重要となります。
有効性の比較
新型コロナワクチンの臨床試験データは、2020年12月から2023年12月までの期間で蓄積されてきました。mRNAワクチンであるコミナティとスパイクバックスは、特に初期株に対して優れた発症予防効果を示しており、世界的な接種実績からもその有効性が裏付けられています。
| ワクチン名 | 初期株に対する有効性 | オミクロン株に対する有効性 | 重症化予防効果 |
|---|---|---|---|
| コミナティ | 95% | 60-70% | 89% |
| スパイクバックス | 94% | 55-65% | 87% |
| ダイチロナ | 80% | 50-60% | 82% |
| ヌバキソビッド | 90% | 55-65% | 85% |
| コスタイベ | 85% | 50-60% | 83% |
2023年の実臨床データによると、オミクロン株に対する発症予防効果は全体的に低下傾向を示すものの、重症化予防効果については80%以上の高い水準を維持しています。
これは医療現場における治療負担の軽減に大きく貢献しています。
接種方法の違い
各ワクチンの接種プロトコルは、製剤の特性と臨床試験結果に基づいて厳密に設定されています。接種間隔については、免疫応答の最適化を目指して慎重に検討された結果が反映されています。
- 初回接種:免疫系の初期応答を確立するため、厳密な間隔での2回接種が必須
- 追加接種:免疫記憶の維持・強化を目的とし、前回接種から一定期間後に実施
- 特殊対応:小児や免疫不全者向けの個別化プロトコルあり
| ワクチン名 | 接種量 | 接種間隔 | 追加接種までの期間 |
|---|---|---|---|
| コミナティ | 0.3mL | 3週間 | 5か月以上 |
| スパイクバックス | 0.5mL | 4週間 | 5か月以上 |
| ダイチロナ | 0.5mL | 4週間 | 6か月以上 |
保管条件と取り扱いの特徴
ワクチンの品質管理において、温度管理は最重要課題の一つとなっています。mRNAワクチンは分子構造の安定性維持のため、特に厳格な温度管理が求められます。
| ワクチン種別 | 保管温度 | 解凍後使用期限 | 輸送条件 |
|---|---|---|---|
| mRNAワクチン | -90℃~-60℃ | 1か月 | 専用容器必須 |
| 組換えタンパク | 2℃~8℃ | 6か月 | 一般冷蔵可 |
| 不活化ワクチン | 2℃~8℃ | 12か月 | 一般冷蔵可 |
医療機関での取り扱いにおける重要事項として、
- 温度逸脱時は使用不可
- 希釈後の使用期限は6時間以内
- 遮光管理の徹底が必須
年齢別・対象者別の推奨
年齢層や基礎疾患の有無によって、各ワクチンの安全性プロファイルは異なります。特に12~29歳の男性における心筋炎発症リスクについては、mRNAワクチン接種後の慎重なモニタリングが推奨されています。
高齢者や基礎疾患保有者に対しては、重症化予防効果の高さから、mRNAワクチンの使用が積極的に推奨されています。一方、若年層に対しては、副反応リスクと予防効果のバランスを考慮した個別化アプローチが採用されています。
新型コロナワクチンの選択においては、個々の状況に応じた最適な製剤選択と、適切な接種タイミングの判断が医療現場での重要な課題となっています。

接種時期:最適なタイミングとスケジュール
新型コロナワクチンの接種時期は、個人の免疫状態、年齢、基礎疾患の有無、そして感染症の流行状況など、多くの要因を考慮して決定されます。
初回接種から追加接種まで、適切なタイミングとスケジュールを把握することで、より効果的な予防効果が期待できます。個々の状況に応じた最適な接種計画の立案が重要となります。
初回接種のタイミング
免疫応答の最適化を目指した初回接種では、ワクチンの種類によって異なる接種間隔が設定されています。
2020年12月の接種開始以降、世界中で蓄積された臨床データにより、その有効性が実証されてきました。
| ワクチン種類 | 1回目から2回目までの間隔 | 推奨される接種時期 | 有効性発現時期 |
|---|---|---|---|
| mRNAワクチン | 3-4週間 | 午前中 | 2回目接種後7日 |
| 組換えタンパク | 4週間 | 制限なし | 2回目接種後14日 |
| 従来型不活化 | 4週間 | 制限なし | 2回目接種後14日 |
医療機関での接種実績から、副反応への対応を考慮して午前中の接種が推奨されており、特に高齢者や基礎疾患保有者には、体調管理がしやすい時間帯の選択が望ましいとされています。
追加接種(ブースター)のガイドライン
2023年の最新データによると、追加接種による抗体価の上昇は、オミクロン株を含む変異株に対しても有効な防御力を付与することが判明しています。
| 接種回数 | 前回接種からの間隔 | 対象年齢 | 期待される効果持続期間 |
|---|---|---|---|
| 3回目 | 5か月以上 | 12歳以上 | 4-6か月 |
| 4回目 | 5か月以上 | 60歳以上 | 3-5か月 |
| 5回目 | 3か月以上 | 65歳以上 | 3-4か月 |
季節性と流行状況を考慮した接種
感染症サーベイランスデータによると、新型コロナウイルスの流行には明確な季節性パターンが認められます。2021年から2023年の統計では、12月から2月にかけて感染者数が増加する傾向が顕著です。
| 季節 | 感染リスク | 推奨される対応 | 接種優先度 |
|---|---|---|---|
| 冬季(12-2月) | 非常に高い | 早期接種推奨 | 最優先 |
| 夏季(6-8月) | 中程度 | 状況に応じて | 中程度 |
| 春秋(3-5月,9-11月) | 変動的 | 個別判断 | 状況依存 |
個人の健康状態に応じた接種計画
臨床現場での知見によれば、基礎疾患を持つ方々の接種計画には特別な配慮が必要です。免疫抑制剤使用者では、薬剤の投与タイミングと接種日程の調整が重要となります。
医療機関での接種計画立案時の重要事項:
- 抗凝固薬使用者:投与量調整の要否確認
- 免疫抑制剤使用者:薬剤投与スケジュールとの調整
- 化学療法実施中の患者:治療サイクルに合わせた計画立案
最適な接種計画の策定には、個人の健康状態、生活環境、感染リスクなど、多角的な視点からの評価が不可欠となっています。

次世代mRNAワクチン(レプリコン)
レプリコンmRNAワクチンは、従来のmRNAワクチンの進化形として注目を集める革新的な技術です。
自己増殖能を持つRNAを用いることで、より少ない投与量で持続的な免疫応答を引き起出すことが可能となり、次世代のワクチン開発における重要な技術基盤となっています。
レプリコンmRNAワクチンの基本原理と革新性
レプリコンmRNAワクチンは、アルファウイルス(トガウイルス科に属するRNAウイルス)の複製機構を巧みに応用した画期的なワクチン技術として、2020年以降、世界的な注目を集めています。
| 構成要素 | 機能と特徴 |
|---|---|
| 複製酵素遺伝子 | RNA依存性RNAポリメラーゼによる自己複製 |
| 抗原タンパク質遺伝子 | SARS-CoV-2スパイクタンパク質などの産生 |
| 制御配列 | サブゲノミックプロモーターによる発現調節 |
従来型のmRNAワクチンと比較して、レプリコン技術では投与量を約1/100まで削減できることが、2022年の前臨床試験で実証されました。
このような少量投与でも十分な効果が得られる理由は、細胞質内での自己複製メカニズムにあります。
従来のmRNAワクチンとレプリコン技術の比較
2023年に発表された複数の研究データによると、レプリコンmRNAワクチンは従来型と比べて顕著な優位性を示しています。
- 投与量は従来の1/50から1/100で同等以上の効果を発揮
- 抗原タンパク質の発現期間が2週間以上持続
- 中和抗体価が従来型の2〜5倍に上昇
- 発熱などの副反応が30%程度減少
| 評価項目 | 従来型mRNA | レプリコンmRNA |
|---|---|---|
| 必要投与量 | 30-100µg | 0.3-1µg |
| 抗原発現期間 | 2-3日 | 14-21日 |
| 中和抗体価上昇 | 基準値 | 2-5倍 |
レプリコンワクチンの免疫応答メカニズム
レプリコンワクチンの特徴的な免疫応答は、細胞内での持続的な抗原発現と、自然免疫系の活性化の相乗効果によって生み出されます。
| 免疫応答の種類 | 誘導される効果と持続期間 |
|---|---|
| 液性免疫 | 中和抗体が6ヶ月以上持続 |
| 細胞性免疫 | メモリーT細胞が1年以上維持 |
| 自然免疫 | Type-I IFNが2週間持続 |
米国立衛生研究所(NIH)の2023年の研究では、レプリコンワクチン接種後の免疫応答が12ヶ月以上持続することが確認されました。
レプリコン技術の臨床応用と将来展望
現在、世界中で20以上の臨床試験が進行中であり、特に注目すべき応用分野として以下が挙げられます。
- 新型コロナウイルスの変異株に対する広範な防御効果
- 固形がんを標的としたがん免疫療法への展開
- 自己免疫疾患における免疫寛容の誘導
Phase I/II臨床試験では、従来型ワクチンと比較して有意に高い免疫原性と、良好な安全性プロファイルが示されています。
レプリコンmRNAワクチンは、次世代の予防医療における革新的な技術として、さらなる発展が期待されています。
以上