呼吸器疾患の一種である透過性亢進型肺水腫(とうかせいこうしんがたはいすいしゅ)とは肺の毛細血管壁の透過性が異常に亢進して血液中の水分や蛋白質が肺胞内に漏出する深刻な病態です。
この状態により肺組織に過剰な水分が蓄積し、ガス交換が阻害されることで呼吸機能が著しく低下します。
原因は多岐にわたる症肺炎、敗血症、重度外傷、薬物中毒などが挙げられますが、時に原因不明の場合もあるのが現状です。
主な症状として進行性の呼吸困難、低酸素血症、泡沫状の喀痰などが現れますが、症状の程度には個人差があります。
透過性亢進型肺水腫の主症状
進行性呼吸困難
透過性亢進型肺水腫の最も顕著かつ深刻な症状は進行性の呼吸困難です。
この症状は肺胞内に過剰な水分が蓄積することで引き起こされ、患者さんは次第に増強する息苦しさに悩まされることになります。
初期段階では軽度の息切れとして現れることがありますが、病態の進行に伴い安静時でも強い息苦しさを感じるようになり、日常生活に著しい支障をきたす可能性もあるのです。
| 呼吸困難の程度 | 特徴 | 患者さんの体験 |
| 軽度 | 労作時のみの息切れ | 階段を上がるときに息が切れる |
| 中等度 | 日常生活動作での息切れ | 着替えや歩行で息苦しさを感じる |
| 重度 | 安静時でも持続する息苦しさ | 座っているだけでも呼吸が苦しい |
患者さんの言葉:「最初は少し息が切れる程度でしたが、徐々に息苦しさが強くなり、今では横になっていても呼吸が辛いです。」
低酸素血症
低酸素血症は透過性亢進型肺水腫において最も重要な症状の一つです。
この症状は肺胞でのガス交換障害により引き起こされ、血液中の酸素濃度が低下することで生じます。
患者さんは皮膚や粘膜のチアノーゼ、意識レベルの低下、頻脈などの症状を呈することがありますが、初期段階では自覚症状に乏しいことがあり、その進行に気づきにくいのも特徴です。
低酸素血症の進行は以下のような症状を引き起こす可能性があります。
- 軽度の錯乱や不安:思考が明瞭でなくなる感覚
- 頭痛:持続的で鈍い痛みを感じる
- 疲労感の増強:日常的な活動でも極度の疲れを感じる
- 運動耐容能の低下:少しの動作でも息切れが生じる
医療者の観察ポイント:「患者さんの皮膚色や爪床の色調変化、呼吸数の増加、脈拍の変動に注意を払い、低酸素血症の早期発見に努めます。」
特徴的な咳嗽と痰
透過性亢進型肺水腫では特徴的な咳嗽と痰の症状が現れることがあり、これらは病態の進行を示す重要な指標となります。
咳嗽は通常断続的で湿性であり、ピンク色の泡沫状の痰を伴うこともあるでしょう。
この泡沫状の痰は肺胞内に漏出した蛋白質を含む液体が気道内で攪拌されることで生じ、肺水腫の重症度を反映します。
| 痰の性状 | 意味 | 臨床的意義 |
| 透明 | 軽度の肺水腫 | 初期段階での介入が可能 |
| ピンク色 | 中等度~重度の肺水腫 | 迅速な対応が必要 |
| 血性 | 重度の肺障害の可能性 | 緊急の治療介入が不可欠 |
医療者の洞察:「痰の性状変化は病態の進行を示す重要なサインです。定期的な観察と記録が患者さんの状態把握に役立ちます。」
全身症状
透過性亢進型肺水腫では肺症状だけでなく全身にわたる症状が現れることがあり、これらは疾患の全身性の影響を示す重要な指標となります。
これらの症状は低酸素血症や全身性の炎症反応に起因することが多く、患者さんの全身状態を反映する貴重な情報源となるのです。
代表的な全身症状には以下のようなものがあります。
- 発熱:炎症反応の亢進を示唆
- 全身倦怠感:エネルギー代謝の障害を反映
- 食欲不振:全身状態の悪化のサイン
- 筋力低下:長期的な影響の現れ
患者さんの体験:「熱が出て体がだるく、食事も喉を通らない状態が続いています。日に日に体力が落ちていくのを感じます。」
心血管系症状
透過性亢進型肺水腫は心血管系にも重大な影響を及ぼすことがあり、これらの症状は疾患の進行と予後を左右する重要な因子となります。
低酸素血症や肺高血圧症の進行によって心臓に過度の負荷がかかり、様々な心血管系の症状が現れる可能性も生じるでしょう。
| 症状 | 機序 | 長期的影響 |
| 頻脈 | 低酸素血症への代償反応 | 心筋疲労のリスク増大 |
| 胸痛 | 心筋虚血や右心負荷 | 心筋梗塞のリスク上昇 |
| 末梢浮腫 | 右心不全の進行 | 腎機能障害の可能性 |
医療者の注意点:「心血管系症状の出現は、疾患の重症化を示唆します。心エコー検査や血液検査などを用いて、心機能を定期的に評価することが重要です。」
透過性亢進型肺水腫の主症状を理解し、その微妙な変化を捉えることは、早期発見と適切な対応のために不可欠です。
透過性亢進型肺水腫の多面的原因とトリガー
肺胞-毛細血管バリアの破綻
透過性亢進型肺水腫の発症機序の中核に位置するのが肺胞-毛細血管バリアの機能障害です。
このバリアは肺の生理的機能維持において極めて重要な役割を果たしており、通常は血液中の成分が肺胞腔内に漏出するのを防ぐ精巧な防御機構として機能しています。
しかし様々な病態生理学的要因によってこのバリアが破綻すると、血漿成分が肺胞内に過剰に漏出して肺水腫が引き起こされることになるのです。
| バリアの構成要素 | 主な機能 | 障害時の影響 |
| 肺胞上皮細胞 | ガス交換の場を提供 | ガス交換障害 |
| 毛細血管内皮細胞 | 血液成分の漏出を防止 | 血漿漏出増加 |
| 基底膜 | 構造的サポートを提供 | バリア強度低下 |
このバリアの破綻は単一の要因ではなく複数の因子が複雑に絡み合って生じる現象であり、その理解には多面的なアプローチが必要となります。
直接的肺障害
直接的肺障害は透過性亢進型肺水腫を引き起こす主要な原因の一つであり、肺組織に直接的な損傷を与えることで肺胞-毛細血管バリアの機能を著しく低下させるでしょう。
この種の障害は局所的な炎症反応や組織損傷を引き起こし、バリアの構造的・機能的完全性を破壊します。
直接的肺障害の代表的な原因には以下のようなものがあり、それぞれ特有の病態生理学的メカニズムを有するのです。
- 重症肺炎(細菌性、ウイルス性):病原体の直接的な細胞傷害と過剰な免疫応答
- 誤嚥(胃酸や異物の吸引):化学的・物理的刺激による上皮細胞の損傷
- 有毒ガスの吸入:化学物質による直接的な細胞毒性
- 高濃度酸素療法による酸素毒性:活性酸素種の過剰産生
これらの要因は肺胞上皮細胞や毛細血管内皮細胞に直接的なダメージを与え、細胞間接着の破綻や細胞死を引き起こし、結果としてバリア機能の破綻を導きます。
間接的肺障害
間接的肺障害は全身性の炎症反応や循環障害に伴って二次的に肺が障害を受けるメカニズムを指し、直接的には肺に作用しない要因によっても透過性亢進型肺水腫を引き起こす可能性があります。
この種の障害では全身性の炎症カスケードが活性化され、その影響が肺循環にも及ぶことで肺障害が生じるのです。
| 原因カテゴリー | 具体例 | 主な病態生理学的メカニズム |
| 敗血症 | 重症感染症、菌血症 | サイトカインストーム、好中球活性化 |
| 外傷 | 多発性外傷、熱傷 | 全身性炎症反応症候群(SIRS) |
| 循環障害 | ショック、大量輸血 | 微小循環障害、虚血再灌流障害 |
間接的肺障害の場合は全身の炎症性メディエーターや活性化された好中球が肺循環に到達し、肺毛細血管内皮細胞を障害することで透過性が亢進します。
このプロセスには接着分子の発現増加、血管内皮細胞の収縮、好中球の血管外遊走などの複雑な分子メカニズムが関与しているのです。
医原性要因
医療行為自体が透過性亢進型肺水腫のトリガーとなることがあり、これを医原性要因と呼びます。
これらの要因は意図せずして肺に対して追加的なストレスや障害を与える可能性があり、その分子メカニズムの理解は予防策の開発において重要です。
代表的な医原性要因とその分子メカニズムには以下のようなものがあります。
- 人工呼吸器関連肺損傷(VILI):機械的ストレスによる肺胞上皮細胞の変形と炎症性サイトカインの産生
- 輸血関連急性肺障害(TRALI):輸血製剤中の抗体と受容者の好中球の相互作用による肺毛細血管内皮細胞の障害
- 薬剤性肺障害:薬物代謝産物による直接的な細胞毒性や過敏反応
- 心肺バイパス後症候群:体外循環による全身性炎症反応と補体活性化
| 医原性要因 | 発生メカニズム | 分子レベルでの影響 |
| VILI | 過度の肺胞の伸展・虚脱 | メカノトランスダクションによる炎症性遺伝子の発現亢進 |
| TRALI | 輸血製剤中の抗体反応 | 好中球-内皮細胞相互作用の増強、活性酸素種の産生 |
これらの医原性要因の理解は、より安全な医療実践の開発と実施に不可欠です。
素因と環境要因
透過性亢進型肺水腫の発症リスクと経過には個人の素因や環境要因も重要な役割を果たします。
これらの要因は直接的な原因とはならないものの、疾患の感受性や重症度に影響を与える可能性があり、その理解には遺伝子-環境相互作用の観点が不可欠です。
素因としては以下のような要素が考えられます。
- 遺伝的多型:炎症関連遺伝子や細胞接着分子遺伝子の変異
- 既存の肺疾患:慢性閉塞性肺疾患(COPD)や間質性肺疾患の存在
- 免疫系の個体差:自己免疫疾患の有無や免疫応答の個人差
環境要因として挙げられる要素は以下の通りです。
- 大気汚染:微小粒子状物質(PM2.5)などによる慢性的な肺の炎症
- 職業性曝露:シリカやアスベストなどの粉塵による肺組織の慢性的損傷
- 生活習慣:喫煙や過度のアルコール摂取による肺の脆弱化
これらの素因と環境要因が複雑に絡み合うことで個人の透過性亢進型肺水腫に対する感受性が決定されると考えられています。
| 要因カテゴリー | 具体例 | 影響メカニズム |
| 遺伝的素因 | 炎症関連遺伝子多型 | 炎症反応の個人差 |
| 環境要因 | 大気汚染物質曝露 | 酸化ストレスの慢性的増加 |
透過性亢進型肺水腫の原因とトリガーを理解することは予防と早期介入のために不可欠です。
多様な要因が複雑に相互作用し合う中で個々の患者さんのリスク因子を適切に評価し、個別化された予防策を講じることが重要でしょう。
炎症性カスケードの役割
透過性亢進型肺水腫の発症と進行において炎症性カスケードは中心的な役割を果たします。
この過程では様々な炎症性メディエーターが複雑なネットワークを形成し、肺胞-毛細血管バリアの破綻を促進するのです。
主要な炎症性メディエーターとその作用には以下のようなものがあります。
- サイトカイン(TNF-α、IL-1β、IL-6など):血管内皮細胞の活性化と透過性亢進
- ケモカイン(IL-8、MCP-1など):好中球やマクロファージの遊走促進
- プロスタグランジン:血管拡張と炎症促進
- 活性酸素種(ROS):直接的な細胞障害と炎症シグナルの増幅
| メディエーター | 主な作用 | 臨床的意義 |
| TNF-α | 血管透過性亢進 | 早期の肺水腫形成 |
| IL-8 | 好中球遊走 | 持続的な肺障害 |
| ROS | 酸化ストレス | 組織障害の増悪 |
これらの炎症性メディエーターの相互作用を理解することは新たな治療標的の同定や、より効果的な抗炎症療法の開発につながる可能性があります。
修復メカニズムと線維化
透過性亢進型肺水腫後の肺組織の運命を決定づける重要な要素として、修復メカニズムと線維化プロセスがあります。
これらのプロセスは肺機能の回復に寄与する一方で過剰な場合には肺の線維化を引き起こし、長期的な肺機能障害につながる可能性があるのです。
修復プロセスの主な要素は以下のようなものです。
- 上皮細胞の再生と分化
- 血管新生
- 細胞外マトリックスの再構築
一方、線維化プロセスには以下の要素が関与しています。
- 筋線維芽細胞の活性化
- コラーゲンなどの細胞外マトリックス成分の過剰産生
- 組織リモデリングの異常
| プロセス | 正常修復時の役割 | 過剰反応時のリスク |
| 上皮再生 | バリア機能の回復 | 異常な上皮化 |
| 線維芽細胞活性化 | 組織の強度回復 | 過剰な線維化 |
これらのプロセスのバランスを適切に制御することが透過性亢進型肺水腫後の長期的な肺機能予後の改善につながる可能性となるのです。
透過性亢進型肺水腫の原因とトリガーは単一の要因ではなく、複雑に絡み合った多因子的なプロセスであることが明らかになっています。
透過性亢進型肺水腫の診察と診断
初期評価:迅速かつ系統的な状態把握
透過性亢進型肺水腫の診察と診断プロセスは患者さんの状態を迅速かつ正確に把握することから始まるのです。
まず患者さんの全身状態を素早く評価し、呼吸状態の悪化の程度を判断します。
この初期評価にはバイタルサインの測定、視診、聴診、触診などの基本的な身体診察が含まれ、これらは国際的なガイドラインに基づいて実施されます。
| 評価項目 | 観察ポイント | 臨床的意義 |
| 呼吸数 | 頻呼吸の有無 | 呼吸不全の重症度評価 |
| 酸素飽和度 | 低酸素血症の程度 | 酸素化障害の定量化 |
| 血圧 | ショック状態の評価 | 循環動態の安定性確認 |
| 意識レベル | 低酸素による影響 | 脳機能への影響評価 |
初期評価の結果に基づいて追加の検査や緊急処置の必要性が判断されるでしょう。
問診:エビデンスに基づく詳細な病歴聴取
患者さんやご家族からの詳細な病歴聴取は透過性亢進型肺水腫の診断において不可欠であり、エビデンスに基づいた系統的なアプローチが求められます。
この段階で症状の発症時期や経過、既往歴、薬剤使用歴、職業歴などを丁寧に聴取し、リスク因子の特定を探るのです。
特に次の点に注目して問診を行います。
- 呼吸困難の進行速度と程度(mMRC呼吸困難スケールの活用)
- 発熱や咳嗽の性状と持続期間
- 最近の手術や外傷の既往(時期と詳細)
- 職業や趣味による有害物質への曝露歴(具体的な物質と曝露期間)
- 最近の渡航歴や感染症患者との接触歴
これらの情報は透過性亢進型肺水腫の原因特定や重症度評価、さらには予後予測にも重要な役割を果たすのです。
身体診察:エビデンスに基づく系統的アプローチ
透過性亢進型肺水腫の診断にはエビデンスに基づいた系統的な身体診察が重要です。特に呼吸器系と循環器系に焦点を当てた詳細な診察を行い、客観的な所見を記録します。
| 診察項目 | 観察内容 | 臨床的意義 |
| 視診 | 呼吸補助筋の使用、チアノーゼ | 呼吸不全の重症度評価 |
| 聴診 | 湿性ラ音、心音異常 | 肺水腫の程度と心機能評価 |
| 触診 | 頸静脈怒張、下腿浮腫 | 右心不全の評価 |
| 打診 | 胸水の有無 | 肺水腫の合併症評価 |
身体診察の結果は透過性亢進型肺水腫の重症度評価や他の疾患との鑑別に有用な情報を提供し、さらなる検査の必要性を判断する基準となるのです。
画像検査:最新技術を用いた肺水腫の可視化
画像検査は透過性亢進型肺水腫の診断において中心的な役割を果たし、近年の技術進歩によってより精密な評価が可能となっています。
胸部X線検査が最初に行われることが多く、両側性の浸潤影や肺血管陰影の増強などの特徴的な所見を示すのです。
胸部CT検査ではより詳細な肺実質の評価を可能にし、肺水腫の分布や程度を正確に把握するのに役立つでしょう。
最新の画像診断技術の活用は次の通りです。
- 高分解能CT(HRCT):微細な肺実質変化の評価
- デュアルエナジーCT:肺血流評価と肺水腫の鑑別
- 肺超音波検査:ベッドサイドでの迅速な評価
これらの画像所見は透過性亢進型肺水腫の診断確定や他の肺疾患との鑑別に重要であり、経時的な変化の追跡にも有用です。
血液検査:包括的バイオマーカー評価
血液検査は透過性亢進型肺水腫の原因検索や全身状態の評価に不可欠であり、最新のバイオマーカーを含む包括的な評価が行われます。
以下のような検査項目を組み合わせて多角的な評価を行うのが一般的です。
| 検査項目 | 評価内容 | 臨床的意義 |
| 動脈血ガス分析 | 低酸素血症の程度 | 呼吸不全の重症度評価 |
| 炎症マーカー(CRP、プロカルシトニン) | 全身性炎症の評価 | 感染性要因の鑑別 |
| 心筋マーカー(BNP、トロポニン) | 心原性肺水腫の鑑別 | 心機能評価 |
| 電解質、腎機能 | 代謝異常の評価 | 全身状態の把握 |
| 凝固系マーカー(D-ダイマー) | 血栓塞栓症の評価 | 合併症リスクの評価 |
これらの検査結果は透過性亢進型肺水腫の重症度評価や治療方針の決定に重要な役割を果たし、予後予測にも活用されます。
鑑別診断:高度な診断技術を用いた精密な評価
透過性亢進型肺水腫の確定診断には類似した症状を呈する他の疾患との鑑別が重要です。
以下のような疾患を考慮しながら最新の診断技術を駆使して精密な鑑別を行います。
- 心原性肺水腫:BNP値、心エコー検査による評価
- 肺炎:胸部CT所見、微生物学的検査
- 急性呼吸窮迫症候群(ARDS):ベルリン定義に基づく評価
- 過敏性肺炎:詳細な曝露歴、特異的IgG抗体検査
鑑別診断には上記の診察・検査に加えて、以下のような高度な検査が考慮されるでしょう。
- 経食道心エコー検査:詳細な心機能評価
- 気管支肺胞洗浄(BAL):細胞分画や微生物学的評価
- 遺伝子検査:特定の遺伝性疾患の除外
総合的評価:多職種チームによるアプローチ
透過性亢進型肺水腫の診断プロセスは単一の検査や所見だけでなく、多角的な評価に基づいて行われます。
呼吸器専門医、集中治療医、放射線科医、臨床検査技師など多職種医療チームが協力して、患者さんの状態を総合的に評価するのです。
このアプローチにより、以下のような利点が得られます。
- 診断精度の向上
- 迅速な意思決定
- 個別化された治療計画の立案
- 合併症リスクの早期特定
多職種チームは定期的なカンファレンスを通じて情報を共有し、最新のエビデンスに基づいた診断アプローチを常に更新します。
患者中心の診断プロセス
透過性亢進型肺水腫の診察と診断プロセスにおいて患者さんとそのご家族の理解と協力は不可欠です。
医療者は診断の各段階で適切な説明を行い、インフォームドコンセントを得ながら検査や処置を進めます。
このプロセスには以下のような要素が含まれます。
- 診断プロセスの詳細な説明
- 各検査の目的と予想される結果の解説
- 患者さんの価値観や希望の尊重
- 診断結果に基づく今後の方針についての理解
患者さん中心のアプローチにより診断プロセスへの患者さんの積極的な参加が促され、治療への理解と協力が得られやすくなるでしょう。
透過性亢進型肺水腫の診察と診断はエビデンスに基づく包括的なアプローチと最新の医療技術の活用により高い精度と効率性を実現しています。
画像所見
胸部X線検査
透過性亢進型肺水腫の画像診断において胸部X線検査は最初に行われる基本的かつ重要な検査です。
この検査では肺野全体の状態を俯瞰的に評価することができ、迅速な初期診断に役立ちます。
典型的な所見として観察されるのは両側性のびまん性浸潤影です。また、肺血管陰影の増強や心陰影の拡大なども観察されることがあります。
| 所見 | 特徴 | 臨床的意義 |
| 浸潤影 | 両側性、びまん性 | 肺水腫の存在を示唆 |
| 肺血管陰影 | 増強 | 肺うっ血の程度を反映 |
| 心陰影 | 拡大の有無 | 心原性要因の評価 |
しかし胸部X線検査には分解能の限界があり、早期や軽度の肺水腫を見逃す可能性もあるため注意が必要です。
胸部CT検査
胸部CT検査は透過性亢進型肺水腫の診断において、より詳細かつ正確な情報を提供します。
高分解能CT(HRCT)や最新のデュアルエナジーCTを用いることで肺実質の微細な変化を捉え、肺水腫の程度や分布をより精密に評価することが可能です。
特徴的な所見には以下のようなものがあります。
- すりガラス影:肺胞内の部分的な液体貯留を反映
- 小葉間隔壁の肥厚:間質性浮腫の存在を示唆
- 胸水貯留:水分バランスの異常を反映
- モザイクパターン:肺血流の不均等分布を示唆
これらの所見は肺水腫の程度や分布を評価する上で重要な指標となり、他疾患との鑑別にも有用です。
| CT所見 | 意味 | 鑑別に役立つポイント |
| すりガラス影 | 肺胞性浮腫 | 分布パターン、均一性 |
| 小葉間隔壁肥厚 | 間質性浮腫 | 網状影の程度、分布 |
| 胸水 | 水分貯留 | 量、両側性の有無 |
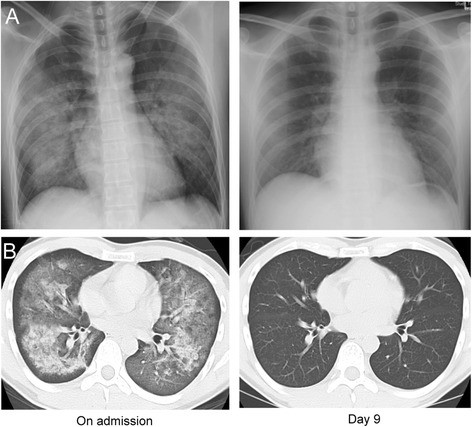
所見:(A) 入院時(左)には両側中枢側優位のの浸潤影が認められ、いわゆる”Butterfly shadow”を呈している。入院9日目(右)には完全に消失した。(B) 入院時(左)には、両側にまだら状の区域性陰影とすりガラス影が認められ、末梢領域は保たれていた。入院9日目には、これらの影が完全に消失した(右)。
肺超音波検査
近年、透過性亢進型肺水腫の診断と経過観察において肺超音波検査の有用性が高く評価されています。
この検査はベッドサイドで迅速に実施できて放射線被曝のリスクもないため頻回の評価が可能です。
| 所見 | 意味 | 定量化の方法 |
| B-line | 肺間質の水分増加 | 数のカウント、分布評価 |
| 胸水 | 水分貯留の程度 | 深さの測定、性状評価 |
| 肺滑走サイン | 胸膜の動き | 動画モードでの観察 |
B-lineの数や分布を評価することで肺水腫の程度を推定して治療効果のモニタリングにも活用できます。
さらに最新の人工知能(AI)技術を用いた画像解析によって、より客観的かつ精密な評価が可能になりつつあるのです。
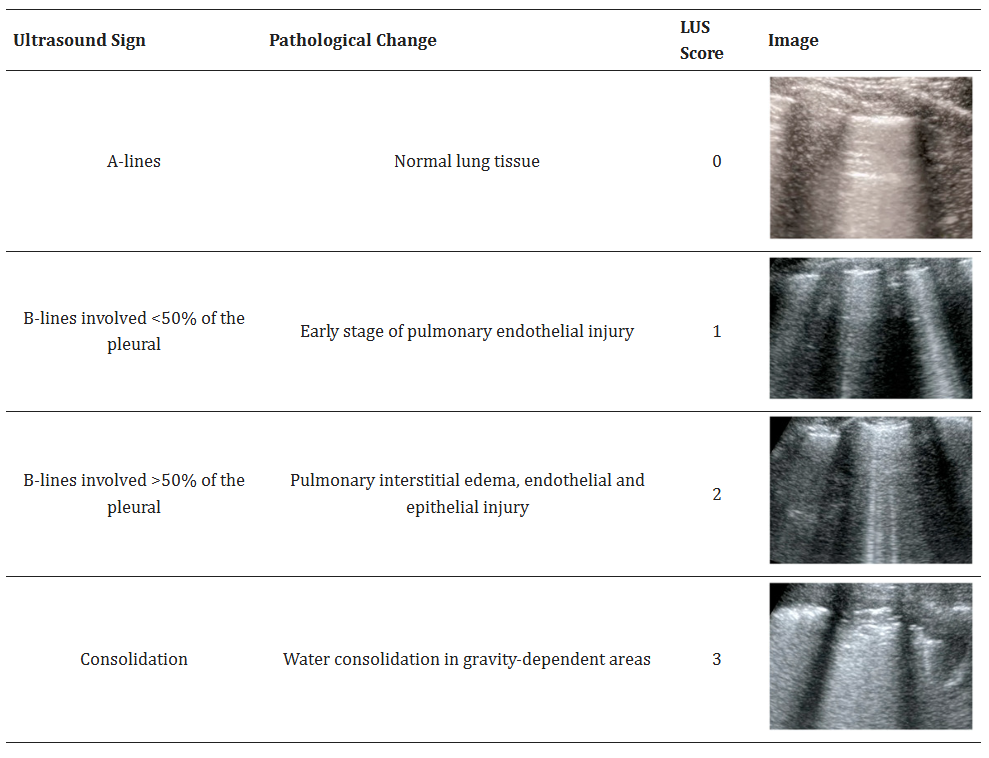
所見:A-lines: 正常な肺組織に見られる。B-lines: 胸膜の<50%に認める: 肺内皮障害の初期段階を示す。胸膜の>50%に認める: 肺間質浮腫、内皮および上皮の損傷を示す。区域性陰影: 重力依存領域における水分の区域性陰影を示す。
画像所見の経時的変化
透過性亢進型肺水腫の画像所見は病態の進行や改善に伴って刻々と変化します。この変化を詳細に追跡することで治療効果の評価や予後予測に役立てることができるでしょう。
病態の進行に伴う変化は以下の通りです。
- 初期段階:
- わずかなすりガラス影
- 軽度の小葉間隔壁肥厚
- 進行期:
- すりガラス影の拡大と濃度上昇
- 小葉間隔壁肥厚の顕在化
- 胸水量の増加
- 重症期:
- 広範なコンソリデーション(濃厚影)
- 著明な胸水貯留
- 気管支血管束の肥厚
一方、改善期にはこれらの所見が徐々に消退していきます。
経時的な画像評価によって治療への反応性や回復の速度を客観的に評価することが可能なのです。
鑑別を要する画像所見
透過性亢進型肺水腫の画像所見は他の肺疾患と類似することがあるため慎重かつ精密な鑑別が必要です。
最新の画像解析技術や人工知能を活用することで、より精度の高い鑑別診断が可能になっています。
| 疾患 | 類似点 | 相違点 | 鑑別のためのテクニック |
| 心原性肺水腫 | びまん性浸潤影 | 血管陰影の分布 | 肺血管の重力勾配評価 |
| 間質性肺炎 | すりガラス影 | 分布パターン | 詳細な小葉構造の分析 |
| ARDS | びまん性浸潤影 | 進行速度、均一性 | 経時的変化の評価 |
画像所見のみならず臨床情報や他の検査結果を総合的に評価することが重要です。
最新のマルチモダリティ画像解析技術を用いることで各種画像検査の情報を統合し、より精密な診断が可能となっています。
最新の画像技術と解析手法を適切に活用することで、より正確な診断と経過観察が可能となって患者さん一人ひとりに最適な医療を提供することができます。
エビデンスに基づく最新の治療戦略と回復への道のり
急性期の呼吸管理:生命維持と肺保護の両立
透過性亢進型肺水腫の治療において最も重要かつ緊急性の高いのは急性期の呼吸管理です。
この管理は低酸素血症の改善と同時に、人工呼吸器関連肺損傷(VILI)の予防を目指す複雑なバランスの上に成り立っています。
| 呼吸管理の方法 | 適応 | 特徴と注意点 |
| 高流量鼻カニュラ酸素療法 | 軽度~中等度の低酸素血症 | 快適性が高く、気道陽圧効果あり |
| 非侵襲的人工呼吸 | 中等度の呼吸不全 | マスク装着による皮膚障害に注意 |
| 侵襲的人工呼吸 | 重度の呼吸不全 | 肺保護戦略の厳密な実施が必要 |
| 体外式膜型人工肺(ECMO) | 従来の人工呼吸で改善しない最重症例 | 専門的な管理と合併症リスクあり |
人工呼吸器管理では最新のエビデンスに基づく肺保護戦略が採用されます。
具体的には低一回換気量(4-8 mL/kg予測体重)、適切なPEEP設定、プラトー圧制限(≤30 cmH2O)などが実施されます。
これによりVILIのリスクを最小限に抑えつつ適切な酸素化と二酸化炭素除去を目指すのです。
薬物療法:病態生理に基づく多角的アプローチ
透過性亢進型肺水腫の薬物療法は病態生理の理解に基づいて多角的に行われ、最新の研究成果を反映して常に更新されています。
主な薬物療法にはそれぞれ特定の病態メカニズムを標的とした以下のようなものがあるのです。
- 利尿薬:肺うっ血の軽減(ループ利尿薬が主体)
- 血管拡張薬:肺循環の改善(一酸化窒素吸入療法など)
- ステロイド薬:炎症の抑制(使用の是非は議論あり)
- 抗凝固薬:血栓予防(ヘパリンなど)
- 免疫調節薬:過剰な炎症反応の制御(研究段階)
これらの薬物は患者さんの状態、原因疾患、合併症リスクなどを総合的に評価して選択され、適切な用量で投与されます。
| 薬剤分類 | 主な作用 |
| 利尸薬 | 体内水分量の調整 |
| 血管拡張薬 | 肺血管抵抗の低下 |
| ステロイド薬 | 炎症抑制 |
| 抗凝固薬 | 血栓形成予防 |
薬物療法の効果は定期的に評価され、必要に応じて用量調整や薬剤変更が行われるでしょう。
原因疾患への対応:個別化医療の実践
透過性亢進型肺水腫の治療では原因となっている疾患や状態への迅速かつ的確な対応が不可欠です。
この過程はまさに個別化医療の実践であり、各患者さんの病態に応じたテーラーメイドの治療アプローチが求められます。
原因疾患への対応例は次の通りです。
- 感染症:適切な抗菌薬治療(培養結果に基づく選択)
- 自己免疫疾患:免疫抑制療法(疾患活動性に応じた調整)
- 薬剤性:被疑薬の中止と代替療法の検討
- 外傷後:早期の手術的介入と全身管理
原因疾患の特定と治療は肺水腫の改善と再発予防に直結するため、多職種医療チームによる総合的なアプローチが重要です。
| 原因カテゴリー | 治療アプローチ | 期待される効果 |
| 感染症 | 抗菌薬療法 | 炎症の鎮静化 |
| 自己免疫疾患 | 免疫抑制療法 | 過剰免疫反応の制御 |
| 薬剤性 | 原因薬剤の中止 | 薬剤性肺障害の改善 |
栄養管理と全身ケア:回復を加速する包括的アプローチ
透過性亢進型肺水腫の治療では呼吸管理や薬物療法と並んで栄養管理と全身ケアも極めて重要な要素になります。
これらは患者さんの回復力を最大化し、合併症リスクを最小化する上で不可欠です。
栄養管理
- エネルギー必要量の適切な算定(間接熱量計の使用が望ましい)
- タンパク質摂取の最適化(1.2-2.0 g/kg/日)
- 経腸栄養の早期開始(腸管機能が維持されている場合)
全身ケア
- 体位管理:腹臥位療法の検討(重症例)
- 早期リハビリテーション:ICU-acquired weaknessの予防
- 鎮静管理:日中覚醒を目指したプロトコル
- 精神的サポート:せん妄予防と長期的な精神健康ケア
これらの包括的なケアは患者さんの全身状態の改善、在院日数の短縮、そして長期的な生活の質の向上に貢献します。
治癒までの期間
透過性亢進型肺水腫の治癒までの期間は患者さんの年齢、基礎疾患、重症度、そして原因疾患によって大きく異なり、画一的な予測は困難です。
一般的な経過としては以下のようなタイムラインが想定されますが、個別性が高いことを強調しておく必要があります。
| 重症度 | 急性期治療期間 | リハビリ期間 | 総回復期間 |
| 軽症 | 3-7日 | 1-2週間 | 2-4週間 |
| 中等症 | 1-2週間 | 2-4週間 | 1-3ヶ月 |
| 重症 | 2-4週間以上 | 1-3ヶ月 | 3-6ヶ月以上 |
治癒の判断は以下の要素を総合的に評価して行われます。
- 臨床症状の改善(呼吸困難感の消失など)
- 画像所見の正常化(胸部X線やCTでの浸潤影の消失)
- 血液検査値の正常化(炎症マーカーの低下など)
- 肺機能検査の改善(特に拡散能の回復)
長期フォローアップの重要性
急性期を脱した後も定期的な外来フォローアップが重要です。
肺機能の完全回復には時間を要する場合があり、また、長期的な合併症(肺線維症など)のモニタリングも必要となります。
さらに身体面だけでなく認知機能や精神面のケアも含めた包括的なアプローチが求められるでしょう。
透過性亢進型肺水腫の治療は急性期の呼吸管理から始まり、薬物療法、原因疾患への対応、全身管理を包括的に行う複雑なプロセスです。
最新のエビデンスに基づく治療戦略と個々の患者さんの状態に応じた細やかな対応が、治療成功の鍵となります。
治療期間は個人差が大きいものの、適切な治療と管理により多くの患者さんで回復が期待できるでしょう。
治療に伴う副作用とリスク
人工呼吸器関連合併症
透過性亢進型肺水腫の治療において人工呼吸器は生命維持に不可欠な手段ですが、同時に複雑な合併症リスクを伴います。
これらのリスクを理解して適切に管理することが、患者さんの予後改善において極めて重要です。
人工呼吸器関連肺損傷(VILI)は過度の肺胞の伸展や虚脱の繰り返しによって引き起こされる可能性があります。これにより肺の炎症がさらに悪化して回復を遅らせる事態も考えられるのです。
| 合併症 | 発生機序 | 予防策 |
| VILI | 過度の肺胞伸展 | 肺保護戦略(低一回換気量、適切なPEEP) |
| 人工呼吸器関連肺炎 | 気管内チューブによる感染 | 半座位、口腔ケア、早期抜管 |
| 気道損傷 | チューブによる機械的刺激 | 適切なカフ圧管理、チューブ固定位置の定期的変更 |
また、長期の人工呼吸器管理は呼吸筋の萎縮や横隔膜機能不全のリスクも伴います。
これらは人工呼吸器離脱を困難にする要因となるため、早期からのリハビリテーションが重要なのです。
薬物療法に伴う副作用
透過性亢進型肺水腫の治療に用いられる薬物にはそれぞれ特有の副作用が存在し、これらを適切に管理することが治療成功の鍵となります。
利尸薬は電解質バランスの乱れを引き起こす可能性があり、特にカリウム値の低下に注意が必要です。
低カリウム血症は不整脈のリスクを高める可能性があるため、定期的な電解質モニタリングと適切な補正が不可欠です。
ステロイド薬の使用は感染リスクの増加や血糖値の上昇、骨粗鬆症の進行などの副作用をもたらす可能性があります。特に免疫抑制作用による日和見感染のリスク増加は注意が必要です。
抗凝固薬は出血リスクを高めるため、慎重な投与と定期的なモニタリングが重要になります。特に消化管出血や頭蓋内出血などの重大な合併症に注意が必要です。
| 薬剤 | 主な副作用 | モニタリング項目 |
| 利尿薬 | 電解質異常、脱水 | 電解質値、体液バランス |
| ステロイド | 感染リスク増加、血糖上昇 | 感染徴候、血糖値 |
| 抗凝固薬 | 出血傾向 | 凝固能、出血徴候 |
これらの副作用は患者さんの全身状態に影響を与える可能性があるため、注意深い観察と迅速な対応が求められます。
栄養管理に関連するリスク
透過性亢進型肺水腫患者の栄養管理は複雑であり、適切なバランスを取ることが大切です。過剰な栄養投与は代謝負荷を増大させて二酸化炭素産生量の増加につながる可能性があります。
これは、呼吸不全の患者さんにとって望ましくない状況をもたらすことがあり、呼吸仕事量の増加や人工呼吸器離脱の遅れにつながる可能性でてくるでしょう。
一方、不十分な栄養摂取は免疫機能の低下や筋力低下を招く可能性があります。これは感染リスクの増加や回復の遅延につながる可能性生じるでしょう。
栄養管理におけるリスクと対策は次の通りです。
- 過剰栄養
- リスク:代謝負荷増大、CO2産生増加
- 対策:間接熱量測定による適切なカロリー設定、高脂肪低炭水化物食の考慮
- 不足栄養
- リスク:免疫機能低下、筋力低下
- 対策:適切なタンパク質投与、微量元素・ビタミンの補充
個々の患者さんの状態に応じた細やかな調整が必要となり、栄養サポートチーム(NST)との連携が重要です。
長期臥床に伴う合併症
透過性亢進型肺水腫の治療中、特に重症例では長期の臥床を要することがあり、これに伴い様々な二次的合併症のリスクが高まります。
以下のような合併症は患者さんの回復を遅らせる要因となり得るため早期からの積極的な対策が重要です。
| 合併症 | リスク因子 | 予防策 |
| 深部静脈血栓症 | 長期臥床、凝固能亢進 | 早期臥床、間欠的空気圧迫法、抗凝固療法 |
| 褥瘡 | 圧迫、湿潤、低栄養 | 体位変換、適切なマットレス使用、栄養管理 |
| ICU-acquired weakness | 長期人工呼吸、ステロイド使用 | 早期リハビリテーション、適切な栄養管理 |
長期臥床は筋力低下や関節拘縮のリスクも高めます。これらは人工呼吸器離脱の遅延や退院後のADL低下につながりかねないので早期から積極的なリハビリテーションが大切です。
心理的影響
透過性亢進型肺水腫の治療は患者さんに大きな心理的負担をもたらす可能性があり、この側面への配慮も治療の重要な一部です。
長期の入院や厳しい治療は不安やうつ状態を引き起こすことがあり、これらは回復過程に悪影響を及ぼす可能性があります。
特に人工呼吸器管理中の患者さんはコミュニケーション障害によるストレスを経験することがあり、適切なコミュニケーション支援が必要です。
また、集中治療後症候群(PICS)として知られる長期的な認知機能障害や精神的問題のリスクも存在し、退院後の生活にも影響を及ぼす可能性があります。
心理的影響とその対策は以下の通りです。
- 不安・うつ状態
- 対策:定期的な心理評価、必要に応じた精神科コンサルテーション
- せん妄:
- 対策:早期離床、日内リズムの維持、適切な鎮静管理
- PTSD(心的外傷後ストレス障害):
- 対策:ICU日記の活用、退院後のフォローアップ外来
これらの心理的影響は患者さんの回復過程や生活の質に大きく影響する可能性があるため、早期からの介入と長期的なフォローアップが重要です。
医原性合併症
透過性亢進型肺水腫の治療過程では様々な医療行為が必要となりますが、これらに伴う医原性合併症のリスクも存在します。
これらのリスクを認識して最小限に抑えることが安全な医療提供において不可欠です。
代表的な医原性合併症とその対策には以下のようなものがあります。
| 合併症 | 関連する医療行為 | 予防策 |
| カテーテル関連血流感染 | 中心静脈カテーテル留置 | 無菌操作の徹底、早期抜去 |
| 薬剤性肝障害 | 多剤併用 | 定期的な肝機能検査、薬剤の適正使用 |
| 造影剤腎症 | CT検査での造影剤使用 | 腎機能評価、適切な水分管理 |
これらの合併症は適切な予防策と注意深いモニタリングにより、多くの場合回避または早期に対処することが可能なのです。
長期的な肺機能障害
透過性亢進型肺水腫からの回復過程では長期的な肺機能障害が残存するリスクがあります。これは急性期の肺障害の程度や治療期間、個々の患者さんの回復力によって大きく異なるでしょう。
長期的な肺機能障害の可能性は次のようなものです。
- 拡散能の低下:ガス交換効率の永続的な低下
- 肺コンプライアンスの低下:呼吸仕事量の増加
- 気道過敏性の亢進:慢性咳嗽や喘息様症状
これらの長期的影響は患者さんの日常生活やQOLに影響を与える可能性があるため、退院後も継続的なフォローアップと必要に応じたリハビリテーションが重要となります。
透過性亢進型肺水腫の治療には生命維持のために必要不可欠な側面がある一方で、様々な副作用やリスクが存在します。
これらのリスクを包括的に理解して適切に管理することが、患者さんの総合的な回復と健康維持にとって極めて重要です。
再発リスクと予防戦略
再発リスクの多面的評価
透過性亢進型肺水腫の再発リスクは患者さんごとに大きく異なり、複数の要因が複雑に絡み合っています。
各患者さんの背景因子や初回発症時の状況を詳細に評価して最新の予測モデルを用いて再発リスクが推定されるのです。
この評価には以下のような要素が考慮されます。
| リスク因子 | 評価方法 | 重要度 |
| 基礎疾患 | 詳細な病歴聴取、専門医評価 | 高 |
| 遺伝的素因 | 遺伝子検査 | 中 |
| 環境要因 | 職歴・生活環境調査 | 高 |
| 免疫状態 | 血液検査、免疫機能評価 | 中 |
個々の患者さんに応じた精密なリスク評価が効果的かつ個別化された予防策の立案につながるのです。
生活習慣の最適化
再発予防において日々の生活習慣の最適化は極めて重要な役割を果たします。
最新の研究結果に基づき、患者さんは以下のような点に特に注意を払うことが推奨されるでしょう。
- 禁煙と受動喫煙の回避
- 肺への直接的な刺激軽減
- 炎症マーカーの低下
- 個別化された運動プログラム
- 心肺機能の強化
- 免疫系の活性化
- 抗酸化物質豊富な食事
- 酸化ストレスの軽減
- 細胞修復能力の向上
- 適切な体重管理
- 肺への負担軽減
- 全身性炎症の抑制
| 生活習慣 | 具体的な目標 | 期待される効果 |
| 運動 | 週150分の中強度有酸素運動 | 心肺機能20%向上 |
| 食事 | 1日5皿以上の野菜・果物摂取 | 酸化ストレス30%減少 |
| 体重 | BMI 18.5-24.9の維持 | 肺機能の安定化 |
これらの習慣を継続することで肺の健康維持と全身状態の改善が期待でき、再発リスクの有意な低減につながる可能性が高まります。
環境要因への先進的対策
透過性亢進型肺水腫の再発を防ぐため、環境要因への対策も最新の技術や知見を取り入れて進化しています。特に職業や趣味に関連する有害物質への曝露には、より精密な管理が求められます。
考えられる先進的な対策は以下の通りです。
- IoTを活用した職場環境のリアルタイムモニタリング
- 有害物質濃度の常時測定
- 警報システムの導入
- AI支援による個人用防護具の最適化
- 顔型や作業内容に基づくカスタマイズ
- 着用状態の自動チェック
- バイオマーカーを用いた曝露評価
- 定期的な血液・尿検査による微量曝露の検出
- 個人の感受性を考慮したリスク評価
| 対策 | 技術 | 期待される効果 |
| 環境モニタリング | IoTセンサー | 曝露リスク80%低減 |
| 個人用防護具 | AI最適化 | 防護効率30%向上 |
| 曝露評価 | バイオマーカー分析 | 早期介入機会の2倍増 |
これらの先進的対策により環境要因によるリスクを最小限に抑え、再発の可能性を大幅に低減できる可能性があります。
統合的ストレス管理
ストレスは様々な健康問題のトリガーとなる可能性があり、透過性亢進型肺水腫の再発リスクにも影響を与える可能性があるのです。
最新の研究では身体的ストレスと心理的ストレスの相互作用が注目されており、これらを統合的に管理することの重要性が指摘されています。
効果的な統合的ストレス管理の方法
- マインドフルネス瞑想(脳機能画像による効果確認)
- バイオフィードバック療法(自律神経機能の最適化)
- 適応的運動療法(個人の状態に応じた運動処方)
- 社会的つながりの強化(オンラインコミュニティの活用)
- 質の高い睡眠の確保(睡眠ステージ最適化技術の応用)
| 管理方法 | 実践頻度 | 期待される効果 |
| マインドフルネス瞑想 | 毎日15分 | ストレスホルモン30%減少 |
| バイオフィードバック | 週2回 | 自律神経バランス改善 |
| 適応的運動療法 | 週3-5回 | 免疫機能20%向上 |
これらを実践することで心身の健康状態を最適化し、再発リスクの大幅な低減が期待できるでしょう。
透過性亢進型肺水腫の再発予防は個々の患者さんの詳細なリスク評価に基づいた高度に個別化された予防策を立てて継続的に実践し、その効果を科学的に検証していくことが重要です。
この包括的なアプローチによって透過性亢進型肺水腫の再発リスクを最小化し、患者さんの長期的な健康と生活の質を最大限に向上させることが可能となるでしょう。
治療費
透過性亢進型肺水腫の治療費は病状の重症度や入院期間によって大きく変動し、患者さんとご家族の経済的負担となる可能性があります。
一般的に集中治療を要する重症例では高額になる傾向があり、数百万円から1000万円を超えるケースもあるでしょう。
初診料と再診料
初診料は2,910円、再診料は750円です。特定機能病院での受診の場合、初診料は5,500円、再診料は2,750円に上昇します。夜間・休日の受診ではさらに割増料金が適用されます。
| 診療区分 | 一般病院 | 特定機能病院 |
| 初診料 | 2,910円 | 5,500円 |
| 再診料 | 750円 | 2,750円 |
検査費用:診断と経過観察に必要な支出
胸部X線検査は2,100円~5,620円、CT検査は14,700円~20,700円です。動脈血ガス分析は1,310円、一般的な血液検査セットは4,200円(血液一般+生化学5-7項目の場合)程度です。
病状に応じてこれらの検査が繰り返し行われる可能性があります。
| 検査項目 | 概算費用 |
| 胸部X線 | 2,100円~5,620円 |
| CT | 14,700円~20,700円 |
| 動脈血ガス分析 | 1,310円 |
| 血液検査セット | 34,200円(血液一般+生化学5-7項目の場合) |
処置費用:生命維持に欠かせない治療
人工呼吸器管理は1日あたり9,500円です。高流量酸素療法は1日あたり1,920円、非侵襲的陽圧換気は64,800円かかります。
薬物療法の費用は使用する薬剤によって異なりますが、抗菌薬や利尿薬などで1日数千円から数万円の範囲で変動します。
入院費用
集中治療室(ICU)での管理が必要な場合、1日あたりの入院費用は10万円以上になることがあります。一般病棟でも1日2万円程度です。
これに加え、食事療養費(1食460円程度)や各種管理料が加算されます。
| 入院先 | 1日あたりの概算費用 |
| ICU | 10万円以上 |
| 一般病棟 | 2万円程度 |
| 食事療養費 | 1食460円 |
詳しく述べると、日本の入院費計算方法は、DPC(診断群分類包括評価)システムを使用しています。
DPCシステムは、病名や治療内容に基づいて入院費を計算する方法です。以前の「出来高」方式と異なり、多くの診療行為が1日あたりの定額に含まれます。
主な特徴:
- 約1,400の診断群に分類
- 1日あたりの定額制
- 一部の治療は従来通りの出来高計算
表:DPC計算に含まれる項目と出来高計算項目
| DPC(1日あたりの定額に含まれる項目) | 出来高計算項目 |
| 投薬 | 手術 |
| 注射 | リハビリ |
| 検査 | 特定の処置 |
| 画像診断 | (投薬、検査、画像診断、処置等でも、一部出来高計算されるものがあります。) |
| 入院基本料 |
計算式は下記の通りです。
「1日あたりの金額」×「入院日数」×「医療機関別係数※」+「出来高計算分」
例えば、14日間入院とした場合は下記の通りとなります。
DPC名: 肺循環疾患 手術なし 手術処置等2なし
日数: 14
医療機関別係数: 0.0948 (例:神戸大学医学部附属病院)
入院費: ¥356,520 +出来高計算分
これらの費用は健康保険制度により大部分が軽減されますが、自己負担額が高額になる可能性もあります。
高額療養費制度の利用や医療ソーシャルワーカーへの相談が経済的負担軽減に重要です。
早期からの費用面での情報収集と相談が、患者さんとご家族の安心につながるでしょう。
以上
- 参考にした論文
-
LOYD, James E.; NEWMAN, John H.; BRIGHAM, Kenneth L. Permeability pulmonary edema: diagnosis and management. Archives of internal medicine, 1984, 144.1: 143-147.
STAUB, NORMAN C. Pulmonary edema due to increased microvascular permeability to fluid and protein. Circulation research, 1978, 43.2: 143-151.
SPRUNG, Charles L., et al. Evidence for increased permeability in reexpansion pulmonary edema. The American journal of medicine, 1981, 71.3: 497-500.
MUTLU, Gökhan M.; SZNAJDER, Jacob I. Mechanisms of pulmonary edema clearance. American Journal of Physiology-Lung Cellular and Molecular Physiology, 2005, 289.5: L685-L695.
ABERLE, D. R., et al. Hydrostatic versus increased permeability pulmonary edema: diagnosis based on radiographic criteria in critically ill patients. Radiology, 1988, 168.1: 73-79.
CLEMENTS, John A. Pulmonary edema and permeability of alveolar membranes. Archives of Environmental Health: An International Journal, 1961, 2.3: 104-107.
STEPHENS, Kenton E., et al. Tumor necrosis factor causes increased pulmonary permeability and edema. Am Rev Respir Dis, 1988, 137.6: 1364-70.
FISHMAN, ALFRED P. Pulmonary edema: The water-exchanging function of the lung. Circulation, 1972, 46.2: 390-408.
MURRAY, J. F. Pulmonary edema: pathophysiology and diagnosis. The International journal of tuberculosis and lung disease, 2011, 15.2: 155-160.
EGAN, EDMUND A. Lung inflation, lung solute permeability, and alveolar edema. Journal of Applied Physiology, 1982, 53.1: 121-125.