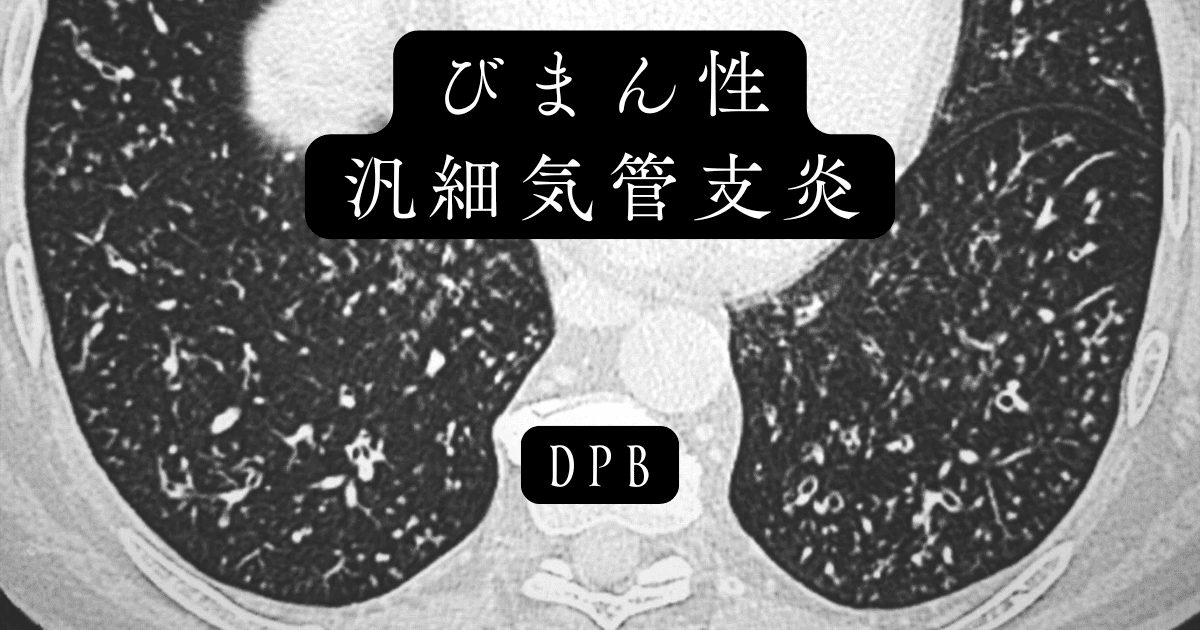
呼吸器疾患の一種であるびまん性汎細気管支炎(びまんせいはんさいきかんしえん)とは、肺の奥深くにある細気管支という小さな通路が慢性的に炎症を起こす珍しい病気です。
この病気はゆっくりと肺全体に広がっていきます。息をするたびに少しずつ酸素を取り込む能力が失われていく様子は、まるで砂時計の砂がこぼれ落ちていくかのようです。
主に東アジアの方々に見られる特徴的な疾患で、その原因は現段階ではまだ完全には解明されていません。

びまん性汎細気管支炎の症状とは
びまん性汎細気管支炎は慢性的な咳、痰、息切れを特徴とする進行性の呼吸器疾患です。その症状は段階的に悪化し、患者の日常生活に甚大な影響を与えることがあります。
持続する咳
びまん性汎細気管支炎の最も顕著な症状は持続する咳です。この咳はまるで終わりのない交響曲のように患者さんの日々を支配します。
この咳の特徴として、初期段階では乾いた咳から始まり、徐々に痰を伴う湿性の咳へと変化していく過程が観察されることが多いです。
特筆すべきはこの咳が朝方や夜間に悪化する傾向があり、患者さんの睡眠を妨げて日中の活動にも支障をきたす可能性が高いという点です。
| 病期 | 咳の頻度 | 日常生活への影響 |
| 初期 | 1日10-20回 | 軽度の睡眠障害 |
| 中期 | 1日50-100回 | 会話や食事の中断 |
| 進行期 | 1日200回以上 | 社会活動の制限 |
粘稠な痰
咳と共に現れるのが痰です。この痰は通常の風邪やアレルギー性鼻炎で見られるものとは一線を画し、非常に粘稠性が高く量も多いことが特徴的です。
多くの患者がさんこの粘稠性の高い痰を排出することに困難を感じ、それが更なる咳を誘発する要因となりって症状の悪循環を引き起こすことがあります。
痰の色は通常白色から黄色、時には緑色を呈することがあり、その色の変化は感染の有無を示唆する重要な指標となる場合があります。
| 病期 | 1日の量 | 色 | 症状の意味 |
|---|---|---|---|
| 初期 | 80-9010ml程度 | 白色 | 炎症による粘液の増加 |
| 中期 | 30-50ml | 黄色 | 好中球の増加 |
| 進行期 | 100ml以上 | 緑色や茶色 | 細菌感染の可能性 |
息切れ
びまん性汎細気管支炎の進行に伴い多くの患者さんが息切れを経験するようになります。
この症状は初期段階では軽度で激しい運動時にのみ感じられることがありますが、病状の進行とともに日常生活のあらゆる場面で感じられるようになるでしょう。
| 呼吸困難の程度 | 状況 |
| 軽度 | 激しい運動時 |
| 中等度 | 階段昇降時 |
| 重度 | 日常生活動作時 |
息切れは患者さんの活動性を極度に制限し、社会生活や仕事にも多大な影響を及ぼす可能性があります。
呼吸器感染
びまん性汎細気管支炎患者は繰り返し呼吸器感染を起こす傾向が強く、これは気道の慢性的な炎症と粘液の貯留が細菌の増殖を促進するためであると考えられているのです。
感染時には以下のような症状が顕著に現れることがあります。
- 高熱
- 咳の頻度と強度の増加
- 痰の量の増加や色の変化
- 呼吸困難感の急激な悪化
これらの感染は既存の症状を著しく悪化させ、患者さんの体力を消耗させる大きな原因となるでしょう。
全身症状
びまん性汎細気管支炎は呼吸器症状だけでなく、慢性的な経過をたどるにつれて全身に広範囲な影響を及ぼすことがあります。
| 全身症状 | 発現頻度 | QOLへの影響 |
| 倦怠感 | 80-90% | 慢性的な疲労感と活力の低下 |
| 体重減少 | 40-50% | 食欲不振や代謝亢進による栄養状態の悪化 |
| 不眠・うつ症状 | 20-30% | 夜間の咳による睡眠障害と日中の集中力低下 |

原因と発症メカニズム
びまん性汎細気管支炎は、遺伝的素因と環境要因の複雑な相互作用によって引き起こされる多因子疾患であり、その発症メカニズムには免疫系の異常や微生物叢の変化も深く関与しています。
遺伝的素因
びまん性汎細気管支炎は東アジア、特に日本や韓国で高い発症率を示す疾患です。この地理的な偏りは特定の遺伝子多型が疾患の発症リスクを高めている可能性を強く示唆しています。
実際、報告によれば、日本人DPB患者の約63%がHLA-Bw54(B54)を保有し、対照健常者の11%と比べ非常に有意な関連を示しました。このオッズ比は10前後にもなり、HLA-B54が発症素因となることは間違いないとされています。
また、嚢胞性線維症の原因遺伝子であるCFTRの変異もびまん性汎細気管支炎の発症リスクを高めることが示唆されています。
環境因子
遺伝的素因に加えて様々な環境要因がびまん性汎細気管支炎の発症や進行に加担しているとされています。
例えば大気汚染物質への長期曝露や喫煙習慣は気道上皮細胞に直接的なダメージを与え、慢性的な炎症状態を引き起こす要因です。
さらに、溶接工や化学工場など職業性の粉塵や化学物質への曝露も気道の過敏性を高め、疾患の発症リスクを増大させる懸念要因として認識されています。
| 環境因子 | 影響メカニズム |
| PM2.5 | 酸化ストレス誘導、炎症性サイトカイン産生 |
| タバコ煙 | 繊毛機能障害、粘液分泌亢進 |
| 職業性有害物質 | 気道上皮バリア機能の破綻 |
| 寒冷刺激 | 気道収縮、粘液分泌増加 |
免疫系の異常
びまん性汎細気管支炎の病態形成には免疫系の異常がが関与している可能性もあるのです。
特に気道における過剰な炎症反応と粘液の過剰分泌が特徴的であり、これらは免疫細胞の機能異常や炎症性メディエーターのバランス崩壊によってもたらされます。
最新の免疫学的研究により、以下のような異常が明らかになっています。
- Th1/Th2バランスの崩壊による過剰な炎症性サイトカイン産生
- 好中球エラスターゼの過剰放出による組織障害
- 制御性T細胞(Treg)の機能不全による炎症抑制機構の破綻
- 自然免疫系の過剰活性化によるパターン認識受容体シグナルの増強
これらのサイトカインの異常はが持続的な炎症反応を引き起こし、病気の進行を促進すると考えられているのです。
感染症
特定の感染症が、びまん性汎細気管支炎の発症や進行を促進する可能性があります。
注目されている病原体と発症メカニズムは以下の通りです。
- マイコプラズマ・ニューモニエ:気道上皮細胞の繊毛機能を障害
- インフルエンザウイルス:気道粘膜のバリア機能を破壊
- 緑膿菌:バイオフィルム形成により慢性感染を引き起こす
これらの微生物は気道の慢性的な炎症を引き起こすだけでなく、免疫系の異常活性化を通じてびまん性汎細気管支炎の発症や進行を加速させることがあるとされているのです。

診察と正確な診断への道筋
びまん性汎細気管支炎(びまんせいはんさいきかんしえん)の診断は、詳細な問診、身体診察、画像検査、および機能検査を組み合わせて総合的に行われます。
問診
問診では患者さんの病歴や生活環境について詳細な情報収集が行われますが、特に症状の経過や持続期間、家族歴、職業歴、喫煙歴などを確認することが重要です。
| 問診項目 | 確認内容 |
| 症状経過 | 発症時期、進行速度 |
| 家族歴 | 類似疾患の有無 |
| 職業歴 | 有害物質への曝露 |
これらの情報は、診断の方向性を決定する上で重要な役割を果たすのです。
身体診察
身体診察では視診、聴診、打診、触診によって全身状態を観察し、特に呼吸器系の異常を注意深く評価します。
- 呼吸音の聴取
- 胸郭の動きの観察
- チアノーゼの有無の確認
これらの所見は、病状の進行度や重症度を判断する上で大切な情報です。
画像検査
画像検査はびまん性汎細気管支炎の診断において中心的な役割を果たします。
| 検査種類 | 主な所見 |
| 胸部X線 | びまん性粒状影 |
| 胸部CT | 小葉中心性結節影 |
特に高分解能CT(HRCT)は細気管支周囲の小結節や気管支壁の肥厚を詳細に描出することができ、診断精度の向上に寄与するでしょう。
肺機能検査
患者さんの呼吸機能を客観的に評価するために行われるのが肺機能検査です。
主な検査項目
- スパイロメトリー
- フローボリューム曲線
- 拡散能力測定
これらの検査結果は病状の重症度評価や経過観察に活用されます。
血液検査
血液検査では炎症マーカーや免疫学的指標が評価されます。
| 検査項目 | 意義 |
| CRP | 炎症の程度 |
| KL-6 | 間質性肺疾患の活動性 |
これらの検査結果は他の呼吸器疾患との鑑別や病勢の評価に役立つことがあるのです。
気管支鏡検査
気管支鏡検査は気道内の直接的な観察と組織採取を可能にします。
この検査により気道粘膜の状態や分泌物の性状を確認し、必要に応じて気管支肺胞洗浄(BAL)や経気管支肺生検(TBLB)を行うことができます。

画像所見:微細な変化を捉える診断の要
びまん性汎細気管支炎の画像所見は、本疾患の診断において極めて重要な役割を果たします。胸部X線や高分解能CT(HRCT)などの画像検査により、特徴的な所見が観察され、診断の確実性を高めることができます。
さらに、詳細な所見によって疾患の進行度や重症度を反映することが可能になるのです。
胸部X線所見:びまん性の微細変化
胸部X線検査はびまん性汎細気管支炎の初期評価において基本となる画像検査です。典型的な所見として、両側肺野に広がるびまん性の粒状影や小結節影が観察されます。
| 所見 | 特徴 |
| 粒状影 | 両側びまん性 |
| 小結節影 | 1-5mm大 |
これらの所見は特に肺底部や中下肺野で顕著に認められることがあります。

所見:両側肺野にびまん性の粒状影と気管支壁肥厚、肺過膨脹が認められ、DEBとして合致する。
高分解能CT所見:微細構造の詳細な描出
高分解能CT(HRCT)はびまん性汎細気管支炎の診断において最も有用で、特徴的な所見は以下の通りです。
- 小葉中心性結節
- 樹枝状気管支拡張
- モザイク様陰影
これらの所見は細気管支周囲の炎症や気道壁の肥厚を反映しています。
小葉中心性結節:本疾患の特徴的所見
小葉中心性結節はびまん性汎細気管支炎の最も特徴的なHRCT所見です。
| 所見 | 描写 |
| 大きさ | 2-3mm |
| 分布 | びまん性 |
これらの結節は細気管支周囲の炎症性変化を反映しており、肺の二次小葉の中心部に位置することが特徴です。
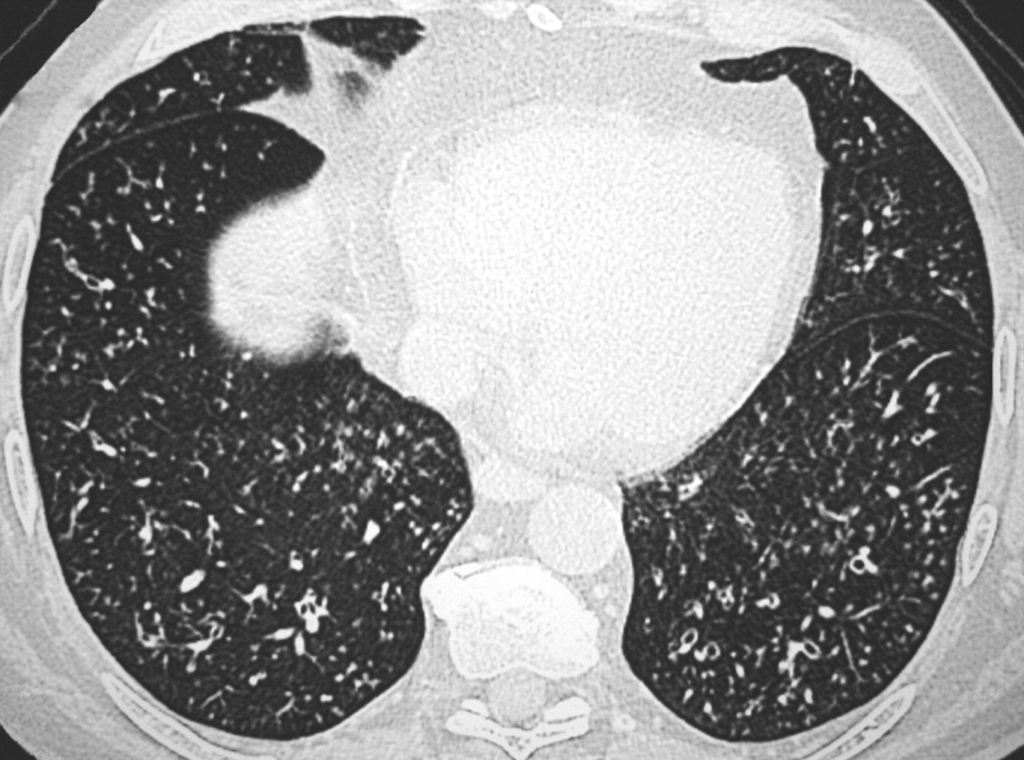
所見:両肺に小葉中心性粒状影と気管支壁肥厚がびまん性に認められる。
気管支拡張所見:進行した病態の反映
病態の進行に伴ってHRCTでは以下のような気管支拡張所見が認められることがあります。
- 気管支内腔の拡大
- 気管支壁の肥厚
- 気管支の蛇行
これらの所見は慢性的な炎症による気道のリモデリングを示唆しているのです。
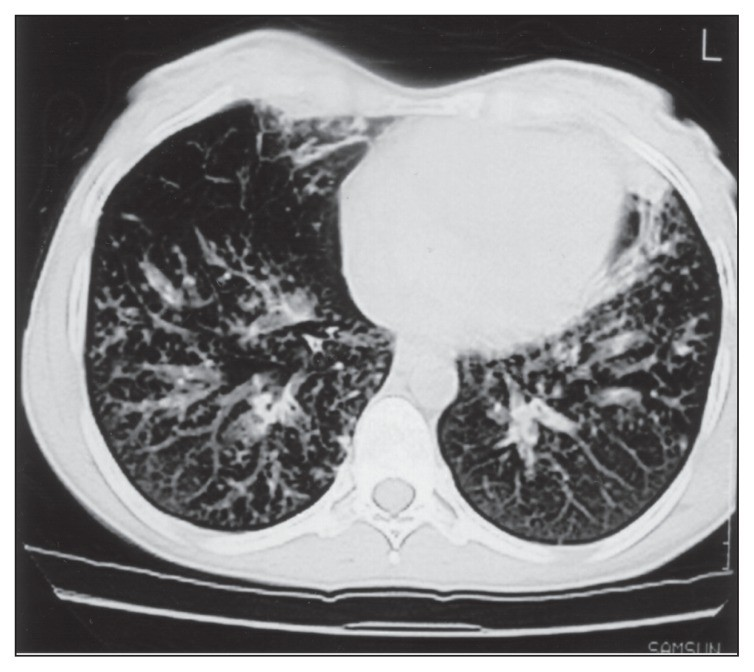
所見:両肺に小葉中心性粒状影とともに、著明な気管支拡張・壁肥厚・粘液栓が目立つ。
モザイク様陰影:換気血流不均等の表現
モザイク様陰影はびまん性汎細気管支炎における換気血流不均等を反映した所見です。
| 所見 | 意味 |
| 高吸収域 | 血流増加領域 |
| 低吸収域 | 換気障害領域 |
これらのモザイク様陰影は特に吸気時と呼気時のHRCT画像を比較することで、より明確に観察されることがあります。
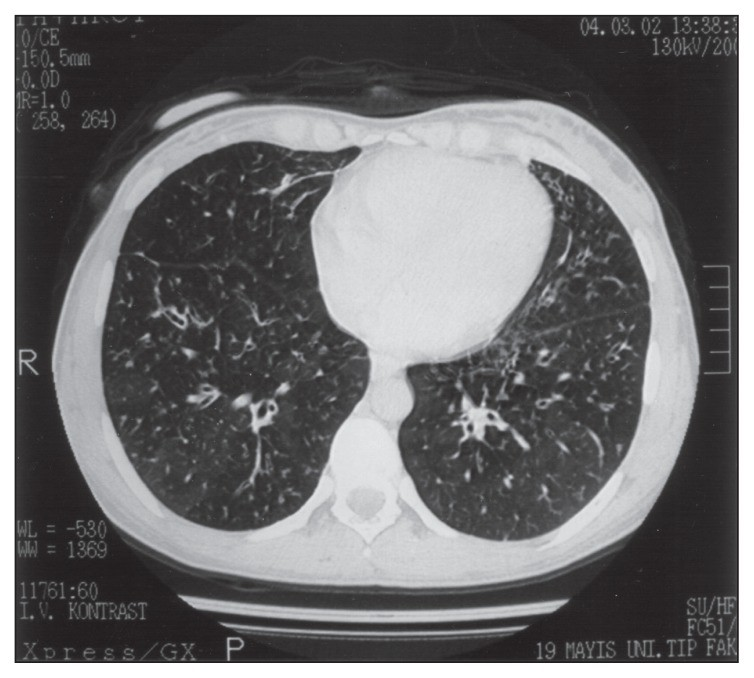
所見:少量中心性粒状影や気管支壁肥厚と共に、両肺にモザイクパターンが認められ、換気血流不均衡を反映した所見である。

治療のアプローチと回復への道のり
びまん性汎細気管支炎の治療は主に薬物療法を中心に行われ、患者さんの状態に応じて長期的な管理が必要です。
適切な治療により症状の改善や進行の抑制が期待できますが、完全な治癒までには個人差があり、数ヶ月から数年の期間を要することがあります。
マクロライド系抗菌薬:治療の主軸
びまん性汎細気管支炎の治療において、マクロライド系抗菌薬が中心的な役割です。
これらの薬剤は抗菌作用に加えて抗炎症作用や免疫調節作用を有しており、長期的な使用により病態の改善が期待できます。
| 薬剤名 | 通常用量 |
| エリスロマイシン | 400-600mg/日 |
| クラリスロマイシン | 200-400mg/日 |
マクロライド療法は通常6ヶ月以上の長期投与が行われ、症状や検査所見の改善に応じて継続されるのが一般的です。
気管支拡張薬:呼吸機能の改善
気管支拡張薬は気道を広げることで呼吸機能の改善を図ります。主に使用される薬剤には以下の通りです。
- β2刺激薬
- 抗コリン薬
- テオフィリン製剤
これらの薬剤は単独または併用で使用され、患者さんの症状や重症度に応じて選択されるでしょう。
ステロイド薬:炎症の抑制
重症例や急性増悪時にはステロイド薬が使用されることがあります。
| 投与経路 | 使用状況 |
| 経口 | 中等症以上 |
| 吸入 | 軽症〜中等症 |
ステロイド薬は強力な抗炎症作用を持ちますが、長期使用による副作用のリスクがあるため慎重に使用することが必要です。
酸素療法:呼吸不全への対応
進行した病態で呼吸不全を伴う場合には在宅酸素療法(HOT)、非侵襲的陽圧換気療法(NPPV)といった酸素療法が導入されることがあります。
これらの療法は患者さんのQOL改善や生命予後の改善に寄与するでしょう。
治療効果の評価と経過観察
治療効果は以下のような評価項目に基づいて定期的に評価され、必要に応じて治療の継続や変更が検討されます。
| 評価時期 | 主な評価項目 |
| 治療開始3ヶ月後 | 症状、CRP、画像 |
| 6ヶ月後 | 上記+呼吸機能 |
治療期間は個人差が大きく、完全な治癒までには時間を要することも少なくありません。多くの場合マクロライド療法開始後3〜6ヶ月で症状の改善が見られ始めますが、治療の継続が必要となります。
長期的な経過観察と適切な治療管理により良好な予後が期待できる可能性が高いです。

治療の副作用とリスク
びまん性汎細気管支炎の治療には様々な薬剤が使用されますが、これらの薬剤にはそれぞれ副作用やリスクが伴う可能性があります。
長期的な治療管理においてこれらの副作用やリスクを理解し、適切に対処することが重要です。
マクロライド系抗菌薬の副作用
マクロライド系抗菌薬はびまん性汎細気管支炎の治療の主軸となりますが、長期使用に伴う副作用に注意が必要です。
主な副作用には以下のようなものがあります。
| 副作用 | 発生頻度 |
| 消化器症状(悪心、嘔吐、下痢) | 5-10% |
| 肝機能障害 | 1-5% |
| QT延長(心電図異常) |
これらの副作用は多くの場合軽度で一過性ですが、重篤化する可能性もあるため定期的なモニタリングが大切になります。
気管支拡張薬のリスク
気管支拡張薬は呼吸機能の改善に有効ですが、使用に伴うリスクも存在します。
β2刺激薬の主な副作用
- 動悸
- 手指振戦
- 低カリウム血症
抗コリン薬の副作用
- 口渇
- 排尿障害
- 眼圧上昇
これらの副作用は薬剤の用量調整や投与方法の変更により管理できることがありますが、患者さんの状態を慎重に観察することが重要です。
ステロイド薬の長期使用に伴うリスク
ステロイド薬は強力な抗炎症作用を持ちますが、長期使用による様々なリスクが知られています。
| 副作用 | 影響 |
| 骨粗鬆症 | 骨折リスク上昇 |
| 糖尿病 | 血糖コントロール悪化 |
| 感染症 | 易感染性 |
これらの副作用はステロイド薬の用量や使用期間に依存して増加する傾向があるため、可能な限り最小限の使用にとどめることが望ましいです。
酸素療法に関連するリスク
酸素療法は呼吸不全の改善に有効ですが、以下のような長期使用に伴うリスクも存在します。
- 二酸化炭素ナルコーシス
- 酸素毒性
- 身体活動の制限
また、在宅酸素療法を行う場合は火災のリスクや機器の管理に関する負担が生じる可能性もあるでしょう。
薬剤耐性菌の出現リスク
長期的な抗菌薬使用に伴い、薬剤耐性菌が出現するリスクがあります。
| 菌種 | 耐性化リスク |
| 緑膿菌 | 中等度 |
| MRSA | 高度 |
耐性菌の出現は治療の難渋化や感染症のコントロール不良につながる可能性があるため、適切な抗菌薬の選択と使用が重要です。

再発リスクと予防戦略
びまん性汎細気管支炎は適切な管理により症状の改善が期待できる疾患ですが、再発のリスクも存在します。再発予防には継続的な医療管理と生活習慣という両面からのアプローチが重要です。
定期的なフォローアップを継続しながら、日常生活における注意点を守ることが、長期的な疾患管理において大切です。
再発リスクの評価
びまん性汎細気管支炎の再発リスクは患者さんの状態や治療経過によって異なります。
再発リスクに影響を与える要因
- 治療の中断
- 感染症の合併
- 環境因子への曝露
| リスク因子 | 再発率への影響 |
| 治療の中断 | 2-3倍上昇 |
| 喫煙の継続 | 1.5-2倍上昇 |
これらのリスク因子を適切に管理することが、再発予防の鍵となります。
定期的なフォローアップの重要性
再発を早期に発見して適切な対応を行うためには定期的なフォローアップが不可欠です。
フォローアップ項目
- 自覚症状の評価
- 呼吸機能検査
- 画像検査(胸部X線、CT)
| フォローアップ頻度 | 検査項目 |
| 3-6ヶ月毎 | 呼吸機能、血液検査 |
| 年1回 | 胸部CT |
これらの定期的な評価により、再発の兆候を早期に捉えることが可能となります。
生活習慣の改善による再発予防
日常生活における注意点や習慣の改善、再発予防に重要な役割を果たします。再発予防のための生活習慣改善策として以下のようなものが挙げられるでしょう。
- 禁煙の徹底
- 適度な運動の継続
- バランスの取れた栄養摂取
- ストレス管理
| 生活習慣 | 再発リスク低減効果 |
| 禁煙 | 30-50% |
| 運動療法 | 20-30% |
感染予防対策
びまん性汎細気管支炎患者は呼吸器感染症に罹患しやすい傾向があります。感染予防は再発予防の観点からも重要です。
具体的には手洗い・うがいの徹底、マスクの着用、予防接種(インフルエンザ、肺炎球菌)といった対策をすることで感染症のリスクを低減し、再発の誘因を減らすことが可能となるでしょう。
環境因子への配慮
環境因子もびまん性汎細気管支炎の再発に影響を与える可能性があります。
注意すべき環境因子は以下の通りです。
| 環境因子 | 対策 |
| 大気汚染 | 外出時のマスク着用 |
| 職業性粉塵 | 防護具の使用 |
| 室内環境(温度・湿度) | エアコンなどの活用 |
これらの環境因子への曝露を最小限に抑えることで再発リスクを低減できるでしょう。

治療費:詳細な内訳
びまん性汎細気管支炎の治療費は診断から長期管理まで多岐にわたり、患者さんの経済的負担が大きくなることがあります。
初診料は2,910円、再診料は750円ですが、専門外来では別途加算されることもあります。検査費用はCT検査で14,700円~20,700円、呼吸機能検査で2,300円~5,700円です。
薬物療法の費用
マクロライド系抗菌薬の月額費用は、例えばエリスロシン(エリスロマイシン)600mg/日の少量長期投与の場合、10.8円×3錠/日の30日分であり、972円になります。
入院費用
入院費は1日約5,000〜10,000円、個室利用では追加料金が必要です。
詳しく述べると、日本の入院費計算方法は、DPC(診断群分類包括評価)システムを使用しています。
DPCシステムは、病名や治療内容に基づいて入院費を計算する方法です。以前の「出来高」方式と異なり、多くの診療行為が1日あたりの定額に含まれます。
主な特徴:
- 約1,400の診断群に分類
- 1日あたりの定額制
- 一部の治療は従来通りの出来高計算
表:DPC計算に含まれる項目と出来高計算項目
| DPC(1日あたりの定額に含まれる項目) | 出来高計算項目 |
| 投薬 | 手術 |
| 注射 | リハビリ |
| 検査 | 特定の処置 |
| 画像診断 | (投薬、検査、画像診断、処置等でも、一部出来高計算されるものがあります。) |
| 入院基本料 |
計算式は下記の通りです。
「1日あたりの金額」×「入院日数」×「医療機関別係数※」+「出来高計算分」
例えば、14日間入院とした場合は下記の通りとなります。
DPC名: 慢性閉塞性肺疾患 手術なし 手術処置等1なし 手術処置等2なし 定義副傷病名なし
日数: 14
医療機関別係数: 0.0948 (例:神戸大学医学部附属病院)
入院費: ¥355,000 +出来高計算分
長期管理費用
年間の総治療費は外来管理で約30〜50万円、入院を要する場合は100万円以上になることも考えておかなければなりません。
経済的支援策
保険適用となると1割~3割の自己負担であり、更に高額医療制度の対象となるため、実際の自己負担はもっと安くなります。
なお、上記値段は2024年6月時点のものであり、最新の値段を適宜ご確認ください。
難病医療費助成制度の活用により、自己負担額が軽減される可能性があります。
以上