感染症の一種であるパラチフスとは、サルモネラ属の細菌が引き起こす深刻な消化器系疾患です。
この病気は、汚染された食品や水を摂取することで感染します。 発展途上国を中心に世界中で発生しています。
主な症状には、持続する高熱、腹痛、下痢などがあります。 時に重篤な合併症を引き起こす可能性もあります。
パラチフスは、チフス(腸チフス)に似た症状を呈することから、その名が付けられました。 しかし、原因となる菌が異なります。予防には、衛生管理と安全な飲食習慣が重要です。

感染症の一種であるパラチフスの主症状について
パラチフスは深刻な消化器系疾患であり、その主症状は多岐にわたる複雑な様相を呈します。
初期症状
パラチフスの初期症状は、一般的な風邪や胃腸炎と類似しているため、見逃されやすいという特徴を持ちます。
発熱は最も顕著な症状の一つで、徐々に上昇し、39度から40度に達することもあります。この高熱は数週間持続し、患者さんの体力を著しく消耗させる主要因となります。
頭痛や筋肉痛、全身倦怠感も初期段階でよく観察される症状です。これらの症状は急激に現れる場合もあれば、緩やかに進行する場合もあります。
| 症状 | 特徴 |
| 発熱 | 徐々に上昇し39〜40度に達する |
| 頭痛 | 持続的で強い痛みを伴う |
| 筋肉痛 | 全身に及ぶ広範囲の痛み |
| 倦怠感 | 日常生活に支障をきたす程度 |
消化器症状
パラチフスの進行に伴い、消化器系の症状がより顕著になってきます。
腹痛は初期から見られることが多く、その程度は軽度から重度まで様々な様相を呈します。下痢は特徴的な症状の一つで、初期には便秘傾向にあったものが、時間の経過とともに水様性の下痢に変化します。
食欲不振も一般的な症状で、長期間続くと栄養状態の悪化を引き起こします。嘔吐が見られる場合もありますが、必ずしも全ての患者さんに現れるわけではありません。
- 腹痛(軽度から重度まで幅広い)
- 下痢(初期は便秘傾向から水様性へ変化)
- 食欲不振
- 嘔吐(一部の患者さんのみ)
これらの消化器症状は、患者さんの生活の質を著しく低下させる主要因となります。
その他の全身症状
パラチフスは全身性の感染症であるため、様々な臓器に影響を及ぼします。
皮膚症状として、体幹部にバラ疹(淡いピンク色の斑点)が現れます。このバラ疹は数日で消失しますが、パラチフスの診断において重要な手がかりとなります。
肝臓や脾臓の腫大が見られる場合もあり、これらは触診で確認できます。精神症状として、意識レベルの低下や錯乱状態が現れることもあります。
特に高齢者や免疫力の低下した方では、このような症状が顕著に現れやすいので注意します。
| 症状 | 特徴 |
| バラ疹 | 体幹部に出現する淡いピンク色の斑点 |
| 肝脾腫 | 触診で確認可能な肝臓・脾臓の腫大 |
| 精神症状 | 意識レベル低下や錯乱状態 |
合併症
パラチフスの経過中に、様々な合併症が生じます。
消化管出血や腸穿孔は重大な合併症の一つで、緊急の対応を要します。髄膜炎や心筋炎などの重篤な合併症が発生することもあり、これらは生命を脅かす危険性を秘めています。
2019年に発表された研究によると、パラチフス患者の約5%に何らかの合併症が見られたと報告されています。
この数字は一見低く見えるかもしれませんが、実際には看過できない割合であり、早期発見と適切な対応の重要性を示唆しています。
| 合併症 | 危険度 |
| 消化管出血 | 高 |
| 腸穿孔 | 極めて高 |
| 髄膜炎 | 高 |
| 心筋炎 | 高 |
- 消化管出血(緊急対応を要する)
- 腸穿孔(致命的な転帰をたどる可能性がある)
- 髄膜炎(中枢神経系への影響が大きい)
- 心筋炎(心機能低下のリスクが高い)
パラチフスの症状は、軽症から重症まで幅広い臨床像を呈します。
上記で述べた症状のいくつかが組み合わさって現れることが多いですが、全ての症状が同時に出現するわけではありません。
症状の程度や持続期間も異なるため、医療機関での適切な診断が不可欠です。

パラチフスの原因やきっかけ
病原体
パラチフスを引き起こす主要な病原体は、サルモネラ属菌の特定の種類です。
具体的には、サルモネラ・パラチフィA(Salmonella Paratyphi A)、サルモネラ・パラチフィB(Salmonella Paratyphi B)、サルモネラ・パラチフィC(Salmonella Paratyphi C)の3種類が知られています。
これらの菌は、ヒトの腸内で増殖し、感染を引き起こします。
| 菌種 | 学名 | 特徴 |
| パラチフィA | Salmonella Paratyphi A | 最も一般的な原因菌 |
| パラチフィB | Salmonella Paratyphi B | 地域によって発生頻度が異なる |
| パラチフィC | Salmonella Paratyphi C | 比較的稀だが重症化しやすい |
感染経路
パラチフスの主たる感染経路は経口感染です。汚染された食品や水を摂取することで、体内に病原体が侵入します。
特に衛生状態が劣悪な地域では、水系感染のリスクが顕著に上昇します。以下に、主な感染源を列挙します。
- 不適切な処理がなされた飲料水
- 非衛生的な環境で調理された食品
- 生食や加熱不足の食材(特に二枚貝などの水産物)
- 感染者が取り扱った食品
これらの摂取が、パラチフス感染の主要な原因となります。
感染リスク要因
パラチフス感染のリスクを高める要因には、複数の環境的・社会的要素が複雑に関与しています。
発展途上国や衛生設備が不十分な地域への渡航は、感染リスクを著しく増大させます。また、人口密度が高く、衛生状態が劣悪な地域での生活も、感染の機会を増加させます。
さらに、免疫機能が低下している人々は、感染しやすく、重症化のリスクも高くなります。
| リスク要因 | 詳細 | 影響度 |
| 地域特性 | 発展途上国、衛生設備不足地域 | 高 |
| 生活環境 | 人口密集地、衛生状態不良地域 | 中〜高 |
| 個人の健康状態 | 免疫機能低下者 | 非常に高 |
感染源となる保菌者
パラチフスの感染源として特に警戒すべきは、無症状保菌者の存在です。
これらの人々は、自覚症状がないまま病原体を排出し、周囲に感染を拡大させます。
特に食品業界で働く無症状保菌者は、大規模な集団感染を引き起こす潜在的な危険性があるため、公衆衛生上極めて重要な問題となっています。
- 回復後も一定期間病原体を排出し続ける回復期保菌者
- 慢性的に腸管内に病原体を保持する慢性保菌者
- 胆嚢に病原体が定着している胆嚢内保菌者
これらの保菌者が、知らぬ間に感染源となり、パラチフスの伝播を助長します。
環境要因
パラチフス菌の生存や増殖に影響を与える環境要因も、感染リスクに密接に関連しています。
高温多湿な気候条件下では、菌の増殖が活発化するため、感染のリスクが上昇します。また、自然災害による水道設備の破壊や、避難所での衛生状態の悪化も、感染拡大の一因となります。
| 環境要因 | 影響 | 対策 |
| 気候条件 | 高温多湿で菌増殖促進 | 食品の適切な保存・管理 |
| 自然災害 | 衛生インフラ破壊 | 迅速な復旧と代替手段の確保 |
| 避難生活 | 衛生状態悪化 | 避難所の衛生管理強化 |
パラチフスの原因や感染経路は、単一の要因ではなく、複数の要素が複雑に絡み合って感染リスクを高めています。

パラチフスの診察と診断
問診と身体診察
パラチフスの診断プロセスは、まず詳細な問診から始まります。医師は患者さんの渡航歴、食事歴、周囲の感染状況などを丁寧に聴取し、病歴を把握します。
続いて行われる身体診察では、全身状態や特徴的な身体所見を綿密に確認します。この段階で得られた情報は、後の検査方針決定に重要な影響を与えます。
| 問診項目 | 確認内容 | 診断上の意義 |
| 渡航歴 | 発展途上国への訪問 | 感染リスクの評価 |
| 食事歴 | 生水や非加熱食品の摂取 | 感染経路の推定 |
| 周囲の状況 | 同様の症状を呈する人の有無 | 集団感染の可能性 |
血液検査
パラチフスの診断において、血液検査は欠かすことのできない重要な手段です。一般的な血液検査では、白血球数やCRP値(C反応性タンパク質)を測定し、体内の炎症の程度を評価します。
さらに、肝機能や腎機能の検査も併せて行うことで、全身状態を総合的に把握します。これらの検査結果は、パラチフスの診断のみならず、重症度の判定や合併症の早期発見にも寄与します。
- 白血球数(多くの場合減少傾向を示す)
- CRP値(通常、上昇が見られる)
- 肝機能検査(AST、ALTなどの肝酵素値)
- 腎機能検査(BUN、クレアチニンなどの腎機能マーカー)
これらの検査項目を総合的に評価することで、パラチフスの可能性を推測し、さらなる精密検査の必要性を判断します。
血液培養
パラチフスの確定診断において、最も信頼性の高い方法が血液培養です。患者さんの血液を採取し、特殊な培地で培養することで、原因菌を直接同定します。
ただし、血液培養の陽性率は病期によって変動するため、複数回の採取が必要となる場合があります。また、結果が出るまでに数日を要するという欠点もあります。
| 検査名 | 特徴 | 診断的価値 |
| 血液培養 | 確定診断に最適 | 非常に高い |
| 便培養 | 回復期に有用 | 中程度 |
| 骨髄培養 | 感度が高いが侵襲的 | 高い(特殊な場合) |
便培養検査
便培養検査もまた、パラチフス菌の検出に有効な手段です。特に回復期には、便中に菌が排出されるため、診断率が向上します。
ただし、抗菌薬投与後は偽陰性となる可能性があるため、結果の解釈には細心の注意を払います。便培養は、血液培養と併用することで、診断の精度を高めることができます。
血清学的検査
ウィダール反応(Widal test)は、パラチフスの診断に古くから用いられてきた血清学的検査法です。患者さんの血清中の抗体価を測定することで、感染の有無を判定します。
しかしながら、この検査は感度・特異度に課題があり、現在では補助的診断としての位置づけとなっています。より精度の高いELISA法(酵素免疫測定法)などの新しい血清学的検査も開発されています。
| 検査名 | 原理 | 特徴 | 診断的価値 |
| ウィダール反応 | 抗体価測定 | 感度・特異度に課題あり | 補助的 |
| ELISA法 | 抗体検出 | より高感度 | 中〜高 |
| PCR法 | 遺伝子検出 | 迅速だが設備が必要 | 高い |
分子生物学的検査
近年、PCR法(ポリメラーゼ連鎖反応)などの分子生物学的手法を用いた診断も普及しつつあります。これらの方法は、従来の培養法に比べて迅速かつ高感度であり、早期診断に大きく貢献します。
ただし、専門的な設備や技術が必要となるため、全ての医療機関で実施できるわけではありません。地域の中核病院や大学病院などの高次医療機関で主に行われています。
- リアルタイムPCR法(菌の遺伝子を短時間で検出)
- LAMP法(Loop-mediated Isothermal Amplification、等温増幅法の一種)
これらの方法は、菌の遺伝子を直接検出するため、抗菌薬投与後でも診断が可能という利点があります。

画像所見
胸部X線検査
パラチフスでは、肺炎などの呼吸器合併症が発症することがあり、胸部X線検査はこれらの合併症を評価する上で基本的かつ不可欠な検査となります。
典型的な所見としては、両側性のびまん性浸潤影や肺水腫様の像が観察されます。これらの所見は、パラチフスによる全身性の炎症反応や循環動態の変化を反映していると考えられています。
| 所見 | 特徴 | 臨床的意義 |
| 浸潤影 | びまん性両側性 | 肺炎合併の可能性 |
| 肺水腫様陰影 | 主に下肺野 | 循環動態異常の示唆 |
| 胸水 | 少量〜中等量 | 炎症の波及を示唆 |

所見:「肺水腫の症例である。両側肺門周囲の浸潤が“コウモリの翼”状の配置を示している。仰臥位の投影では心臓の大きさについての評価は困難である。胸水は認められない。」
腹部X線検査
腹部X線検査は、パラチフスにおける消化管合併症の評価に有用な手法です。特に腸穿孔が疑われる場合、遊離ガス像の有無を確認するために実施されます。
この検査で得られる情報は、緊急手術の必要性を判断する上で極めて重要な役割を果たします。以下に、腹部X線検査で観察される主な所見を列挙します。
- 遊離ガス像(横隔膜下や腹腔内に見られる異常なガス像で、腸管穿孔を強く示唆)
- 腸管拡張像(腸閉塞や麻痺性イレウスの可能性を示唆)
- 腸管ループの異常配列(腸管の癒着や捻転を疑わせる所見)
これらの所見が認められた場合、緊急の外科的処置が検討されるため、迅速な判断と対応が求められます。
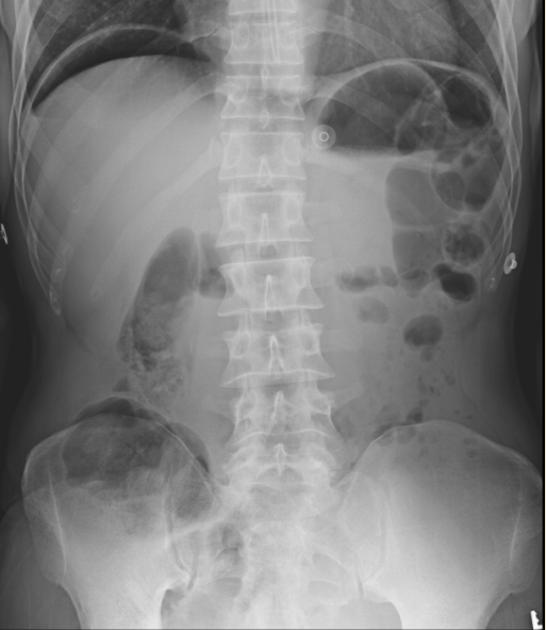
所見:「下部消化管穿孔の症例である。立位腹部X線では、右横隔膜下に三日月状のガスが認められる。」
腹部超音波検査
腹部超音波検査は、非侵襲的かつリアルタイムで結果が得られるという大きな利点を持ちます。パラチフスでは、肝臓や脾臓の腫大、腸管壁の肥厚などが観察されることがあり、これらの所見は疾患の進行度や重症度を反映します。
| 所見 | 特徴 | 臨床的意義 |
| 肝脾腫 | びまん性腫大 | 全身性炎症反応の指標 |
| 腸管壁肥厚 | 回腸末端部に多い | 局所的な炎症の程度を反映 |
| 腹水 | 少量〜中等量 | 腹膜炎の可能性を示唆 |
超音波検査は、ベッドサイドでも実施可能であり、患者さんの状態が不安定な場合でも比較的安全に行えるという利点があります。
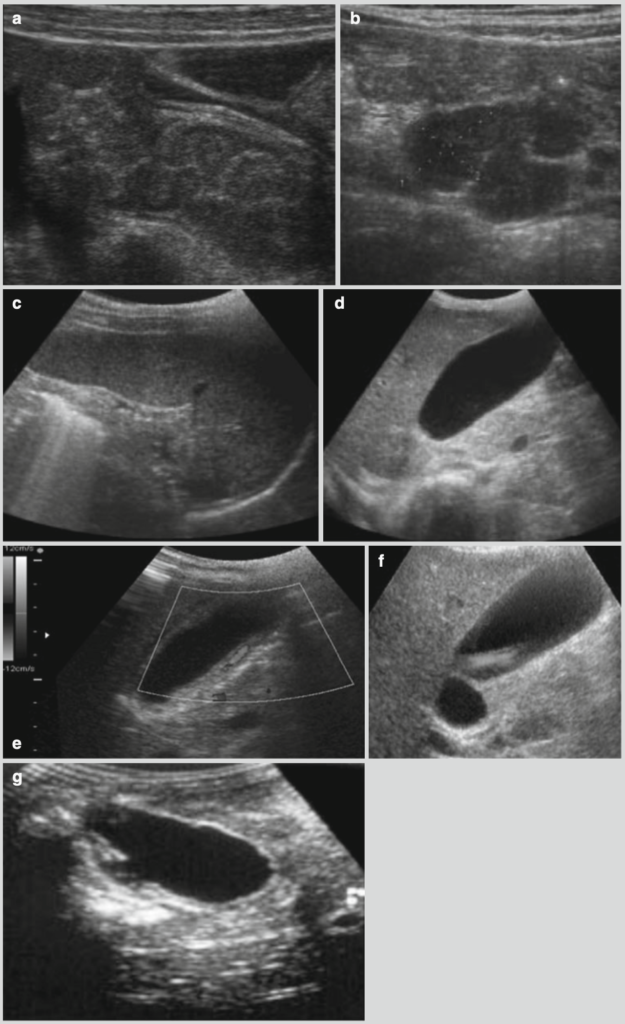
所見:「腸チフスの腹部臓器(回腸、脾臓、胆嚢)およびリンパ節病変。(a–g) 超音波では、回腸壁の肥厚、腸間膜リンパ節の腫大、正常なエコー構造を伴う脾腫、腫大した胆嚢、胆嚢壁の肥厚および血管の増加、胆汁うっ滞、胆嚢粘膜の潰瘍およびその連続性の中断が示されている。」
腹部CT検査
腹部CT検査は、より詳細な解剖学的情報を提供し、パラチフスの合併症評価に大きく貢献します。この検査では、腸管壁の肥厚、腸間膜リンパ節腫大、肝脾腫などが特徴的な所見として捉えられます。
- 腸管壁の肥厚(特に回腸末端部に顕著)
- 腸間膜リンパ節腫大(炎症の波及を示唆)
- 肝脾腫(全身性炎症反応の指標)
- 腹水貯留(腹膜炎の可能性を示唆)
これらの所見は、パラチフスの診断や合併症の評価に重要な情報をもたらし、治療方針の決定に大きく影響します。
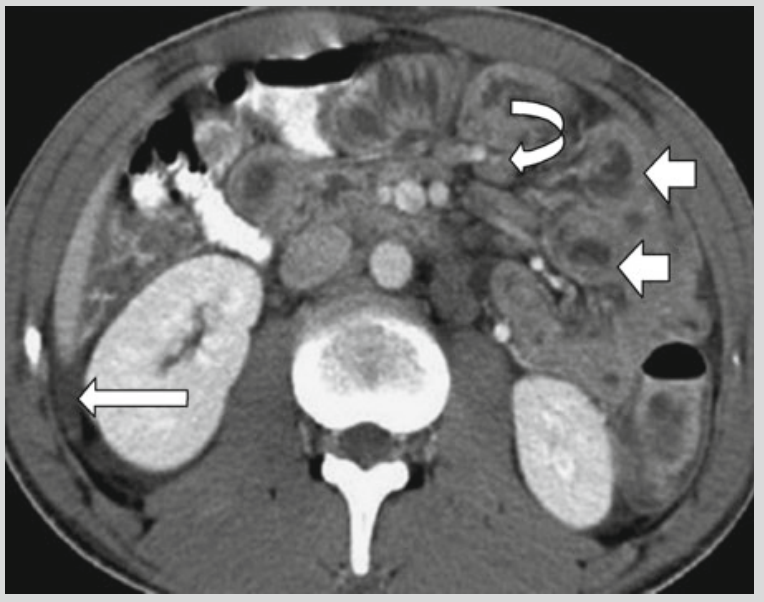
所見:「こちらは腸チフスの症例であるが、パラチフスでも同様です。本CTスキャンでは、空腸壁の肥厚(短い矢印)、リンパ節の腫大(曲線矢印)、および腹水(長い矢印)が確認される。」
MRI検査
MRI検査は、軟部組織のコントラスト分解能に優れており、パラチフスに関連する中枢神経系の合併症、例えば脳炎や髄膜炎の評価に特に有用です。
この検査では、脳実質の信号変化や髄膜の造影増強効果などが観察され、中枢神経系の病変を詳細に評価することができます。
| 検査部位 | 主な所見 | 臨床的意義 |
| 脳 | 浮腫、脳炎像 | 中枢神経系合併症の評価 |
| 脊髄 | 髄膜増強効果 | 髄膜炎の診断補助 |
MRI検査は、放射線被曝がないという利点もあり、特に若年患者や妊娠中の患者の評価に適しています。
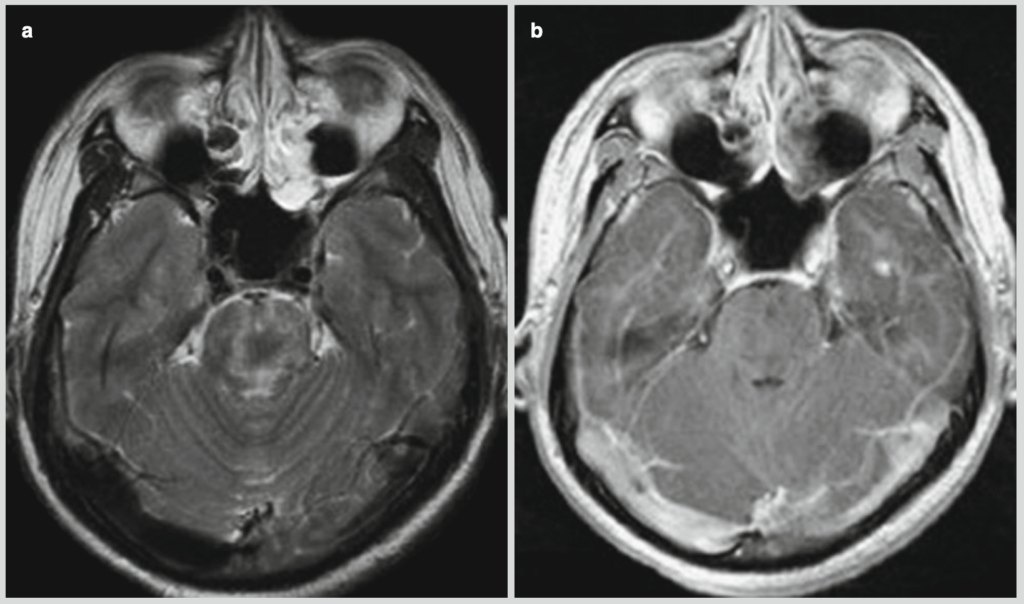
所見:「パラチフスAが脳幹に及んだ症例。(a, b) MRIでは脳幹に高信号の広がりが示される。(a) Gd造影T1WIでは明らかな異常な増強は認められない。」
核医学検査
核医学検査は、パラチフスの診断に直接的に用いられることは比較的少ないですが、合併症の評価や鑑別診断において有益な情報を提供します。
例えば、ガリウムシンチグラフィーは、全身の炎症性病変の局在を評価するのに有用で、パラチフスによる多臓器への影響を包括的に把握するのに役立ちます。
これらの画像検査は、それぞれ特徴的な情報を提供し、パラチフスの診断や経過観察において重要な役割を果たしています。
しかし、画像所見だけでパラチフスと確定診断することは困難であり、臨床症状や他の検査所見と併せて総合的に判断する必要があります。
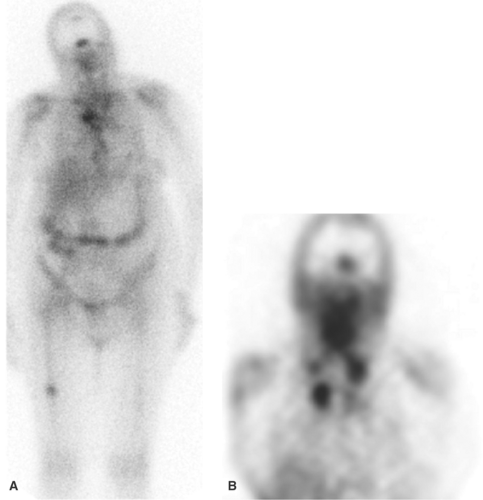
所見:「こちらは原因不明の発熱を呈する転移性腎細胞癌の症例であるが、全身の炎症などチェックする際はこのように有用である。(A) 全身前面画像および(B) 冠状断SPECT画像は、ガリウム-67検査を実施した81歳女性(腎細胞癌の既往あり、持続的な発熱、局所徴候なし)の所見である。縦隔、左鎖骨上領域、脳、右大腿骨遠位部に限局的な活動性の増加が確認された。縦隔リンパ節生検により、腎細胞癌の転移が確認された。脳および大腿骨の転移は画像診断で確認された。」

パラチフスの治療方法と薬、治癒までの期間
抗菌薬治療
パラチフスの主要な治療法は抗菌薬療法です。適切な抗菌薬の選択と投与が治療の成否を大きく左右します。一般的に使用される抗菌薬には、以下のようなものがあります。
- シプロフロキサシン(ニューキノロン系抗菌薬)
- アジスロマイシン(マクロライド系抗菌薬)
- セフトリアキソン(第三世代セフェム系抗菌薬)
- クロラムフェニコール(クロラムフェニコール系抗菌薬)
これらの抗菌薬は、患者の状態や薬剤感受性試験の結果に基づいて慎重に選択されます。選択の際には、薬剤の特性や副作用、患者の年齢や基礎疾患なども考慮に入れます。
| 抗菌薬 | 一般的な投与期間 | 特徴 |
| シプロフロキサシン | 7-14日 | 経口投与可能、耐性菌にも有効 |
| アジスロマイシン | 5-7日 | 短期間投与、組織移行性良好 |
| セフトリアキソン | 10-14日 | 重症例に適応、静脈内投与 |
| クロラムフェニコール | 14-21日 | 髄膜炎合併時に考慮、副作用に注意 |
支持療法
抗菌薬治療と並行して、支持療法も極めて重要な役割を果たします。脱水の予防や電解質バランスの維持が必要となり、以下のような対応が行われます。
- 十分な水分補給(経口または点滴による)
- 電解質の補正(特にナトリウムとカリウムのバランス維持)
- 栄養サポート(経腸栄養や場合によっては一時的な経静脈栄養)
これらの支持療法は、患者の全身状態の改善に大きく寄与し、抗菌薬治療の効果を最大化するために不可欠です。
合併症への対応
重症例では様々な合併症が生じる場合があり、それぞれに適切な対応が求められます。特に腸穿孔などの外科的処置が必要な合併症に対しては、迅速かつ適切な判断と対応が生命予後を左右します。
| 合併症 | 対応 | 留意点 |
| 腸穿孔 | 緊急手術 | 術後の感染管理が重要 |
| 出血性ショック | 輸血、集中治療 | 循環動態の厳密なモニタリング |
| 髄膜炎 | 抗菌薬の髄液移行性考慮 | 神経学的所見の継続的評価 |
| 骨髄炎 | 長期的抗菌薬治療 | リハビリテーションの早期介入 |
治療経過と回復期間
パラチフスの治療期間は個々の症例により異なりますが、一般的には以下のような経過をたどります。
- 抗菌薬投与開始後3-5日で解熱
- 症状改善まで7-14日程度
- 完全回復には4-6週間程度
2019年に発表された多施設共同研究では、適切な抗菌薬治療を受けた患者の95%が3週間以内に臨床的に回復したと報告されています。この研究結果は、早期診断と適切な治療の重要性を強く示唆しています。
再発予防と経過観察
治療終了後も一定期間の経過観察が必要です。再発のリスクがあるため、注意深いフォローアップが求められます。
| フォローアップ項目 | 頻度 | 目的 |
| 血液培養 | 治療終了後1-2週間 | 菌血症の再燃確認 |
| 便培養 | 1、3、6か月後 | 慢性保菌者化の確認 |
| 肝機能検査 | 1-2か月ごと | 肝機能障害の評価 |
| 免疫学的検査 | 6か月後 | 長期的な免疫応答の評価 |
薬剤耐性への対応
近年、薬剤耐性菌の出現が大きな問題となっています。多剤耐性菌による感染症では、治療に難渋する場合があります。このような状況に対処するため、以下のような対策が取られています。
- 薬剤感受性試験の徹底実施
- 複数の抗菌薬の併用療法
- 新規抗菌薬の使用検討
- 地域ごとの耐性菌サーベイランス
これらの対策により、耐性菌への効果的な対応が可能となり、治療成功率の向上が期待されます。
パラチフスの治療は、適切な抗菌薬の選択と支持療法の組み合わせが基本となります。治療開始後は患者の状態を注意深く観察し、必要に応じて治療内容を柔軟に調整することが大切です。

パラチフスの治療の副作用やデメリット(リスク)
パラチフスの治療には、様々な副作用やリスクが伴います。
抗菌薬関連の副作用
パラチフス治療で使用される抗菌薬には、多岐にわたる副作用が報告されています。これらの副作用は、患者の生活の質に多大な影響を及ぼす可能性があり、慎重な経過観察が求められます。
主な副作用として、以下のようなものが挙げられます。
- 消化器症状(悪心、嘔吐、下痢など)
- 皮膚反応(発疹、蕁麻疹、光線過敏症など)
- 肝機能障害(トランスアミナーゼの上昇)
- 腎機能障害(クレアチニンクリアランスの低下)
これらの副作用は、抗菌薬の種類や投与量、患者の体質によって発現頻度や程度が著しく異なります。医療従事者は、患者の状態を綿密にモニタリングし、適切な対応を講じることが求められます。
| 抗菌薬 | 主な副作用 | 注意点 |
| シプロフロキサシン | 腱障害、光線過敏症 | 高齢者や運動選手に特に注意 |
| アジスロマイシン | QT延長、肝機能障害 | 心疾患患者への投与に注意 |
| セフトリアキソン | アナフィラキシー、胆石形成 | アレルギー歴の確認が重要 |
| クロラムフェニコール | 骨髄抑制、灰白色症候群 | 定期的な血液検査が必須 |
耐性菌の出現
長期間の抗菌薬使用は、耐性菌の出現リスクを著しく高めます。耐性菌の発生は、治療の難渋化や他の患者への感染拡大につながる深刻な問題を引き起こします。
耐性菌出現に伴う主な問題点は以下の通りです。
- 多剤耐性菌の出現(MDR:Multi-Drug Resistant bacteria)
- 治療オプションの著しい制限
- 入院期間の大幅な延長
- 医療費の急激な増加
耐性菌対策は、個人レベルのみならず、医療機関全体、さらには社会全体で取り組むべき喫緊の課題となっています。
腸内細菌叢の乱れ
抗菌薬治療は、腸内細菌叢(マイクロバイオーム)のバランスを大きく崩す可能性があります。これにより、様々な消化器症状や二次感染のリスクが顕著に高まります。
| 影響 | 結果 | 長期的影響 |
| 善玉菌の減少 | 消化吸収障害 | 栄養不良、免疫機能低下 |
| 悪玉菌の増殖 | 下痢や腹痛 | 慢性的な消化器症状 |
| 菌交代症 | カンジダ症など | 難治性真菌感染症 |
腸内細菌叢の回復には相当の時間を要し、長期的な健康への影響も懸念されます。プロバイオティクスの補充や食事療法など、腸内環境の改善に向けた積極的なアプローチが必要となる場合もあります。
薬剤相互作用
パラチフス治療に使用される薬剤は、他の薬剤と予期せぬ相互作用を起こす可能性があります。これにより、重篤な副作用や治療効果の著しい減弱が生じる場合があり、細心の注意を払う必要があります。
主な薬剤相互作用のリスクとして、以下のようなものが挙げられます。
- 抗凝固薬との相互作用(出血リスクの顕著な増大)
- 制酸薬との相互作用(抗菌薬の吸収が著しく低下)
- 免疫抑制剤との相互作用(免疫機能の急激な変動)
薬剤相互作用のリスクを最小限に抑えるためには、患者の服用薬剤を詳細に把握し、慎重な薬剤管理を行うことが不可欠です。
長期入院に伴うリスク
重症のパラチフス患者では、長期入院が必要となる場合があります。長期入院には、以下のようなリスクが伴い、患者の全体的な予後に多大な影響を及ぼす可能性があります。
| リスク | 詳細 | 対策 |
| 院内感染 | MRSA、C.difficile感染症 | 厳重な感染対策 |
| ADL低下 | 筋力低下、廃用症候群 | 早期リハビリテーション |
| 心理的影響 | 不安、うつ状態 | 心理サポート、カウンセリング |
| 経済的負担 | 高額な医療費 | 医療費助成制度の活用 |
これらのリスクを軽減するためには、多職種による包括的なケアアプローチが必要不可欠です。
免疫機能への影響
パラチフスそのものや、その治療による免疫機能への影響が報告されています。免疫機能の低下は、他の感染症のリスクを著しく高める可能性があり、長期的な健康管理の観点から重要な問題となります。
主な免疫機能への影響として、以下のようなものが挙げられます。
- 日和見感染症のリスク顕著な増大
- ワクチン接種後の免疫応答が著しく低下
- 自己免疫疾患の顕在化や増悪
免疫機能の回復には相当の時間を要し、慎重かつ長期的な経過観察が必要となります。場合によっては、免疫機能を補助するための追加的な治療介入が検討されることもあります。

パラチフス治療にかかる費用
処方薬の薬価
パラチフス治療に用いられる抗菌薬の価格は、薬剤の種類や投与方法、用量によって大きく異なります。
一般的に使用されるシプロフロキサシン(ニューキノロン系抗菌薬)やアジスロマイシン(マクロライド系抗菌薬)などの薬剤では、1日あたり65円から2000円程度の費用が発生します。
| 抗菌薬 | 1日あたりの薬価 | 特徴 |
| シプロフロキサシン | 65.8〜2,398円(内服〜点滴) | 広域スペクトラム、経口投与可能 |
| アジスロマイシン | 317.8円 | 長時間作用型、組織移行性が高い |
これらの薬価は、厚生労働省が定める公定価格であり、実際の患者負担額は保険適用後さらに低くなります。
1週間の治療費
外来診療の場合、初診料や再診料、処方箋料、薬剤費を合算すると、1週間で概ね1万円から2万円程度の費用となります。この金額には、必要に応じて実施される血液検査や細菌培養検査の費用も含まれます。
一方、入院加療が必要となった場合、入院基本料や検査費用、注射料などが加算され、1週間で5万円から10万円程度にまで上昇します。
入院期間中は、病状の推移や合併症の有無によって日々の医療費が変動するため、正確な金額を事前に見積もることは困難です。
1か月の治療費
重症例で長期入院が必要となった際は、1か月の治療費が50万円を超過する事態も想定されます。この高額な医療費の内訳には、以下のような項目が含まれます。
- 入院基本料(病床の種類や病院の規模により異なる)
- 抗菌薬などの薬剤費(静脈内投与の場合は高額になりやすい)
- 各種検査費用(血液検査、画像診断、細菌学的検査など)
- 食事療養費(1食あたり460円程度)
- 処置料(点滴管理、創傷処置など)
ただし、日本の医療費計算システム、特に入院費の算出方法は、2003年に導入されたDPC(Diagnosis Procedure Combination:診断群分類包括評価)システムを中心に運用されています。このシステムは、従来の「出来高払い」方式から大きく転換し、より効率的で透明性の高い医療費計算を目指しています。
DPCシステムの特徴は、患者の診断名や実施された処置に基づいて、入院費用を包括的に評価する点にあります。具体的には、各疾患や処置に対して、1日あたりの定額が設定されており、この定額には多くの診療行為や薬剤費が含まれています。
DPCによる入院費の計算方法は以下の公式で表されます:
入院費 = (1日あたりの点数 × 入院日数 × 医療機関別係数) + 出来高計算分
ここで重要な要素となるのが「医療機関別係数」です。この係数は、各病院の機能や役割、地域性などを反映して個別に設定されており、同じ治療でも病院によって最終的な費用が異なる要因となります。
例えば、高度な医療を提供する大学病院では、この係数が高く設定されることが一般的です。
具体例として、「細菌性腸炎」で14日間入院した場合を考えてみましょう。
- DPC名:細菌性腸炎(手術処置等2なし)
- 入院日数:14日
- 医療機関別係数:0.0948(例:神戸大学医学部附属病院の場合)
この場合、基本的な入院費は330,790円と算出されます。ただし、これに加えて、DPCの包括評価に含まれない特定の治療や検査などの「出来高計算分」が別途加算されることがあります。
このシステムにより、医療機関は効率的な医療サービスの提供を促進され、患者側も事前に概算の医療費を把握しやすくなるというメリットがあります。ただし、複雑な疾患や予期せぬ合併症が発生した場合には、実際の費用が当初の見込みを上回る可能性もあることに注意が必要です。
なお、上記の価格は2024年10月時点のものであり、最新の価格については随時ご確認ください。
以上

- 参考にした論文