内分泌疾患の一種である成長ホルモン分泌不全性低身長症(GHD)とは体の成長を促進する重要なホルモンである成長ホルモンの分泌が不足することにより、身長の伸びが妨げられる状態を指します。
この病気では下垂体から分泌される成長ホルモンの量が正常値よりも少なくなっています。
成長ホルモンは骨や筋肉の成長を促進するだけでなく、体の代謝にも重要な役割を果たしています。
そのためこの疾患は単に身長が低くなるだけでなく、体の組成や代謝にも影響を与える可能性があるのです。
GHDの主症状
成長ホルモン分泌不全性低身長症はその名が示す通り低身長が主要な症状ですが、実際にはそれだけにとどまらず、患者さんの身体的・精神的発達に幅広い影響を及ぼします。
この疾患の症状は成長ホルモンが体内の様々な組織や器官に作用することから多岐にわたります。
患者さんの年齢や成長ホルモン不足の程度によって症状の現れ方や程度は異なりますが、早期発見と適切な対応が患者さんのQOL向上に不可欠です。
低身長と成長速度の低下
成長ホルモン分泌不全性低身長症の最も顕著な症状はその名の通り低身長です。患者さんの身長は同年齢・同性の平均身長を大きく下回ることがあります。
| 年齢 | 平均身長との差 |
| 幼児期 | -2〜-3 SD |
| 思春期前 | -2〜-4 SD |
| 思春期以降 | -3〜-5 SD |
SD(標準偏差)は平均からのずれを示す統計学的指標です。
低身長に加えて、以下のような特徴が見られることがあります。
- 年間成長速度の低下(通常の成長曲線から外れる)
- 骨年齢の遅れ(実年齢に比べて骨の成熟が遅れる)
- 体重増加不良(身長に対する体重比は正常か、やや肥満傾向)
これらの症状は成長期を通じて徐々に顕在化していくため、定期的な成長曲線のチェックが重要です。
身体組成の変化
成長ホルモンは骨や筋肉の成長だけでなく、体脂肪の分布にも影響を与えます。
そのため、成長ホルモン分泌不全性低身長症の患者さんでは特徴的な身体組成の変化が見られることがあります。
| 変化 | 特徴 |
| 体脂肪率増加 | 特に腹部に脂肪が蓄積 |
| 筋肉量減少 | 全身の筋力低下 |
| 骨密度低下 | 骨折リスクの上昇 |
このような変化は以下のような症状として現れることがあります。
- 腹部のふくらみ(いわゆる「人形様体型」)
- 運動能力の低下
- 易疲労感(疲れやすさ)
身体組成の変化は患者さんの日常生活や運動能力に影響を与える可能性があるため注意が必要です。
顔貌の特徴
成長ホルモン分泌不全性低身長症の患者さんでは特徴的な顔貌が見られることがあります。これは成長ホルモンが顔面骨の成長にも影響を与えるためです。
| 顔貌の特徴 | 説明 |
| 額の突出 | 前頭部が比較的大きく見える |
| 鼻根部の陥凹 | 鼻の付け根が低く見える |
| 中顔面の低形成 | 顔の中央部が小さく見える |
また、以下のような特徴も観察されることがあります。
- 頭囲が身長に比べて大きい
- 髪の毛が細く、成長が遅い
- 歯の生え揃えが遅れる
これらの顔貌の特徴は成長とともに徐々に目立つようになることがあります。
代謝への影響
成長ホルモンは体内の代謝にも重要な役割を果たしています。
そのため、成長ホルモン分泌不全性低身長症の患者さんでは様々な代謝の変化が見られることがあります。
| 代謝の変化 | 影響 |
| 糖代謝異常 | インスリン感受性の低下 |
| 脂質代謝異常 | コレステロール値の上昇 |
| 基礎代謝低下 | エネルギー消費量の減少 |
これらの代謝の変化は以下のような症状として現れることがあるでしょう。
- 空腹時血糖値の上昇
- 血中コレステロール値の上昇
- 体温調節機能の低下(寒がり、暑がり)
代謝への影響は長期的には心血管系のリスク因子となる可能性があるため注意深い観察が大切です。

原因と発症メカニズム
成長ホルモン分泌不全性低身長症の原因は多岐にわたり、単一の要因だけでなく、複数の要因が複雑に絡み合って発症することがあります。
原因は大きく分けて先天性と後天性に分類され、それぞれ異なる発症機序を持ちます。
先天性要因
先天性の成長ホルモン分泌不全性低身長症は遺伝子の異常や先天的な脳の形成異常に起因することが多いです。
これらの要因は胎児期や出生直後から存在し、成長ホルモンの産生や分泌に影響を与えます。
| 遺伝子異常 | 影響 |
| GH1遺伝子 | 成長ホルモン産生不全 |
| GHRHR遺伝子 | 成長ホルモン放出ホルモン受容体異常 |
| POU1F1遺伝子 | 下垂体前葉ホルモン産生細胞の発生異常 |
先天性要因には以下のようなものがあります。
- 単一遺伝子疾患(常染色体劣性遺伝、X連鎖劣性遺伝など)
- 染色体異常(ターナー症候群など)
- 先天奇形症候群(中枢神経系の形成異常を伴うもの)
これらの先天性要因は出生時から成長ホルモンの分泌不全を引き起こす可能性があるのです。
後天性要因
後天性の成長ホルモン分泌不全性低身長症は出生後に何らかの原因で下垂体や視床下部に障害が生じることで発症します。
これらの要因は成長期のどの段階でも発生する可能性があり、それまで正常だった成長ホルモンの分泌に影響を与えます。
| 後天性要因 | 例 |
| 腫瘍性疾患 | 頭蓋咽頭腫、下垂体腺腫 |
| 炎症性疾患 | 下垂体炎、サルコイドーシス |
| 外傷 | 頭部外傷、手術後の合併症 |
後天性要因には次のようなものもあります。
- 放射線治療の影響(脳腫獺の治療など)
- 中枢神経系の感染症(髄膜炎、脳炎など)
- 自己免疫疾患(下垂体機能低下症を伴うもの)
これらの後天性要因は突発的に発症することもあれば、徐々に進行することもあるのです。
特発性成長ホルモン分泌不全症
特発性成長ホルモン分泌不全症は明確な原因が特定できない成長ホルモン分泌不全性低身長症を指します。
この型は全体の中でも比較的多く見られ、複雑な要因が関与していると考えられています。
| 特徴 | 説明 |
| 原因不明 | 明確な器質的異常が見られない |
| 多因子性 | 遺伝的要因と環境要因の相互作用 |
| 可逆性 | 成長期終了後に自然回復することがある |
特発性成長ホルモン分泌不全症では以下のような要因が複合的に作用している可能性が考えられます。
- 軽度の遺伝子多型
- 成長ホルモン分泌リズムの乱れ
- 環境要因(栄養状態、ストレスなど)
これらの要因が複雑に絡み合い、成長ホルモンの分泌不全を引き起こすのです。
環境要因と二次性成長ホルモン分泌不全
環境要因や他の全身疾患が引き金となって二次的に成長ホルモンの分泌が低下することがあります。
これらの要因は直接的に下垂体や視床下部に影響を与えるわけではありませんが、体全体の代謝や内分泌環境に変化をもたらし、結果として成長ホルモンの分泌不全を引き起こします。
| 環境要因 | 影響 |
| 慢性的な栄養不良 | 全身の代謝低下 |
| 過度のストレス | 内分泌環境の乱れ |
| 睡眠障害 | 成長ホルモン分泌リズムの乱れ |
二次性成長ホルモン分泌不全を引き起こす可能性のある全身疾患には以下のようなものがあります。
- 慢性腎不全
- 炎症性腸疾患
- 膠原病
これらの要因による成長ホルモン分泌不全は原因となる環境要因や疾患の改善により、回復する可能性があります。

診察と診断
診察の流れと重要なポイント
成長ホルモン分泌不全性低身長症の診察では、患者さんの成長曲線を詳細に評価することが非常に大切です。
身長や体重の推移を経時的に追跡して標準的な成長曲線と比較します。
この過程で成長速度の低下や成長曲線の平坦化が認められるときは、本疾患を疑う根拠となります。
加えて問診では家族歴や既往歴、生活環境などの情報収集も欠かせません。
| 診察項目 | 確認内容 |
| 身体計測 | 身長・体重・BMI |
| 成長曲線 | 成長速度・曲線の形状 |
| 問診 | 家族歴・既往歴・生活環境 |
身体所見の観察も診断の手がかりとなることがあります。例えば年齢不相応な幼児様顔貌や体幹に比べて四肢が短いといった特徴が見られる場合があります。
これらの所見は成長ホルモン分泌不全による骨成熟の遅れを示唆する可能性があるため、注意深く観察することが求められます。
成長ホルモン分泌刺激試験の実施
GHDの確定診断には成長ホルモン分泌刺激試験が不可欠です。この検査では薬剤を投与して成長ホルモンの分泌を促し、経時的に血中濃度を測定します。
分泌刺激試験には複数の種類があり、患者さまの状態に応じて適切な方法を選択します。
- インスリン負荷試験
- アルギニン負荷試験
- クロニジン負荷試験
検査結果の解釈には専門的な知識が必要となるため、内分泌専門医による評価が推奨されます。
成長ホルモンの頂値が基準値を下回る場合、本疾患の診断につながる可能性が高まります。
ただし単一の検査結果だけでなく、臨床症状や他の検査所見と併せて総合的に判断することが肝要です。
画像診断の役割
成長ホルモン分泌不全性低身長症の診断プロセスにおいて画像診断も重要な位置を占めます。
特にMRI検査は下垂体の形態異常や腫瘍性病変の有無を確認するのに有用です。
| 画像検査 | 主な確認事項 |
| MRI | 下垂体の形態 |
| X線 | 骨年齢の評価 |
また、手首や手のX線撮影により骨年齢を評価することも診断の一助となります。骨年齢が暦年齢に比べて遅れている場合、成長ホルモン分泌不全を示唆する所見となり得ます。
これらの画像検査結果は成長ホルモン分泌刺激試験の結果と合わせて総合的に解釈されます。
他の内分泌機能評価
成長ホルモン分泌不全性低身長症の診断過程では他の内分泌機能も併せて評価することが望ましいです。
下垂体前葉ホルモンの包括的な検査を行うことで複合型下垂体機能低下症の可能性も検討できます。
具体的には甲状腺刺激ホルモン(TSH)、副腎皮質刺激ホルモン(ACTH)、性腺刺激ホルモン(LH、FSH)などの測定が挙げられます。
| 検査項目 | 評価対象 |
| TSH | 甲状腺機能 |
| ACTH | 副腎機能 |
| LH、FSH | 性腺機能 |
これらの検査結果は成長ホルモン分泌不全性低身長症の原因究明や合併症の早期発見に役立ちます。
また、IGF-1(インスリン様成長因子-1)の測定も診断の補助となることがあります。
IGF-1は成長ホルモンの作用を反映する指標であり、低値を示す場合は成長ホルモン分泌不全を疑う根拠になり得ます。
ただしIGF-1値は年齢や性別、栄養状態などの影響を受けるため、解釈には慎重さが求められます。

GHDの画像所見
MRIによる下垂体の評価
成長ホルモン分泌不全性低身長症の診断においてMRI検査は下垂体の形態学的評価に不可欠です。
MRIでは下垂体の大きさや形状、周囲の構造物との関係を詳細に観察することが可能となります。
正常な下垂体は成人では高さが約5〜7mm程度であり、幼児期から思春期にかけて徐々に大きくなっていきます。
GHDの患者さんでは下垂体の低形成や欠損が認められることがあります。
| 下垂体所見 | 特徴 |
| 正常 | 高さ5〜7mm (成人) |
| 低形成 | 高さ3mm未満 |
| 欠損 | 下垂体が確認できない |
特に下垂体茎の断裂や後葉の異所性位置などの所見は、先天性の成長ホルモン分泌不全を示唆する重要な手がかりとなります。
これらの所見は患者さんの臨床症状や内分泌学的検査結果と合わせて総合的に解釈されます。
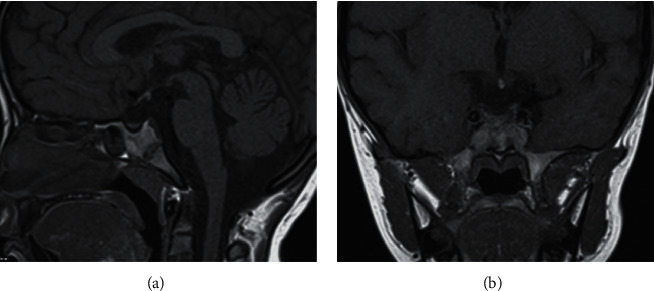
所見:矢状断T1WIおよび冠状断造影T1WIにて、下垂体前葉の萎縮が観察され、欠損した下垂体柄が認められる。
下垂体周囲の構造物の評価
MRI検査では下垂体そのものだけでなく、周囲の構造物も注意深く観察することが大切です。
視交叉や視床下部、海綿静脈洞などの周辺組織の状態を確認することで成長ホルモン分泌不全の原因となり得る病変を特定できる可能性があります。
- 視交叉の圧迫所見
- 視床下部の異常信号
- 海綿静脈洞の浸潤像
これらの所見が認められた際は腫瘍性病変や炎症性疾患の存在を疑う必要があるでしょう。
また、頭蓋咽頭腫や胚芽腫などの腫瘍が存在する場合、それらが下垂体機能に影響を与え、成長ホルモン分泌不全を引き起こしている可能性も考えられます。
| 周辺構造物 | 確認事項 |
| 視交叉 | 圧迫の有無 |
| 視床下部 | 信号異常 |
| 海綿静脈洞 | 浸潤の有無 |
こうした周辺構造物の詳細な評価は成長ホルモン分泌不全性低身長症の原因究明と治療方針の決定に重要な役割を果たします。
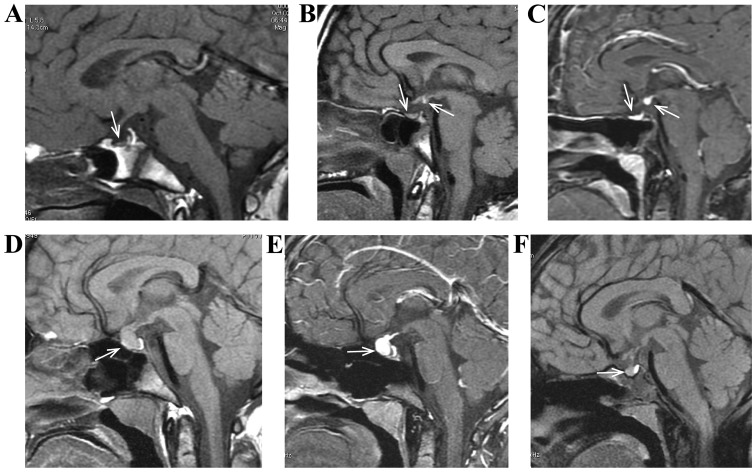
所見:(A) 5歳の男性、下垂体前葉形成不全。成長遅滞と低身長を呈し、特徴として薄く小さい下垂体前葉と高信号を示す下垂体後葉が認められる。(BおよびC) 6歳の女性、下垂体柄中断症候群。成長遅滞と低身長を呈し、特徴として薄く小さい下垂体前葉、下垂体柄の欠如、および高信号を示す下垂体後葉T1が認められる。(D-F) 10歳の女性、原発性甲状腺機能低下症による下垂体過形成。成長遅滞を呈し、特徴として造影スキャン時に均一な増強を示す下垂体前葉の肥大が認められる。(F) 治療後の再検査で磁気共鳴画像検査により患者の下垂体は正常サイズに戻った。
骨年齢の評価
成長ホルモン分泌不全性低身長症の画像診断において骨年齢の評価も欠かせません。
骨年齢の評価には主に左手および手首のX線撮影が用いられます。この検査では骨の成熟度を評価し、暦年齢との比較を行います。
成長ホルモン分泌不全性低身長症の患者さんでは多くの場合、骨年齢が暦年齢に比べて遅れていることが特徴的です。
| 評価項目 | 正常 | 成長ホルモン分泌不全 |
| 骨年齢 | 暦年齢と一致 | 暦年齢より遅れる |
骨年齢の遅れは成長ホルモンが骨の成熟に重要な役割を果たしていることを反映しています。
ただし骨年齢の遅れは成長ホルモン分泌不全に特異的な所見ではないため、他の臨床所見や検査結果と併せて総合的に判断することが大切です。
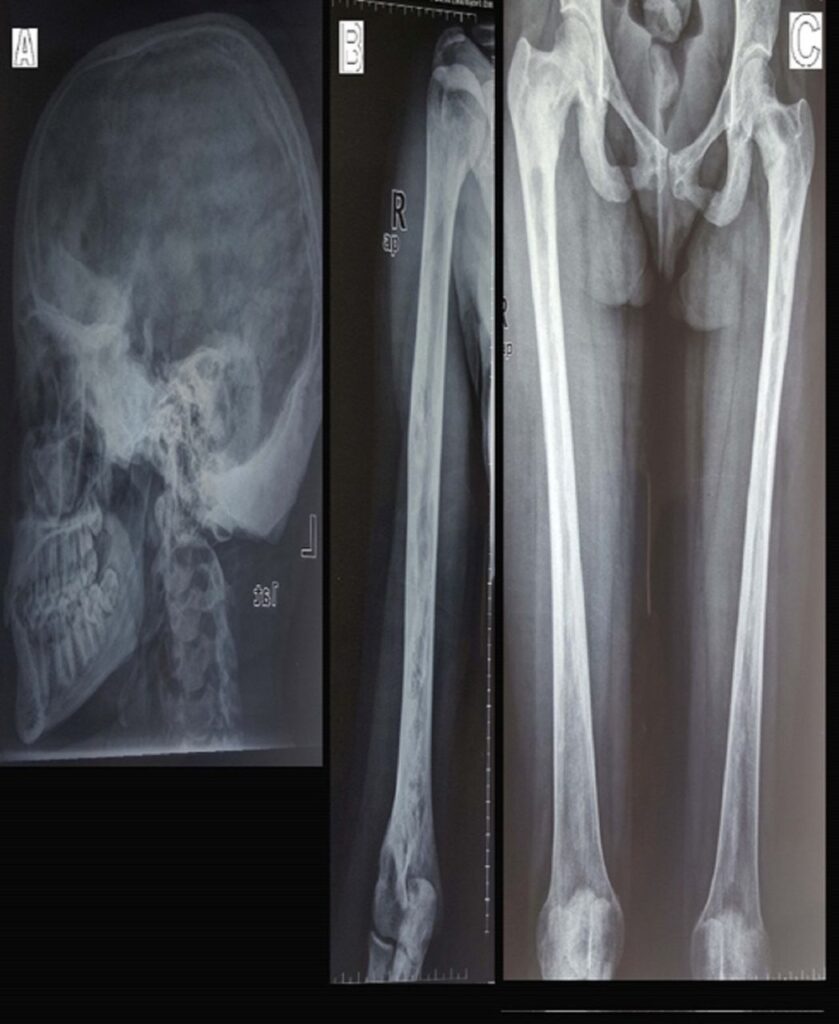
所見:(A) 頭蓋骨:前頭骨および前頭蓋窩の床が硬化および拡大し、蝶形骨にまで及んでいる。後頭骨および後頭頂骨の著しい肥厚および硬化が認められる。(B) 上腕骨:骨幹部の皮質の肥厚、骨幹端部の硬化した厚い縁を伴う嚢胞性病変が見られる。(C) 大腿骨:右および左大腿骨頸部の斑状硬化および拡大、骨幹部の皮質肥厚、スカロッピング、ならびに透過性を伴うすりガラス状の外観が両側に認められる。
骨密度の評価
成長ホルモン分泌不全性低身長症の患者さんでは骨密度の低下が認められることがあります。
骨密度の評価には主にDEXA(二重エネルギーX線吸収測定法)が用いられます。
この検査方法は低被曝量で精度の高い骨密度測定が可能であり、小児においても安全に実施できます。
成長ホルモンは骨形成を促進して骨量を維持する働きがあるため、その分泌不全は骨密度の低下につながる可能性があります。
- 腰椎骨密度
- 大腿骨頸部骨密度
- 全身骨密度
これらの部位の骨密度を測定し、年齢や性別に応じた基準値と比較することで、骨の健康状態を評価します。
| 測定部位 | 評価指標 |
| 腰椎 | BMD (g/cm²) |
| 大腿骨頸部 | T-score |
| 全身 | Z-score |
骨密度の低下が認められた場合、成長ホルモン補充療法による骨密度の改善効果が期待できます。
ただし骨密度の変化は緩やかであるため、治療効果の評価には長期的なフォローアップが必要です。
その他の画像所見
成長ホルモン分泌不全性低身長症の患者さんでは上記の所見以外にもいくつかの特徴的な画像所見が観察されることがあります。
例えば体組成の変化も画像診断によって評価することが可能です。特に脂肪組織の増加と筋肉量の減少は、成長ホルモン分泌不全に関連する所見として知られています。
これらの変化はMRIやCTなどの断層撮影で評価することが可能なのです。
| 体組成変化 | 特徴 |
| 脂肪組織 | 増加 |
| 筋肉量 | 減少 |
また、内臓脂肪の蓄積も観察されることがあり、これは代謝異常のリスク因子となる可能性があります。
これらの画像所見は成長ホルモン分泌不全性低身長症の診断や経過観察において補助的な役割を果たします。
しかしこれらの所見だけで確定診断を下すことはできず、臨床症状や内分泌学的検査結果と併せて総合的に判断することが重要です。

治療法と経過
成長ホルモン補充療法の基本
成長ホルモン分泌不全性低身長症の主な治療法は成長ホルモン補充療法です。
この治療法は体内で不足している成長ホルモンを外部から補充することで患者さんの成長を促進し、代謝機能を改善することが目的です。
成長ホルモン製剤は遺伝子組み換え技術を用いて作られた人工的なホルモンであり、天然の成長ホルモンと同じ構造を持っています。
治療は通常専門医の指導のもとで行われ、患者さんの年齢や体重、症状の程度に応じて投与量が調整されます。
| 治療法 | 目的 |
| 成長ホルモン補充療法 | 成長促進、代謝改善 |
| 定期的な身長測定 | 治療効果の評価 |
成長ホルモン補充療法は長期にわたって継続する必要があるため、患者さんとご家族の理解と協力が重要です。
治療の開始時期や継続期間については個々の患者さんの状況に応じて慎重に判断されます。
投与方法と頻度
成長ホルモン製剤の投与は通常、皮下注射によって行われます。注射は毎日行う必要があり、就寝前に行うことが多いです。
これは成長ホルモンの分泌が自然な状態では夜間に最も活発になることを模倣するためです。
投与部位は腹部、大腿部、上腕部などを交互に使用し、同じ部位への連続した注射を避けることが推奨されます。
- 皮下注射の手技
- 投与部位のローテーション
- 注射器具の適切な取り扱い
近年では患者さんの負担を軽減するために、ペン型注入器や無針注射器などの使いやすいデバイスが開発されています。
これらのデバイスにより自宅での投与がより簡便になり、治療の継続性が向上することが期待されています。
| 投与方法 | 特徴 |
| 皮下注射 | 毎日就寝前に実施 |
| ペン型注入器 | 使用が簡便 |
| 無針注射器 | 痛みが少ない |
投与量や頻度は定期的な診察と検査結果に基づいて調整されます。
成長の度合いや血中IGF-1濃度などのバイオマーカーを参考に最適な投与レジメンが決定されるでしょう。
治療効果と経過観察
成長ホルモン補充療法の効果は個々の患者さんによって異なりますが、多くの場合、治療開始後数か月以内に成長速度の改善が見られます。
治療効果を評価するために定期的な身長測定と成長曲線の作成が行われるのが一般的です。
また、骨年齢の評価や血液検査も定期的に実施され、治療の進捗状況が総合的に判断されます。
| 評価項目 | 頻度 |
| 身長測定 | 3〜6か月ごと |
| 骨年齢評価 | 年1回 |
| 血液検査 | 3〜6か月ごと |
治療の継続期間は成長の状況や骨年齢の進行度によって個別に決定されます。多くの場合、骨端線が閉鎖するまで、すなわち最終身長に達するまで治療が継続されるでしょう。
この期間は個人差が大きく、数年から10年以上に及ぶこともあるのです。
長期的な展望と生活の質の改善
成長ホルモン補充療法の目標は単に身長を伸ばすだけでなく、患者さまの全体的な健康状態と生活の質を向上させることにあります。
治療を通じて体組成の改善、骨密度の増加、心血管系機能の向上など多面的な効果が期待されます。
長期的な治療効果を最大化するためには適切な栄養摂取と運動習慣の確立も大切です。
| 長期的効果 | 期待される改善 |
| 体組成 | 筋肉量増加、体脂肪率低下 |
| 骨密度 | 骨折リスクの減少 |
| 代謝機能 | インスリン感受性の向上 |
また、治療を通じて自己肯定感が高まり、社会生活や人間関係の面でも好ましい変化が見られることがあります。
成長ホルモン補充療法は成長期だけでなく、成人期に移行した後も継続が必要となる場合があります。
そのため長期的な視点で治療計画を立て、患者さんの人生全体を見据えたサポートを提供することが重要です。

治療の副作用とリスク
局所的な副作用
成長ホルモン分泌不全性低身長症の治療において最も頻繁に見られる副作用は注射部位に関連するものです。
これらの局所的な反応は多くの場合軽度であり、時間とともに自然に解消することが多いです。しかし患者さんによっては不快感や心理的な負担を感じる可能性があります。
| 副作用 | 特徴 |
| 発赤 | 注射部位の赤み |
| 腫れ | 局所的な膨らみ |
| 痛み | 軽度の疼痛 |
これらの副作用を軽減するためには注射部位のローテーションや適切な注射技術の習得が重要です。
医療従事者による定期的な指導と患者さん自身による注意深い観察が求められます。
全身性の副作用
成長ホルモン補充療法に伴う全身性の副作用には様々なものが報告されています。
これらの副作用は成長ホルモンの生理学的作用に関連していることが多く、個人差が大きいのが特徴です。
頻度の高い全身性副作用としては以下のようなものが挙げられます。
- 頭痛
- 関節痛
- 筋肉痛
- 浮腫(むくみ)
これらの症状は多くの場合一過性であり、投与量の調整によって改善することがあります。
ただし症状が持続したり、日常生活に支障をきたす場合には、医療機関への相談が不可欠です。
| 副作用 | 対応策 |
| 頭痛 | 鎮痛剤の使用、休息 |
| 関節痛 | 投与量の調整、運動療法 |
| 浮腫 | 塩分制限、利尿剤の検討 |
全身性副作用の発現には個人差が大きいため、患者さんごとの丁寧な経過観察と対応が求められます。
代謝への影響とリスク
成長ホルモンは体内の代謝に広範な影響を及ぼすため、補充療法に伴い代謝関連の副作用が生じる可能性があります。
特に注意が必要なのは糖代謝への影響です。
成長ホルモンはインスリン拮抗作用を持つため、血糖値の上昇や、稀にインスリン抵抗性の増大を引き起こすことがあります。
このため糖尿病の既往がある患者さんや糖尿病のリスクが高い方々では、より慎重な経過観察が重要です。
| 代謝パラメーター | モニタリング頻度 |
| 空腹時血糖 | 3〜6か月ごと |
| HbA1c | 6か月〜1年ごと |
| インスリン | 必要に応じて |
また、脂質代謝への影響も報告されており、コレステロール値やトリグリセリド値の変動に注意が必要になります。
これらの代謝パラメーターの定期的なチェックと必要に応じた生活習慣の指導が大切です。
長期使用に関連するリスク
成長ホルモン補充療法は長期にわたって継続されることが多いため、長期使用に伴うリスクについても考慮する必要があります。
過去には成長ホルモン療法と腫瘍発生リスクの関連性について議論が生じました。
しかし現在の科学的知見では、適切に管理された成長ホルモン補充療法が腫瘍発生リスクを有意に増加させるという明確なエビデンスは示されていません。
それでも慎重を期すべき事項として以下のような点が挙げられます。
- 既往の腫瘍性疾患の再発モニタリング
- 新規腫瘍の発生に対する注意深い観察
- 家族歴を考慮したリスク評価
長期使用に関するデータは徐々に蓄積されつつありますが、個々の患者さまの状況に応じた慎重な判断が求められます。
心理社会的な影響
成長ホルモン補充療法は患者さまの身体的な成長だけでなく、心理社会的な側面にも影響を与える可能性があります。
治療に伴う定期的な通院や日々の注射は患者さん、特に小児の場合、心理的な負担となる可能性があるのです。
また、治療効果への期待と現実のギャップがストレスや不安を引き起こすことも考えられます。
| 心理社会的影響 | 対応策 |
| 治療への不安 | 心理カウンセリング |
| 自己イメージの変化 | 支援グループへの参加 |
| 学校生活への影響 | 教育関係者との連携 |
これらの心理社会的な影響に対しては、医療チームによる包括的なサポートが重要です。
患者さんとそのご家族に対する継続的な教育と心理的支援が、治療の成功と生活の質の向上に不可欠です。

GHDの再発可能性と予防策
再発の定義と頻度
成長ホルモン分泌不全性低身長症の「再発」という概念は、一般的に成人期に入ってから成長ホルモンの分泌能が再び低下することを指します。
小児期に診断され治療を受けた患者さんの中には成人期に入ってから再度成長ホルモン補充が必要となるケースがあるのです。
この現象は成長終了後の再評価で明らかになることが多く、その頻度は報告によって異なりますが、おおよそ10〜50%程度とされています。
| 再発の定義 | 特徴 |
| 成人期での再低下 | 成長終了後の分泌能低下 |
| 補充療法の再開 | 成人GH分泌不全の基準を満たす |
再発のリスクは原因疾患や小児期の重症度によって異なることが知られています。特に器質的な下垂体疾患を背景に持つ患者さんでは、再発のリスクが高いです。
再発のリスク因子
成長ホルモン分泌不全性低身長症の再発リスクにはいくつかの要因が関与していると考えられて、これらのリスク因子を理解することは再発の予防や早期発見に役立ちます。
以下は主なリスク因子です。
- 先天性の下垂体形成異常
- 頭蓋咽頭腫などの腫獰性疾患の既往
- 頭部への放射線治療歴
- 複合型下垂体機能低下症
これらの背景を持つ患者さんでは成人期に入ってからも注意深い経過観察が求められます。
また、小児期の成長ホルモン分泌刺激試験で重度の分泌不全を示した患者さんも再発のリスクが高いとされているのです。
| リスク因子 | 再発リスク |
| 器質的下垂体疾患 | 高い |
| 特発性GHD | 比較的低い |
| 重度の分泌不全 | 高い |
これらのリスク因子を持つ患者さんに対しては成人期への移行期における慎重な評価が重要となります。
再発の予防と早期発見
成長ホルモン分泌不全性低身長症の再発を完全に予防することは困難ですが、早期発見と適切な対応によって再発に伴う健康上の問題を最小限に抑えることが可能です。
予防と早期発見のためには特に以下のような取り組みが大切です。
- 定期的な内分泌機能評価
- 成人期への移行期における再評価
- 生活習慣の改善
- ストレス管理
特に成長終了後の数年間は年に1回程度の内分泌機能評価を受けることが推奨されます。この評価には血中IGF-1濃度の測定や必要に応じて成長ホルモン分泌刺激試験が含まれます。
| 予防策 | 内容 |
| 定期検査 | 年1回の内分泌機能評価 |
| 生活習慣改善 | 適度な運動、バランスの良い食事 |
また、患者さん自身による自己観察も重要です。
成人成長ホルモン分泌不全症の症状について理解し、異常を感じた際には速やかに医療機関を受診することが望ましいでしょう。
再発時の対応と長期的な管理
成長ホルモン分泌不全性低身長症が再発した場合、成人成長ホルモン分泌不全症としての評価と管理が必要です。
再発が確認されたときは成人用量での成長ホルモン補充療法の再開が検討されます。
成人期の成長ホルモン補充療法は身長増加ではなく、代謝機能の改善や生活の質の向上が目的です。
再発後の管理においては特に以下の点に注意が払われます。
- 代謝パラメーターのモニタリング
- 骨密度の評価
- 心血管リスクの管理
- 生活の質の評価
これらの項目について定期的な評価を行い、必要に応じて補充療法の用量調整や他の介入を検討します。
| 管理項目 | 評価頻度 |
| 代謝パラメーター | 3〜6か月ごと |
| 骨密度 | 1〜2年ごと |
| QOL評価 | 6か月〜1年ごと |
長期的な管理においては患者さんの年齢や併存疾患、ライフステージに応じた個別化されたアプローチが重要です。
再発予防のための生活習慣
成長ホルモン分泌不全性低身長症の再発予防において適切な生活習慣の維持は大切な要素です。
健康的な生活習慣は成長ホルモンの自然な分泌を促進し、全身の代謝機能を改善する可能性があります。
再発予防に役立つ生活習慣としては以下のようなものが挙げられます。
- 規則正しい睡眠習慣
- バランスの取れた食事
- 適度な運動 ストレス管理
特に質の良い睡眠は成長ホルモンの分泌に密接に関連しているため十分な睡眠時間の確保と良好な睡眠環境の整備が推奨されます。
また、適度な運動は成長ホルモンの分泌を刺激するだけでなく、全身の代謝機能改善にも寄与するでしょう。
| 生活習慣 | 推奨内容 |
| 睡眠 | 7〜9時間の質の良い睡眠 |
| 運動 | 週3〜5回の中強度有酸素運動 |
これらの生活習慣の改善は再発予防だけでなく、全身の健康維持にも有益です。ただし過度な運動や極端な食事制限は逆効果となる可能性があるため、バランスの取れたアプローチが求められます。

治療費
GHDの治療費は長期にわたる継続的な治療が必要なため高額になる傾向があります。初診料や検査費用に加え、成長ホルモン注射の費用が主な支出となります。
公的医療保険の適用により自己負担は軽減されますが、家計への影響を考慮し経済的な準備が重要です。
初診・再診料と検査費用
初診料は通常2,910円~5,410円で、再診料は750円~2,660円の範囲です。
血液検査やMRI検査などの費用は項目により異なりますが、10,000円から50,000円ほどかかることがあります。
| 項目 | 概算費用 |
| 初診料 | 2,910円~5,410円 |
| 再診料 | 1750円~2,660円 |
| 検査費 | 採血検査 4,200円(血液一般+生化学5-7項目の場合) +その他下垂体などのホルモンなど3項目以上5項目以下4,100円、6項目又は7項目6,230円、8項目以上9,000円 +下垂体前葉負荷試験 イ 成長ホルモン(GH) 12,000円 MRI検査 19,000円~30,200円 |
成長ホルモン注射の費用
治療の中心となる成長ホルモン注射は高価であり、月額10万円前後から30万円ほどの費用がかかる場合があります。ただし、公的医療保険の適用により、自己負担額は大幅に減少します。
入院費用
入院が必要になった際の費用は入院期間や病室のタイプによって変動します。一般的な目安として1日あたり5,000円から20,000円程度です。
詳しく説明すると、日本の入院費はDPC(診断群分類包括評価)システムを使用して計算されます。このシステムは、患者の病名や治療内容に基づいて入院費を決定する方法です。以前の「出来高」方式とは異なり、DPCシステムでは多くの診療行為が1日あたりの定額に含まれます。
DPCシステムの主な特徴
- 約1,400の診断群に分類される
- 1日あたりの定額制
- 一部の治療は従来通りの出来高計算が適用される
DPCシステムと出来高計算の比較表
| DPC(1日あたりの定額に含まれる項目) | 出来高計算項目 |
|---|---|
| 投薬 | 手術 |
| 注射 | リハビリ |
| 検査 | 特定の処置 |
| 画像診断 | |
| 入院基本料 |
DPCシステムの計算方法
計算式は以下の通りです:
「1日あたりの金額」×「入院日数」×「医療機関別係数」+「出来高計算分」
*医療機関別係数は各医療機関によって異なります。
例えば、患者が14日間入院した場合の計算は以下のようになります
DPC名: 神経異栄養症、骨成長障害、骨障害(その他) 手術なし
日数: 14
医療機関別係数: 0.0948 (例:神戸大学医学部附属病院)
入院費: ¥304,510 +出来高計算分
保険が適用されると、自己負担額は1割から3割になります。また、高額医療制度の対象となる場合、実際の自己負担額はさらに低くなります。
なお、上記の価格は2024年7月時点のものであり、最新の価格については随時ご確認ください。
経済的支援制度
治療費の負担を軽減するため、自治体独自の助成制度や民間の難病支援団体による援助プログラムがあります。
これらの制度を利用することで家計への影響を抑えることが可能です。
| 支援制度 | 概要 |
| 自治体助成 | 治療費の一部補助 |
| 民間団体支援 | 経済的・情報的サポート |
長期的な治療に伴う経済的負担に備えるため、早期からの情報収集と計画策定が不可欠です。
以上

- 参考にした論文




