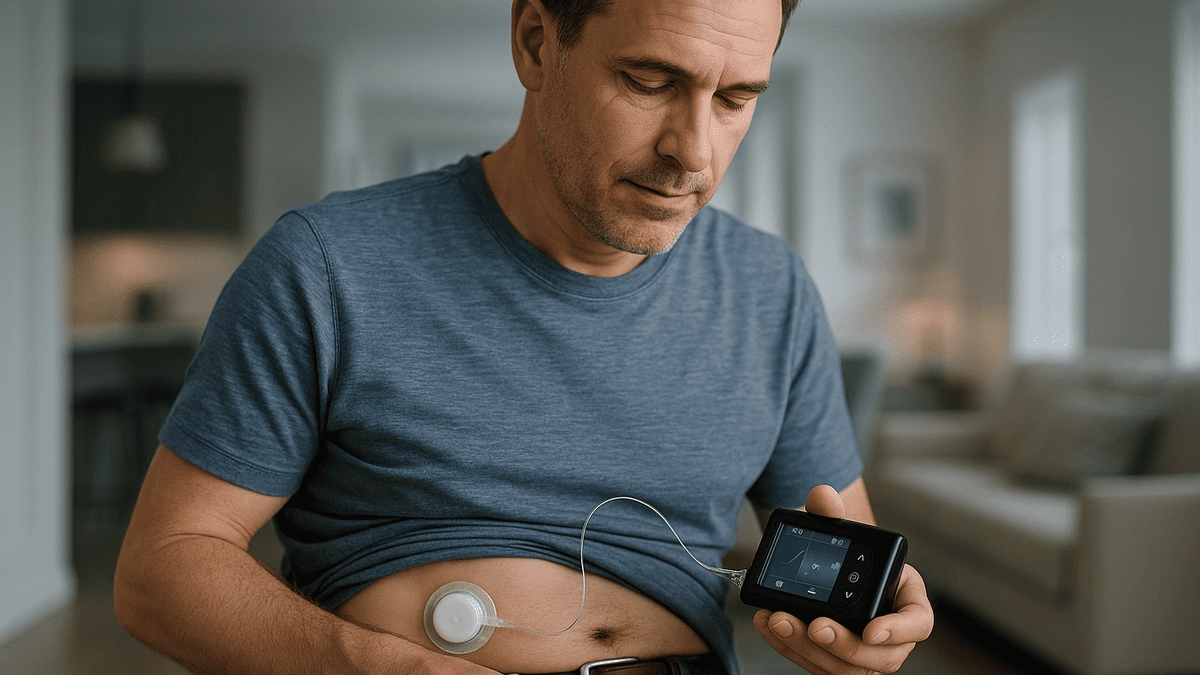
糖尿病のインスリン治療は血糖値をきめ細かくコントロールすることが重要です。近年、テクノロジーの進歩により、より精密な血糖管理を目指せる治療法が登場しています。その一つが「SAP療法」です。
SAP療法はインスリンポンプと持続血糖測定器を連携させることで、従来の治療法よりも安全かつ効果的に血糖値を安定させることを目指します。
この記事ではSAP療法がどのような糖尿病治療なのか、その仕組みやメリット、保険適用や費用について専門の観点から分かりやすく解説します。
SAP療法とは何か
SAP(Sensor Augmented Pump)療法は、日本語で「センサー付きインスリンポンプ療法」と訳します。インスリン治療を必要とする糖尿病患者様のための先進的な血糖管理方法の一つです。
インスリンポンプと持続血糖測定器(CGM)の融合
SAP療法は二つの医療機器を組み合わせて行います。
一つは、インスリンを24時間持続的に皮下へ注入する「インスリンポンプ」。もう一つは、皮下のグルコース値を5分ごとに測定し続ける「持続血糖測定器(CGM)」です。
この二つが連携し、血糖値の変動をリアルタイムで把握しながらインスリン注入量を調整します。
血糖値を「見える化」してインスリンを注入
従来のインスリン治療では指先から採血して血糖値を測定し、その値に基づいてインスリンを注射していました。
一方、SAP療法ではCGMが血糖値の「今の値」だけでなく「これからの変動傾向」も矢印で示します。
患者様や医療者はこの情報を基に、より的確なインスリン量の調整ができます。
従来のインスリン療法との違い
1日数回の注射と血糖測定を行う従来の治療法(MDI療法)と比べ、SAP療法は血糖コントロールの精度と安全性を大きく向上させます。
特に低血糖のリスクを減らしながら、血糖値を目標範囲内に維持しやすくなる点が大きな違いです。
SAP療法と従来のインスリン注射(MDI)との比較
| 項目 | SAP療法 | MDI療法 |
|---|---|---|
| 血糖測定 | 持続的(5分ごと) | 断続的(1日数回) |
| インスリン注入 | 持続的・微量調整可能 | 断続的(1日数回注射) |
| 低血糖予防 | 予測機能、自動停止機能あり | 自己判断による補食など |
SAP療法を構成する機器とその働き
SAP療法はインスリンポンプ、CGMセンサー、トランスミッターという3つの主要な機器で構成されます。それぞれの機器が連携して、精密な血糖管理を実現します。
インスリンポンプ本体
携帯電話ほどの大きさの装置で、インスリンのタンクとそれを送り出すポンプが内蔵されています。
あらかじめ設定したプログラムに従って、基礎インスリンを24時間持続的に注入します。食事の際に必要な追加インスリンも、ボタン操作で簡単に注入できます。
CGMセンサーとトランスミッター
CGMセンサーは腹部などに貼り付けた細い電極で、皮下の間質液中のグルコース濃度を測定します。
トランスミッターはセンサーに取り付け、測定したグルコース値のデータを無線でインスリンポンプ本体へ送信する役割を担います。
SAP療法を構成する主な機器
| 機器 | 主な役割 | 装着場所の例 |
|---|---|---|
| インスリンポンプ | インスリンの注入 | ベルト、ポケット |
| CGMセンサー | グルコース値の測定 | 腹部、腕、お尻 |
| トランスミッター | 測定データの無線送信 | センサーに接続 |
機器同士の連携による血糖管理
インスリンポンプの画面にはCGMで測定された血糖値がリアルタイムでグラフ表示されます。これにより、血糖値が今どうなっているか、これからどう変動しそうかを視覚的に把握できます。
この「見える化」された情報が、SAP療法の大きな特徴です。
SAP療法が糖尿病治療にもたらす主なメリット
SAP療法は血糖コントロールの質を向上させるだけでなく、患者様の生活の質(QOL)にも多くの良い影響を与えます。
低血糖のリスクを大幅に低減
SAP療法の最大のメリットの一つが、危険な低血糖を予防できる点です。
CGMが血糖値の低下を予測するとポンプに警告を発し、設定によっては低血糖になる前にインスリンの注入を自動的に停止する機能(スマートガード機能)があります。
これにより、特に夜間の無自覚性低血糖のリスクを大きく減らすことができます。
より厳格で安定した血糖コントロールの実現
血糖値の変動を常時把握できるため、高血糖にも低血糖にも早めに対処できます。
食事や運動など生活の中での血糖変動パターンを学び、インスリン量をより細かく調整することで、血糖値を目標範囲内に維持する時間の割合(Time in Range)を高めることができます。
血糖コントロール指標の改善
| 指標 | SAP療法による改善効果 |
|---|---|
| HbA1c | 平均血糖値の低下による改善が期待できる |
| Time in Range | 目標範囲内(70-180mg/dL)の時間の延長 |
| 低血糖頻度 | 予測アラートと自動停止機能で減少 |
生活の質(QOL)の向上
1日数回の注射から解放されることや、低血糖への不安が軽減することは、精神的な負担を大きく減らします。
血糖変動を気にすることなく、食事や運動、旅行などをより自由に楽しめるようになり、生活の質が向上します。
SAP療法の対象となる方
SAP療法はインスリン治療を行うすべての方が対象となるわけではありません。その特性から、特に以下のような方に有用な治療法と考えられています。
血糖コントロールが不安定な1型糖尿病の方
インスリンを自己分泌できない1型糖尿病の方で、従来の注射療法では血糖値の変動が激しい(ブリットル型)場合、SAP療法は非常に良い適応となります。
無自覚性低血糖や夜間低血糖を繰り返す方
低血糖の症状を自覚できない「無自覚性低血糖」や、睡眠中に起こる「夜間低血糖」は、命に関わる危険な状態です。
SAP療法の低血糖予測機能や自動停止機能は、こうした方の安全を確保する上で大変重要です。
厳格な血糖管理を必要とする方
妊娠を計画している女性や妊娠中の糖尿病患者様、あるいは合併症の進行を抑えるために、より厳格な血糖コントロールが求められる方もSAP療法の良い適応です。
SAP療法の主な対象患者像
| 対象 | SAP療法が有用な理由 |
|---|---|
| 1型糖尿病 | 生理的なインスリン分泌に近い補充が可能 |
| 頻回低血糖 | 低血糖のリスクを予測・回避できる |
| 血糖変動大 | 変動パターンを把握し、細やかな調整が可能 |
SAP療法を始めるまでの流れ
SAP療法を始めるには専門の医療機関で相談し、適切な教育を受ける必要があります。安全に治療を継続するための大切な準備期間です。
専門医による診察と適応の判断
まずは糖尿病専門医が診察を行い、現在の血糖コントロールの状態や生活習慣、合併症の有無などを評価します。
その上で患者様本人の治療への意欲も確認し、SAP療法が適切かどうかを総合的に判断します。
機器の選択と使用方法の学習
SAP療法で用いる機器には複数の種類があります。医師や医療スタッフと相談しながら、ご自身のライフスタイルに合った機器を選択します。
その後、ポンプの操作方法、センサーやカニューレ(インスリン注入チューブ)の交換方法、トラブル時の対処法などについて時間をかけて学習します。
入院または外来での導入と調整
SAP療法の開始は多くの場合、数日間の教育入院を通じて行います。入院中に実際に機器を装着し、専門スタッフの指導のもとで操作に慣れていきます。
インスリンの基礎注入量(ベーサル)や、食事に対するインスリン量(ボーラス)の設定なども実際の血糖値の動きを見ながら細かく調整していきます。
施設によっては外来での導入も可能です。
SAP療法導入の主な学習内容
| 項目 | 学習内容の例 |
|---|---|
| 機器操作 | ポンプのボタン操作、メニュー設定 |
| 自己管理手技 | センサー・カニューレの交換、血糖測定 |
| 応用 | カーボカウント、シックデイルール |
SAP療法の保険適用と費用
SAP療法は健康保険が適用される治療法ですが、一定の条件を満たす必要があります。また、従来の治療法に比べて費用が高くなる傾向があります。
保険適用となる条件
SAP療法が保険適用となるのは、インスリン治療を必要とする糖尿病患者様のうち、「血糖コントロールが不安定である」と医師が判断した場合です。
具体的には1型糖尿病の患者様や、インスリンを分泌する能力が著しく低下している2型糖尿病の患者様などが対象となります。
月々の費用の目安
SAP療法にかかる費用は、インスリンポンプやセンサーなどの機器に関連する費用と、インスリン製剤や穿刺器具などの消耗品の費用からなります。
自己負担割合にもよりますが、3割負担の場合、月々の医療費は従来の注射療法よりも高額になります。
SAP療法の費用内訳(月額・3割負担の目安)
| 項目 | 費用の目安 |
|---|---|
| ポンプ・CGM関連費用 | 約15,000円〜25,000円 |
| インスリン・消耗品費用 | 約10,000円〜15,000円 |
| 合計 | 約25,000円〜40,000円 |
高額療養費制度などの活用
医療費の自己負担額が高額になった場合でも、「高額療養費制度」を利用することで、所得に応じて定められた上限額を超える分が払い戻されます。
また、1型糖尿病の患者様の場合は自治体独自の医療費助成制度の対象となることもあります。
詳しくは医療機関の相談員や加入している健康保険組合、市区町村の窓口にご確認ください。
SAP療法に関するよくある質問
最後に、SAP療法を検討されている患者様からよくいただく質問についてお答えします。
- Q機器をずっと身に着けていないといけませんか?
- A
はい、インスリンポンプとCGMセンサーは基本的に24時間装着し続ける必要があります。
ただし、インスリンポンプはカニューレとの接続を一時的に外すことができるため、入浴や着替え、スポーツなどの際には短時間であれば取り外しが可能です。
どのくらいの時間外せるかは主治医と相談してください。
機器の交換頻度の目安
機器 交換頻度 インスリン注入セット(カニューレ) 2〜3日に1回 CGMセンサー 約7〜14日に1回(機種による) インスリンポンプ本体 4年の保証期間で交換
- Qセンサーやカニューレの装着は痛いですか?
- A
センサーやカニューレを皮下に挿入する際にチクッとした軽い痛みを感じることがありますが、多くの場合、装着後はほとんど痛みや違和感はありません。
挿入を補助する器具(サーター)を使うことで、より簡単に痛みも少なく装着できます。
慣れるまでは少し戸惑うかもしれませんが、すぐに習熟できます。
- Q日常生活(入浴、運動)で気をつけることはありますか?
- A
多くのインスリンポンプには防水機能がありますが、CGMのトランスミッターは防水ではない場合があるため、入浴時はポンプを一時的に取り外すのが一般的です。
水泳などのスポーツも可能ですが、機器の固定方法や取り外しのタイミングについて事前に主治医や医療スタッフとよく相談しておくことが重要です。
- 入浴時:ポンプを一時的に外す
- 運動時:血糖値の変動に注意し、必要に応じて補食やインスリン量の調整を行う
- 機器の固定:汗などで剥がれないよう、テープなどで補強する
以上
参考にした論文
TAKAGI, Satoshi, et al. A sensor augmented pump may improve awareness of hypoglycemia and quality of life in Japanese patients with type 1 diabetes mellitus. Diabetology international, 2022, 13.1: 280-287.
TAMURA, Rie Kaneshima, et al. A sensor-augmented pump with a predictive low-glucose suspend system could lead to an optimal time in target range during pregnancy in Japanese women with type 1 diabetes. Diabetology international, 2024, 15.3: 447-455.
SUGAI, Keiji, et al. Successful introduction of sensor‐augmented pump therapy in a patient with diabetes and needle phobia: A case report. Journal of Diabetes Investigation, 2023, 14.11: 1318-1320.
AKIYAMA, Tomoaki, et al. Effects of hybrid closed‐loop system on glycemic control and psychological aspects in persons with type 1 diabetes treated with sensor‐augmented pump: a prospective single‐center observational study. Journal of Diabetes Investigation, 2024, 15.2: 219-226.
IMAFUKU, Hitomi, et al. Advantages of sensor‐augmented insulin pump therapy for pregnant women with type 1 diabetes mellitus. Journal of Diabetes Investigation, 2023, 14.12: 1383-1390.
NISHIHAMA, Kota, et al. Sudden death associated with severe hypoglycemia in a diabetic patient during sensor-augmented pump therapy with the predictive low glucose management system. The American Journal of Case Reports, 2021, 22: e928090-1.
SUGANUMA, Yuka, et al. Elevated urinary albumin predicts increased time in range after initiation of SGLT2 inhibitors in individuals with type 1 diabetes on sensor-augmented pump therapy. Diabetology International, 2024, 15.4: 806-813.
FUKUDA, Yuya, et al. Long-term sensor-augmented pump therapy for neonatal diabetes mellitus: a case series. Clinical Pediatric Endocrinology, 2022, 31.3: 178-184.
NOTEMI, Léonie Makuété, et al. Long-term efficacy of sensor-augmented pump therapy (Minimed 640G system) combined with a telemedicine follow-up in patients with type 1 diabetes: A real life study. Journal of Clinical & Translational Endocrinology, 2022, 30: 100306.
KOIDE, Keiko; AZUMA, Koichiro; ATSUMI, Yoshihito. Worsening of Glycemic Control in a Patient With Fulminant Type 1 Diabetes Receiving Sensor-Augmented Pump Therapy: A Case of Extensive Localized Lipoatrophy Requiring Attention in Relation to Cannula Insertion Sites. Clinical Diabetes, 2022, 40.1: 125-128.